实验2-2 海水的蒸馏 知识点题库
-
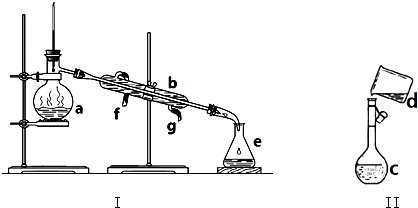
(1) 写出下列仪器的名称:
a. b. c..
-
(2) 仪器a~e中,使用前必须检查是否漏水的有.(填序号)
-
(3) 若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是,将仪器补充完整后进行实验,冷凝水由(填f或g)口通入.
-
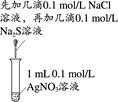
(4) 现需配制1mol•L﹣1 NaCl溶液100mL,装置II是某同学转移溶液的示意图.
①图中的错误是.除了图中给出的仪器和托盘天平外,为完成实验还需要的仪器有:.
②根据计算得知,所需称量NaCl 的质量为g.
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次).
A.用少量蒸馏水洗涤烧杯和玻璃棒2﹣3次,洗涤液均注入容量瓶
B.将称好的氯化钠固体放入烧杯中,再加入适量蒸馏水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氯化钠溶液注入100mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1﹣2cm处
-
(5) 试分析下列操作对所配溶液的浓度有何影响(填:增大、减少、或无影响)
①容量瓶用蒸馏水洗净后没有干燥就直接用来配溶液,对所配溶液浓度的影响:;
②定容时,俯视刻度线,对所配溶液浓度的影响:;
-
(6) 若该NaCl溶液的密度是1.17g•cm﹣3则该溶液中NaCl的质量分数是;
-
(7) 取出该NaCl溶液10mL加水稀释到100mL,稀释后溶液中NaCl的物质的量浓度是.
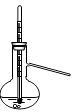 B .
B . 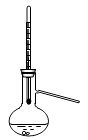 C .
C . 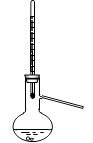 D .
D . 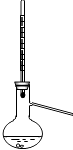
|
相对分子质量 |
熔点/℃ |
沸点/℃ |
密度/g•cm-3 |
溶解性 |
|
|
二苯基羟乙酮 |
212 |
133 |
344 |
1.310 |
不溶于冷水,溶于乙醇 |
|
二苯基乙二酮 |
210 |
97 |
348 |
1.084 |
不溶于水,能溶于乙醇 |
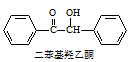 +2FeCl3
+2FeCl3 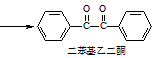 +2FeCl2+2HCl
+2FeCl2+2HCl
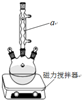
在反应装置中,加入10mL冰醋酸、5.50g FeCl3固体、10mL水及少量碎瓷片,加热至沸腾,停止加热,待沸腾平息后加入2.12g二苯基羟乙酮,继续加热回流至二苯基羟乙酮完全反应。反应结束后加水煮沸,冷却后即有二苯基乙二酮粗产品析出,用70%乙醇水溶液重结晶提纯,得到1.80g产品。
重结晶过程如下:
加热溶解→活性炭脱色→趁热过滤→冷却结晶→抽滤→洗涤→干燥
请回答以下问题:
-
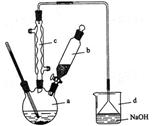
(1) 装置图中仪器a的名称是,其作用是。
-
(2) 加入碎瓷片的作用是。若加热后发现未加碎瓷片,应采取的正确方法是。
-
(3) 实验中可采用薄层色谱跟踪反应进程,其原理和操作与纸上层析类同,通过观察薄层色谱展开后的斑点(在实验条件下,只有二苯基羟乙酮和二苯基乙二酮能够产生斑点)判断样品中的成分。如图分别为加入二苯基羟乙酮后反应开始、回流15min、30min、45min和60min时,用毛细管取样、点样,薄层色谱展开后的斑点:

该实验条件下加热____后可认为反应结束。
A . 15min B . 30min C . 45min D . 60min -
(4) 上述重结晶过程中,(填步骤名称)操作除去了不溶性杂质。
-
(5) 在重结晶过程中,不可选用明火直接加热,原因是。
-
(6) 不选择蒸馏的方法提纯二苯基乙二酮粗产品的原因是。
-
(7) 本实验的产率是%。(保留3位有效数字)
 检验溶液中是否含有K+
B .
检验溶液中是否含有K+
B . 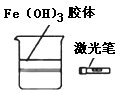 用激光笔照射Fe(OH)3胶体,产生丁达尔效应
C .
用激光笔照射Fe(OH)3胶体,产生丁达尔效应
C . 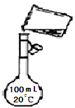 转移溶液
D .
转移溶液
D . 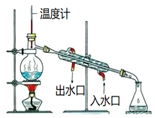 分离乙醇(沸点为78.3℃)和苯(沸点为80.1℃)的混合物
分离乙醇(沸点为78.3℃)和苯(沸点为80.1℃)的混合物
| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
按以下合成步骤回答问题:
-
(1) 在a中加入15 mL苯和少量铁屑。在b中小心加入4.0 mL 液溴。再将b中液溴慢慢加入到a中,充分反应。装置a中发生的主要反应是;装置d的作用是。
-
(2) 反应过程中,a外壁温度升高,为提高原料利用率,采取以下措施:
①采用装置c的目的是。
②利用温度计控制温度,适宜的温度范围为(填序号)。
A.>156℃ B. 59℃-80℃ C.<59℃
-
(3) 液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。
操作②所需要的玻璃仪器除烧杯外,还需,滤液用NaOH溶液洗涤的作用是;
③向分离出的粗溴苯中加入少量的无水氯化钙,静置、过滤。
-
(4) 经过上述分离操作后,粗溴苯中溶解的主要杂质为苯,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母)。A . 重结晶 B . 过滤 C . 蒸馏 D . 萃取
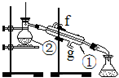
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示
-
(1) 写出下列仪器的名称:① ②
-
(2) 若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是,将仪器补充完整后进行的实验操作的名称是;①的进水口是 (填“f”或“g”)
-
(3) 仪器②中常加入碎瓷片,这样做的目的是
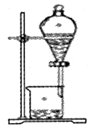
实验二:用CCl4从碘水中萃取I2并分液漏斗分离两种溶液.
其实验操作中有如下两步:
①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔.
②静置分层后,旋开活塞,用烧杯接收下层液体
-
(4) 下层流出的是溶液,上层液体从 得到(填“上口”或“下口”)
-
(5) 萃取碘水中的I2单质时要用到萃取剂,下列关于所加萃取剂的说法正确的是(______)A . 不与碘反应 B . 碘在其中的溶解度大于在水中的溶解度 C . 该萃取剂与水不互溶且密度不同 D . 可以选用CCl4、 酒精做萃取剂.
| | | | |
| A.制备并收集乙酸乙酯 | B.证明氯化银溶解度大于硫化银 | C.验证溴乙烷的消去产物是乙烯 | D.推断S、C、Si的非金属性强弱 |
| A.分离水和乙醇 | B.除去水中的泥沙 | C.从食盐水中获取氯化钠固体 | D.用自来水制取蒸馏水 |
| | | | |
NaBr+H2SO 4 =HBr+NaHSO4 ①
R—OH+HBr→ R—Br+H2O②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br- 被浓硫酸氧化为 Br2等。有关数据列表如下:
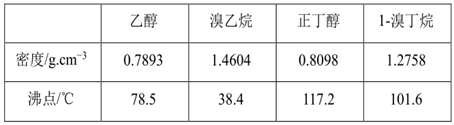
请回答下列问题:
-
(1) 在蒸馏过程中,仪器选择及安装都正确的是(填标号)。
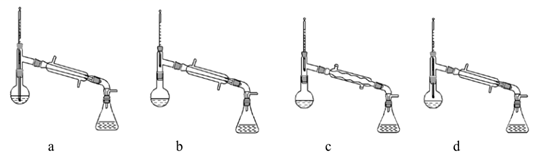
-
(2) 醇的水溶性(填“大于”、“等于”或“小于”)相应的溴代烃。
-
(3) 将 1溴丁烷粗产品置于分液漏斗中加水,振荡后静置,水在(填“上层”“下层”或“不分层”)。
-
(4) 制备操作中,加入的浓硫酸必须进行稀释,其目的是(填字母)。
a.水是反应的催化剂 b.减少 Br2 的生成
c.减少 HBr 的挥发 d.减少副产物烯和醚的生成
-
(5) 欲除去溴乙烷中的少量杂质 Br 2 ,下列物质中最适合的是(填字母)。
a.NaI b.KCl c.NaOH d.NaHSO 3
-
(6) 在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于;但在制备 1溴丁烷时却不能边反应边蒸出产物,其原因是。
①从碘水中提取单质碘时,可用无水乙醇代替CCl4
②可以用NaOH溶液除去溴苯中的溴杂质
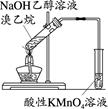
③用酸性KMnO4溶液可以除去乙烯中混有的乙炔
④实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法
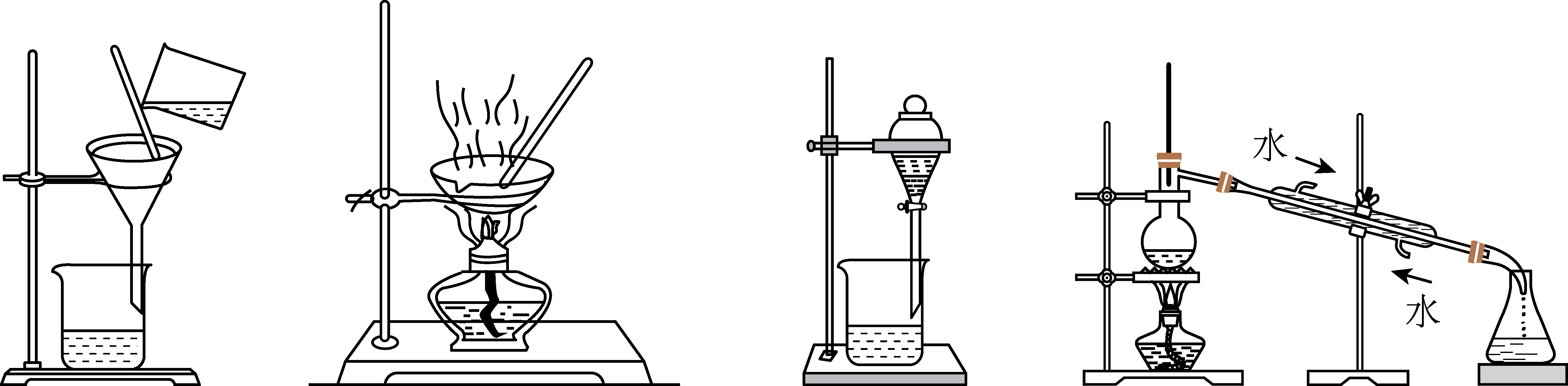
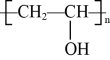 )是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示:
)是重要的化工原料,常用于制造聚乙烯醇缩醛、耐汽油管道、粘合剂等。其制备的工业流程如图所示: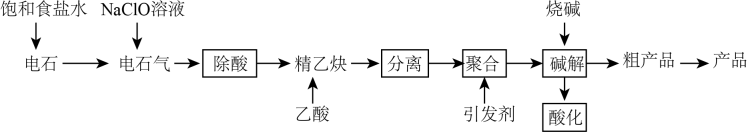
已知:①电石气中通常含有H2S、PH3等杂质②电石气通入次氯酸钠溶液后反应后,溶液仍澄清③乙炔较易与羧酸反应生成酯
回答下列问题:
-
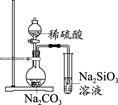
(1) 制取电石气时用饱和食盐水代替水的目的是,电石气通入NaClO溶液发生的主要反应的离子方程式为(写一个即可)。
-
(2) 分离过程中采取的主要操作名称为。
-
(3) 碱解时发生反应的化学方程式为,流程图中可循环利用的物质为。
-
(4) 电石常用CaO与碳素材料在1800~2200℃的高温下制备,甲烷在高温下(1300~1500℃和氧不足的条件下燃烧时所放出的热量可使甲烷发生反应生成乙炔。与电石制乙炔相比,该方法的优点是(写一条即可),若标准状况下22.4m3甲烷可得到聚乙烯醇产品13.2kg,则甲烷的转化率为。
- 物质和运动的辩证关系是( ) A、物质是运动的主体 B、所有的物质都是运动的 C、所有的运动都是物质的运动 D、
- 在给定条件下,下列加点的物质在化学反应中完全消耗的是() A.用浓盐酸与过量的二
- 进入3G时代,消费者最关心的是3G手机的价格和资费能否承受,下列选项中影响3G手机消费的因素是 ①商品的价格 ②商品的质
- 图3为用瓶起开启瓶盖的情景,图4中关于该瓶起使用时的杠杆示意图正确的是( )
- 如下图,在四边形ABCD中,AB=CD,BA和CD的延长线交于点E,若点P使得S△PAB=S△PCD,则满足此条件的点P
- 法兰西第五共和国总统戴高乐提出:争取实现“欧洲人的欧洲”的目标,反对美国在西方联盟中的霸权等。二战后“美国在西方联盟中霸
- 下列各项没有错别字的一项是( )A.溃退 杀戮 响彻云宵 B.鞠躬 瓦砾 富丽堂皇 C.建忘 阻遏 眼花嘹乱 D.泻气
- (本题满分8分)已知是常数),且(为坐标原点). (1)求函数的单调递增区间; (2)若时,的最大值为4,求的值;
- “”是一场给党、国家和各族人民带来深重灾难的内乱。要避免“文革”悲剧的重演,主要在于 A.以德治国
- 光导纤维的主要成分是 A、二氧化硅 B、单质硅 C、硅酸盐 D、铝的合金
- 右图是元素周期表中的一格,从中获取的信息不正确的是( ) A.该元素的原子序数为18 B.该元素
- 下图所示的实验操作正确的是( )
- Helen ______ to a language school when she wasseven.
- )重量为G1的均匀球夹在光滑竖直平面和45°倾角的光滑斜块之间,如图所示,斜块重G2,斜块侧面与水平桌面间的摩擦系数为m
- 以下各项的一组风带中,风向相同的有( )。 A.南半球的信风带与北半球的信风带 B.北半球的极地东风带与南半球的极
- 下列叙述中不是无机盐在细胞中的作用的是 A.它是某些复杂化合物的重要成分 B.它能维持生物体的生命活动 C
- (08年北京卷)假如全世界60亿人同时数1 g水的分子个数,每人每小时可以数5000个,不间断地数,则完成任务所需时间最
- 下列各类有机物:①饱和一元醇 ②饱和一元醛 ③饱和一元羧酸 ④饱和一元醇与饱和一元酸生成的酯 ⑤乙炔的同系物 ⑥苯的同系
- 22.在下面一段文字横线处补写恰当的语句,使整段文字语意完整连贯,内容贴切,逻辑严密。每处不超过15个字。报告文学的力量
- .根据下列表格的对应值: 3.23 3.24 3.25 3.26-0.06 -0.02 0.03 0.09判断方程(≠0