课题3 纯碱的生产 知识点题库
下列关于工业生产的说法正确的是( )
A . 在侯氏制碱工业中,向饱和氯化钠溶液中先通二氧化碳,后通氨气
B . 在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率
C . 在氯碱工业,电解槽一般用铁网作电极
D . 合成氨工业用天然气造气的方法中,与水蒸汽高温反应优于热分解法
侯氏制碱法是连续循环生产的过程,主要流程见图,有关该流程的叙述中正确的是( )
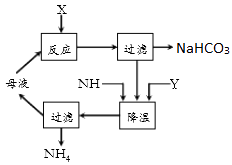
A . 母液中含有大量的Na+、NH4+、Cl﹣、CO32﹣
B . 通入NH3只是为了增加NH4+浓度
C . 加入的Y物质为CO2
D . 生产过程中还需要补充水
我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.如图是在实验室进行模拟实验的生产流程示意图:气体A的饱和溶液 A和食盐的饱和溶液
A和食盐的饱和溶液 悬浊液
悬浊液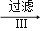 晶体
晶体 纯碱,则下列叙述错误的是( )
纯碱,则下列叙述错误的是( )
 A和食盐的饱和溶液
A和食盐的饱和溶液 悬浊液
悬浊液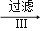 晶体
晶体 纯碱,则下列叙述错误的是( )
纯碱,则下列叙述错误的是( )
A . A气体是NH3 , B气体是CO2
B . 第Ⅲ步得到的晶体是发酵粉的主要成分
C . 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D . 第Ⅳ步操作的主要过程有溶解、蒸发、结晶
下列有关物质工业制法的反应原理错误的是( )
A . 侯氏制碱:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓ 2NaHCO3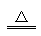 Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O
Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2
H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2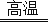 CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融)
CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
 Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O
Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2
H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2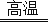 CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融)
CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
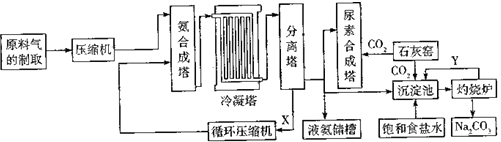
氨气、尿素[CO(NH2)2]、Na2CO3均是重要的化工原料和产品,如图是某化工厂联合生成氨气、尿素[CO(NH2)2]、纯碱的部分工艺流程图.
-
(1) 原料气进入压缩机前需要进行净化处理,其目的是.制备氨合成塔的材料(填“能”或“不能”)使用普通的碳素钢.
-
(2) N2、H2混合气体经压缩后再送入氨合成塔,优点是. 某整个生产中循环使用某些原料可提高生产效益,能循环利用的物质是.
-
(3) 请按要求填写下列空白.
①沉淀池中的离子方程式:.
②生产尿素的化学方程式:.
-
(4) 在较低温度下,可从沉淀池的溶液中分离出一种副产品由此可推断,低温下NH4Cl的溶解度很可能(填“小于”或“大于”)NaCL.NH4Cl是一种氮肥,但长期施用易使土壤酸化,用离子方程式表示其原因.
-
(5) 以焦炭、水为原料制备H2 (碳转化为CO2 , 则1000g纯度为a%((杂质不与水反应)焦炭最多可制备 g尿素(已知合成氨时h2的利用率为b%、合成尿素时NH3的利用率为c%)
我国化学家侯德榜(如图)改进国外的纯碱生产工艺,生产流程可简要表示如图:
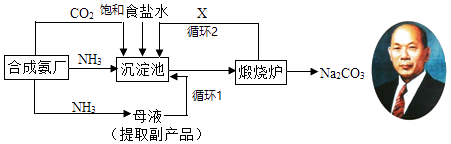
该生产纯碱的方法称联合制碱法或侯德榜制碱法联合制碱法或侯德榜制碱法,在制得纯碱的同时,还可得到一种副产品.
-
(1) 上述沉淀池中发生的化学反应方程式是,实验室分离出沉淀的操作是,该操作使用的玻璃仪器有;
-
(2) 写出上述流程中X物质的分子式;
-
(3) 使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 的循环(填上述流程中的编号1、2);
-
(4) 为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,还需要的试剂有;
-
(5) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品.通氨气的作用有 .A . 增大NH4+的浓度,使NH4Cl更多地析出 B . 使NaHCO3更多地析出 C . 使NaHCO3转化为Na2CO3 , 提高析出的NH4Cl纯度.
在精制饱和食盐水中加入碳酸氢铵可制备小苏打(NaHCO3),并提取氯化铵作为肥料或进一步提纯为工业氯化铵.
完成下列填空:
-
(1) 写出上述制备小苏打的化学方程式;
-
(2) 滤出小苏打后,母液提取氯化铵有两种方法:
①通入氨,冷却、加食盐,过滤
②不通氨,冷却、加食盐,过滤
对两种方法的评价正确的是(选填编号)
a.①析出的氯化铵纯度更高 b.②析出的氯化铵纯度更高
c.①的滤液可直接循环使用 d.②的滤液可直接循环使用
-
(3) 提取的NH4Cl中含少量Fe2+、SO42﹣ . 将产品溶解,加入H2O2 , 加热至沸,再加入BaCl2溶液,过滤,蒸发结晶,得到工业氯化铵.
加热至沸的目的是.滤渣的主要成分是、.
-
(4) 称取1.840g小苏打样品(含少量NaCl),配成250ml溶液,取出25.00ml用0.1000mol/L盐酸滴定,消耗盐酸21.50ml.实验中所需的定量仪器除电子天平外,还有.样品中NaHCO3的质量分数为.(保留1位小数)
-
(5) 将一定质量小苏打样品(含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量.若蒸发过程中有少量液体溅出,则测定结果.(选填“偏高”、“偏低”或“无影响”)
下列贡献与中国科学家无关的是( )
A . 创立侯氏制碱法
B . 发现青蒿素
C . 合成结晶牛胰岛素
D . 发明元素周期表
侯氏制碱法制备碳酸氢钠的原理为NH3+H2O+CO2 +NaCl=NH4Cl+NaHCO3↓,某化学小组用如图装置在实验室中模拟该制备过程,下列说法错误的是( )
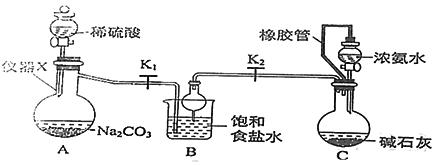
A . 装置A中仪器X的名称为蒸馏烧瓶
B . 装置B中球形干燥管的作用是防止倒吸
C . 装置C中橡胶管的作用是平衡压强,使溶液顺利滴下
D . 实验开始后,应先打开K1一段时间,然后再打开K2
某化学小组参观制碱厂后,绘制了该厂生产纯碱的工艺流程图如图。据图判断下列说法错误的是( )
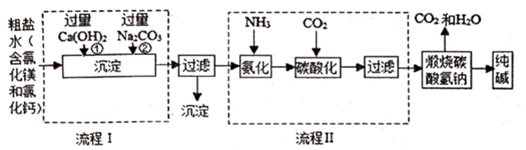
A . 流程图Ⅰ是依次向粗盐水中加入Ca(OH)2和Na2CO3 , 二者加入的顺序可以颠倒
B . 流程Ⅰ后过滤得到的沉淀成分有Mg(OH)2和CaCO3
C . 通入NH3的主要作用是形成碱性溶液,有利于CO2的吸收
D . 碳酸氢钠首先从溶液中结晶析出的原因其溶解度较小
关于下列工业生产过程,说法正确的是( )
A . 工业上电解冶炼铝,由于Al2O3熔点高,可用AlCl3代替
B . 氯碱工业中,选用阳离子交换膜,除了平衡电荷的作用外还可避免气体产物接触出现危险
C . 侯氏制碱法中,在沉淀池中反生反应时,应向饱和食盐水中先通二氧化碳后通氨气
D . 生产普通玻璃的主要原料为石灰石、纯碱和晶体硅
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列说法正确的是( )
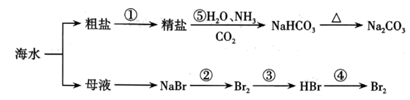
A . 步骤①是指蒸发结晶
B . 步骤⑤是先通CO2再通NH3
C . 在步骤②、③、④中,溴元素均被氧化
D . 制取NaHCO3的反应是利用其溶解度在常温下小于NaCl和NH4HCO3
下列说法正确的是( )
A . 纯碱因碱性过强,不可用于食品工业
B . 分子筛只能用于气体混合物的分离、提纯
C . 新制氯水呈酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
D . 合金的性能可以通过所添加合金元素的种类、含量和生成合金的条件等加以调节
现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下:
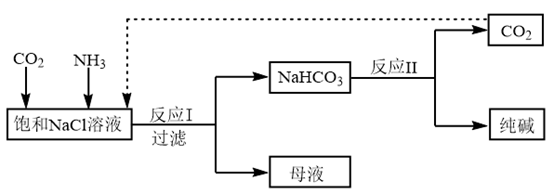
已知:常温常压下,1体积水能溶解1体积CO2;1体积水能溶解700体积NH3。下列有关说法错误的是( )
A . 反应I原理为CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl
B . 反应I生成的沉淀,经过滤、洗涤、煅烧可得到纯碱
C . 向饱和NaCl溶液中先通入足量的CO2 , 再通入足量的NH3
D . 从母液中可获得副产品氯化铵
如图是某小组模拟“侯氏制碱法”实验时所用到的部分装置。下列叙述错误的是( )
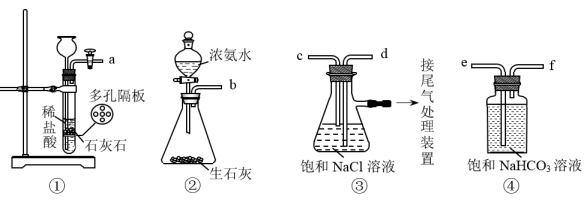
A . 侯氏制碱法的关键反应为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
B . 实验时先从装置③的d口通入足量NH3 , 再从c口通入足量CO2
C . 若改用稀H2SO4和碳酸钙粉末制取CO2 , 其发生装置可选用装置②
D . ④是连接在装置①与装置③之间的气体净化装置,进气口是e
-
(1) I.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:
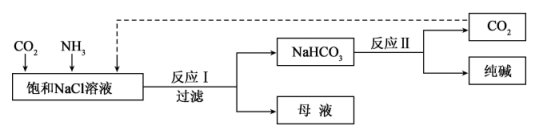
已知NaHCO3在低温下溶解度较小。
反应I的化学方程式为。
-
(2) 反应II的化学方程式为。
-
(3) II.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中Na2CO3的含量。
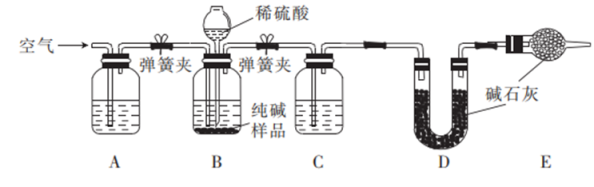
检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若,说明装置不漏气。
-
(4) 装置A中的试剂为,装置C中的试剂为。
-
(5) 实验结束后通入空气的目的:。
-
(6) 实验前称取28.80g样品,实验后测得D装置增重8.80g,则样品中Na2CO3的质量分数为(保留小数点后一位);若缺少E装置,会使测定结果(填“偏高”或“偏低”)。
下列关于物质制备的说法正确的是( )
A . 可用电解饱和食盐水的方法制取金属钠
B . 侯氏制碱法的原料有食盐、氨、二氧化碳,最终制得碳酸钠
C . 工业上主要用Na2O和H2O反应制取NaOH
D . 工业上用氯气与澄清石灰水反应制取漂白粉
某探究活动小组根据侯德榜制碱原理,按下面设计的方案制备碳酸氢钠。实验装置如图所示(图中夹持、固定用的仪器未画出)。下列说法正确的是( )
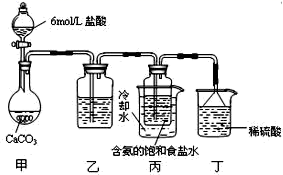
A . 乙装置中盛放的是饱和食盐水
B . 丙装置中的溶液变浑浊,因有碳酸氢钠晶体析出
C . 丁装置中倒扣的漏斗主要作用是防止产生的气体污染空气
D . 实验结束后,分离碳酸氢钠的操作是蒸发结晶
在实验室模拟侯氏制碱法制备碳酸钠,并测定碳酸钠的质量分数。
-
(1) 一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2 , 一段时间后,出现沉淀,过滤得到NaHCO3晶体。该过程的化学方程式为:。
-
(2) 加热 NaHCO3的化学方程式为,实验室进行此操作的装置可以是图中的。
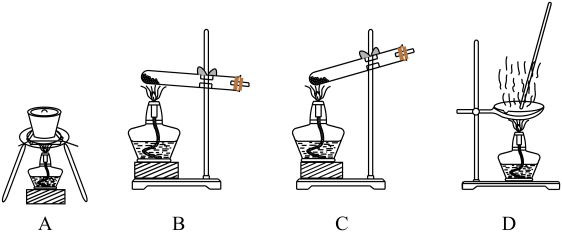
-
(3) 称取
 制得的碳酸钠样品,置于小烧杯中,加水溶解,向小烧杯中滴加足量氯化钙溶液充分反应(杂质不参加反应)。将反应混合物过滤、洗涤、干燥,得到质量为
制得的碳酸钠样品,置于小烧杯中,加水溶解,向小烧杯中滴加足量氯化钙溶液充分反应(杂质不参加反应)。将反应混合物过滤、洗涤、干燥,得到质量为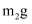 的沉淀。则该样品中碳酸钠的质量分数为(用
的沉淀。则该样品中碳酸钠的质量分数为(用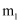 ,
, 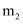 的计算式表示)。
的计算式表示)。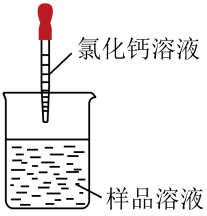
在纯碱工业的发展史上,法国的路布兰、比利时的索尔维和我国的侯德榜等科学家都取得了卓越的成就。
-
(1) 【方法一】路布兰以食盐、浓硫酸、焦炭和石灰石为原料,制得了纯碱。其反应原理为
①2NaCl+H2SO4(浓)
 Na2SO4+2HCl
Na2SO4+2HCl②2Na2SO4+4C
 Na2S+4CO↑
Na2S+4CO↑③Na2S+CaCO3
 Na2CO3+CaS
Na2CO3+CaS写出反应③的基本反应类型
-
(2) 用单线桥法表示反应②的电子转移方向和数目
-
(3) 【方法二】索尔维和侯德榜又发明了新的制碱方法,其模拟流程如下:
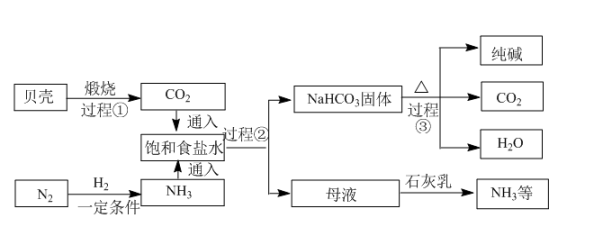
【资料查阅】
I.通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳。
Ⅱ.饱和食盐水中发生的主要反应为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。
上述流程中过程②的主要操作的名称是,可以循环利用的物质是(填化学式)。
-
(4) 写出饱和食盐水中主要反应的离子方程式
-
(5) 为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入(填“NH3”或“CO2”),你的理由是。
-
(6) 母液的主要成分为NH4Cl和NaCl,写出在加热条件下母液与石灰乳反应的化学方程式。
最近更新
- 某种烃A的蒸气折合成标况下的密度是3.214g/L,已知该烃的碳氢质量比为5∶1,求:(1)确定该烃的分子式:_____
- 我国各民族共同缔造了伟大的祖国,下列表述正确的是 ①祖国统一大业是各族人民共同完成的 ②祖国灿烂的文化是各族人民共同创造
- 下列物质属于合金的是________ A.黄金 B.黄铜 C.赤铁矿 D.________
- 下图是实验室制取气体的一些装置,据图回答有关问题。(友情提示:以下所选装置均填装置序号)(1)写出一个初中化学中用装置B
- 阅读下文,完成第1—6题。 湖 革 周美兰 ①湖草被人关注的季节,就是湖草成熟的季节。就像鄱阳湖畔的黄毛丫头,忽然长成
- 楚汉相争末期,汉王刘邦派谋士在项王必经之地“召集”蚂蚁排出“项王必死于此地”几个字,项王因此被攻破心理防线.在这一事件中
- 实施“走出去”战略是我国对外开放新阶段的重大举措,只有“引进来”与“走出去”同时并举,中国经济才能在更大范围内和更高层次
- 培根说“知识就是力量不仅取决于其本身价值的大小,更取决于它是否被传播,以及传播的深度和广度。”这句名言强调了() A.文
- The fact is _______ I have lost his address.
- 秦始皇、汉武帝、唐玄宗等都曾到泰山举行过封禅大典。《五经通义》云:“易姓而王,致太平,必封泰山,禅梁父,何天命以为王,使
- 下图反映的历史事件对中国产生的影响是( ) A. 标志着中国开始对外开放
- 23.贯穿于思想、理论、“三个代表”重要思想的主线是 A.坚持以经济建设为中心,大力发展生产力 B.反对机会主义
- .某无色溶液可能由氯化钙、氢氧化钠、氯化钠、碳酸钠、硫酸钠溶液中的一种或几种混合而成,为探究其组成,小明同学进行了如下实
- (2015届广西柳州中考)阅读下面文段,完成后面题目。 温暖心窝的话语 包利民 ①初中时,语文老师是个严厉的中年女人,姓
- 艾滋病(AIDS)被称为“人类的杀手”,它由艾滋病(AIDS)病毒引起并主要通过血液 进行传播,至今人类还没有找到根治该
- “可怜赵军作坑魂,自此群雄不敢西”说的是下列哪次战役( ) A.城濮之战 B.桂陵之战
- 从下面两题中任选一题作文。 (1)生活中,有很多触动我们心灵的力量:日月交辉,草长莺飞.,蓓蕾初绽;父母的深情,老师的教
- 下列词语中没有错别字的一项是() A.吞噬 模糊 畏缩不前 风餐露宿 B.销蚀 轨道 语无沦次 本
- 直线y=k(x+1)+1(x∈R)与椭圆=1恒有公共点,且椭圆焦点在x轴上,则m的取值范围是__________.
- 下列官职中,只有文官才能担任的是 A.秦朝的郡守 B.北宋的知州 C.明朝的布政司 D.清朝的巡抚



