第一单元 走进化学工业 知识点题库
-
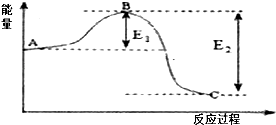
(1) 由图可知该反应为(填“吸热”或“放热”)反应.
-
(2) 该反应通常用V2O5作催化剂,加入V2O5会使图中E1(填“增大”、“减小”或“不变”),加入V2O5 后该反应的△H(填“增大”、“减小”或“不变”).
-
(3) 已知,2H2S(g)+O2(g)═2S(s)+2H2O(g)△H=﹣442.4kJ/mol ①
S(s)+O2(g)═SO2(g)△H=﹣297.0kJ/mol ②
H2S(g)与O2(g)反应产生SO2(g)和H2O(g)韵热化学方程式是.

回答下列问题:
-
(1) Ⅰ.环己烯的制备与提纯
原料环己醇中若含苯酚杂质,检验试剂为,现象为。
-
(2) 操作1的装置如图所示(加热和夹持装置已略去)。
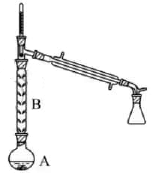
①烧瓶A中进行的可逆反应化学方程式为,浓硫酸也可作该反应的催化剂,选择
 而不用浓硫酸的原因为(填序号)。
而不用浓硫酸的原因为(填序号)。a.浓硫酸易使原料碳化并产生

b.
 污染小、可循环使用,符合绿色化学理念
污染小、可循环使用,符合绿色化学理念c.同等条件下,用
 比浓硫酸的平衡转化率高
比浓硫酸的平衡转化率高②仪器B的作用为。
-
(3) 操作2用到的玻璃仪器是。
-
(4) 将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,,弃去前馏分,收集83℃的馏分。
-
(5) Ⅱ.环己烯含量的测定
在一定条件下,向
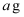 环己烯样品中加入定量制得的
环己烯样品中加入定量制得的 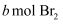 ,与环己烯充分反应后,剩余的
,与环己烯充分反应后,剩余的 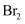 与足量
与足量  作用生成
作用生成  ,用
,用  的
的  标准溶液滴定,终点时消耗
标准溶液滴定,终点时消耗  标准溶液
标准溶液  (以上数据均已扣除干扰因素)。
(以上数据均已扣除干扰因素)。测定过程中,发生的反应如下:
①
②

③
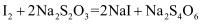
滴定所用指示剂为。样品中环己烯的质量分数为(用字母表示)。
-
(6) 下列情况会导致测定结果偏低的是(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.
 标准溶液部分被氧化
标准溶液部分被氧化
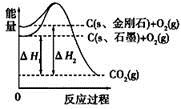
下列说法或表示式正确的是( )
| 实验操作 | 实验现象 | 结论 | |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后溶液中出现气泡,随后有红褐色沉淀生成 | Fe3+催化H2O2分解产生O2 |
| C | 铝片先用砂纸打磨,常温下再加入到浓硝酸中 | 无明显现象 | 常温下,铝不跟浓硝酸反应 |
| D | 向浓度均为0.01mol·L-1的KCl、KI的混合液中逐滴滴加稀AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
 2NH3(g)ΔH=-92.2kJ/mol,此温度下,将1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
2NH3(g)ΔH=-92.2kJ/mol,此温度下,将1molN2和3molH2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(忽略能量损失)( )
 O2(g)=H2O(g) ΔH=-241.8kJ·mol-1 , 该正反应的活化能为167.2kJ·mol-1 , 则其逆反应的活化能为kJ·mol-1
O2(g)=H2O(g) ΔH=-241.8kJ·mol-1 , 该正反应的活化能为167.2kJ·mol-1 , 则其逆反应的活化能为kJ·mol-1 ⑵某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:3A(g)+2B(g)  4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),平衡后加入C,B的平衡转化率(增大、减少、不变)。
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),平衡后加入C,B的平衡转化率(增大、减少、不变)。
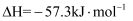 ,分别向
,分别向 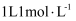 的①
的①  、②
、②  、③
、③  的稀溶液中加入
的稀溶液中加入 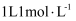 的
的  溶液,完全反应的热效应
溶液,完全反应的热效应  、
、  、
、  的关系正确的是(已知弱酸电离时吸热)( )
的关系正确的是(已知弱酸电离时吸热)( )
 B .
B .  C .
C .  D .
D . 
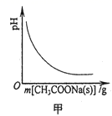 B . 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
B . 图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b 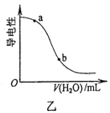 C . 图丙表示催化剂能改变化学反应的焓变
C . 图丙表示催化剂能改变化学反应的焓变 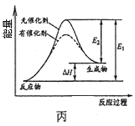 D . 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)
D . 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)  N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0 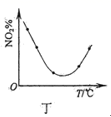
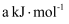 ,Br—Br键为
,Br—Br键为 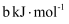 ,H—Br键为
,H—Br键为 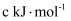 。一定温度下,反应
。一定温度下,反应 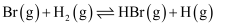
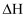 的反应历程与能量的关系如图所示。下列叙述正确的是( )
的反应历程与能量的关系如图所示。下列叙述正确的是( ) 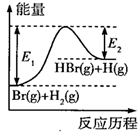
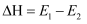 ,加入催化剂时,
,加入催化剂时, 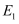 、
、 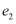 及
及 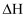 均减小
C . 已知
均减小
C . 已知 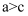 ,若反应
,若反应 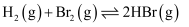
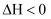 ,则
,则 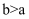 D . 升高温度,正逆反应速率均加快,且正反应速率加快的程度较大
D . 升高温度,正逆反应速率均加快,且正反应速率加快的程度较大
反应Ⅰ: ![]() +CH3OH
+CH3OH

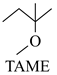 △H1
△H1
反应Ⅱ: ![]() +CH3OH
+CH3OH

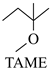 △H2
△H2
反应Ⅲ: ![]()

![]() △H3
△H3
回答下列问题:
-
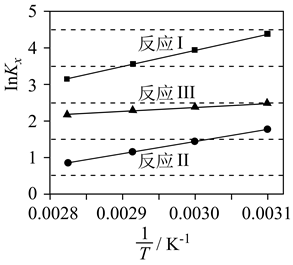
(1) 反应Ⅰ、Ⅱ、Ⅲ以物质的量分数表示的平衡常数Kx与温度T变化关系如图所示。据图判断,A和B中相对稳定的是 (用系统命名法命名);
 的数值范围是(填标号)。
的数值范围是(填标号)。
A.<-1 B.-1~0 C.0~1 D.>1
-
(2) 为研究上述反应体系的平衡关系,向某反应容器中加入1.0molTAME,控制温度为353K,测得TAME的平衡转化率为α。已知反应Ⅲ的平衡常数Kx3=9.0,则平衡体系中B的物质的量为mol,反应Ⅰ的平衡常数Kx1=。同温同压下,再向该容器中注入惰性溶剂四氢呋喃稀释,反应Ⅰ的化学平衡将 (填“正向移动”“逆向移动”或“不移动”)平衡时,A与CH3OH物质的量浓度之比c(A):c(CH3OH)=。
-
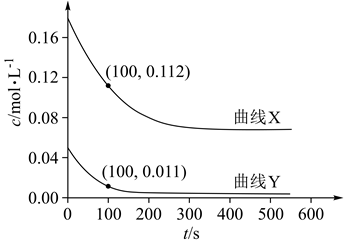
(3) 为研究反应体系的动力学行为,向盛有四氢呋喃的另一容器中加入一定量A、B和CH3OH。控制温度为353K,A、B物质的量浓度c随反应时间t的变化如图所示。代表B的变化曲线为 (填“X”或“Y”);t=100s时,反应Ⅲ的正反应速率v正逆反应速率v逆(填“>”“<”或“=)。
 D . 稀溶液中:HCl(aq)+NH3·H2O(aq)= NH4Cl(aq)+ H2O(l) ΔH = -57.3 kJ·mol-1
D . 稀溶液中:HCl(aq)+NH3·H2O(aq)= NH4Cl(aq)+ H2O(l) ΔH = -57.3 kJ·mol-1
- 下列反应的离子方程式正确的是 A.稀盐酸滴在石灰石上: CO32-+2H+ = CO2↑+H2O B.氯化铝
- 洋务运动时期,我国教育出现新的趋势和特点,它们是 ( )①逐渐由脱离实际向实用发展 ②
- (4分)在长度、质量、力、速度、温度、比热等物理量中,属于矢量的有______,属于标量的有______。
- (2012·南京盐城模拟)下表是《全世界区域性经济合作和一体化组织地区分布统计表》(1996年),从中可以得出的正确结
- 可视为点电荷的A、B两带电小球固定在真空中,所带电荷量均为+q ,若仅将A球所带电荷量变为-q ,则B球所受的库仑力
- 下列叙述中哪一种是正确的: A.所有的辅酶都包含维生素组分B.所有的维生素都可以作为辅酶或辅酶的组分 C.所有的B族维生
- (2014年山东烟台)科学家运用不同的研究方法揭开了自然的奥秘,设计对照实验来获得证据是常用的方法。下列研究不需要对照
- 新中国成立初期,政府合理调整工商业的最主要目的是( ) A.实现国家财政经济的根本好转 B.维护工
- 完形填空(共20小题;每小题1.5分,满分30分) 阅读下面短文,从短文后各题所给四个选项(A、B、C、D)中选出可以填
- --May I have a talk with one of your sports reporters?--Sorr
- 下列物质的用途中,利用其物理性质的是( ) A.铜用于制作导线 B.一氧化碳用于炼铁 C.天然气用作燃
- 用丙酮从口腔上皮细胞中提取脂质,在空气—水界面上铺成单分子层,测得单分子层面积为S1,设细胞膜表面积为S2,则S1与S2
- 如图15所示的杠杆处于平衡状态,若使弹黄秤的示数变为原来的1/2,杠杆仍然保持平衡状态,可以采取哪些措施? ()A、
- I don’t know__________.A. which sweater buy
- 秦朝时制定的法律细密严苛,实行“轻罪重罚”,古罗马《民法大全》规定“……不得基于怀疑而惩罚任何人。…与其判处无罪之人,不
- 离地面某一高度h处的重力加速度是地球表面重力加速度的,则高度h是地球半径的___________倍.
- 请你根据所学化学知识判断,不列说法正确的是 A.铁管在潮湿的空气中不易锈蚀 B.铵盐氮肥与碱性物质混合施用
- “宰相肚里能撑船,将军额头跑得马”,这一古语说的是 ①人与人之间的交往应该斤斤计较,耿耿于怀 ②为人处世应有博大的胸怀
- 如图是实验室常用的实验仪器与装置。依据题目要求回答下列问题:(1)制取氧气有很多种方法,如分解过氧化氢溶液、加热高锰
- Ihave no one ____ me, for I can deal with it all by myself.



