第10章 金属 知识点题库

Ⅰ 金属B的活动性金属D的活动性(填“>”、“<”、“=”);
Ⅱ 若A是一种气体化合物,写出①的化学方程式:;
Ⅲ 向C溶液中加入AgNO3溶液,有白色沉淀,加入稀硝酸,沉淀不溶解,写出其化学反应方程式:;
Ⅳ 写出溶液C与NaOH溶液反应的基本类型:。
-
(1) 钢铁锈蚀主要是铁与发生化学反应的结果,写出用可稀盐酸除去铁锈的化学方程式
-
(2) 不锈钢是铁、铬(Cr)、镍(Ni)的合金,常用来制造医疗器械、餐其等。通过实验得知,铬和镍两种金属都能与稀硫酸反应生成氢气,分別得到硫酸铬(CrSO4)和硫酸镍(NiSO4)溶液。请任意选取铬或镍中的一种,写出其与稀硫酸反应的化学方程式,并设计一种比较铁和铬金属活动性强弱的方法。
-
(1) (作出猜想)他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R,猜想二:R>Al>Cu,猜想三:。
-
(2) (查阅资料)R是一种银白色的金属,RSO4溶液呈蓝色;常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色。
(实验探究)为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究。
猜想
主要操作
主要现象
实验结论
一
打磨R丝,并将其插入到硫酸铜溶液中
R丝表面覆盖了一层红色的物质
猜想一(“成立”或“不成立”)
二
把铝丝插入RSO4溶液中
猜想二成立
三
打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中
①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色
②铝丝表面产生气泡较快
③铜丝表面没有气泡产生
猜想三成立
(交流反思)究竟哪种猜想成立?三位同学经讨论交流,发现乙同学在实验前没有打磨铝丝,这可能会导致实验结论错误。于是他们先打磨铝丝,再将其插入到RSO4溶液中,一段时间后,溶液的颜色由色变为色;进而确认猜想二不成立,猜想三成立。写出Al与稀硫酸反应的化学方程式:。
(归纳总结)探究结束后,他们总结得出:通过金属与酸反应或金属与盐溶液反应可以比较金属活动性强弱。
(查阅资料)①铬是银白色有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜:②能与稀硫酸反应,生成硫酸亚铬(CrSO4)。
(作出猜想)猜想①Cr>Fe>Cu;猜想②Fe>Cu>Cr;猜想③。
(设计与实验)①张明同学取大小相等的铁、铜、铬三种金属片,未经打磨就分别放入等量等浓度的稀硫酸中,记录如下:
|
实验操作 |
铁片放在稀硫酸酸中 |
铜片放在稀硫酸中 |
铬片放在稀硫酸中 |
|
开始的现象 |
有少量气泡产生 |
无气泡 |
无气泡 |
|
结论 |
金属活动性强弱:Fe>Cu,Fe>Cr |
||
②李红同学也取大小相等的铁、铜、铬三种金属片,先用砂纸打磨后再分别放入等量等浓度的稀硫酸中,记录如下:
|
实验操作 |
铁片放在稀硫酸中 |
铜片放在稀硫酸中 |
铬片放在稀硫酸中 |
|
开始的现象 |
产生少量气泡 |
无气泡 |
产生大量气泡 |
|
结论 |
金属活动性强弱:猜想成立 |
||
(讨论交流)为什么张明和李红两个同学记录的铬与稀硫酸反应开始的现象截然不同?
原因是。
(实验验证)为了进一步确认铁、铜、铬三种金属的活动性强弱,刘斌同学将打磨过的两块铁片分别放入硫酸亚铬(CrSO4)溶液和硫酸铜溶液中,观察到在硫酸亚铬溶液中无明显现象,而在硫酸铜溶液中有明显的现象是。
(拓展迁移)写出铬与稀硫酸反应,生成CrSO4的化学反应方程式。
-
(1) 合金和其成分金属相比,合金具有的优良性能之一是;
-
(2) 航天器内的导线常用铜制,主要是铜具有良好的性;
-
(3) 在一些钢铁制品表面喷涂一层油漆,不仅美观,更重要的是可防止钢铁生锈。铁生锈的条件是铁与和同时接触;
-
(4) 生铁和钢都是铁的合金,含碳量是两者重要的不同点之一,其中含碳量较高的是
。
 将一定质量的硫酸铜溶液倒入盛有铁钉的烧杯中
B .
将一定质量的硫酸铜溶液倒入盛有铁钉的烧杯中
B .  高温锻烧石灰石
C .
高温锻烧石灰石
C .  一定量的镁在过量的氧气中充分燃烧
D .
一定量的镁在过量的氧气中充分燃烧
D .  木炭还原氧化铜
木炭还原氧化铜
 如图
如图  ,游戏规则要求图中相邻物质之间能发生化学反应,其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原理之一。
,游戏规则要求图中相邻物质之间能发生化学反应,其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原理之一。 
-
(1) A物质的俗称是,E物质的用途是;
-
(2) B与C反应的化学方程式为。E与D反应的基本类型是。
-
(3) 按游戏规则,下列能替代B物质的是
 填序号
填序号  。
。 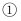 银
银 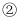 氯化铁
氯化铁 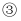 氯化钡
氯化钡 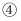 氧化铜
氧化铜
 2CuSO4+2H2O。
2CuSO4+2H2O。 
-
(1) 滤液②中溶质的化学式为 。
-
(2) 写出滤液③和铁粉发生反应的化学方程式 。
-
(3) Cu、Ag、Ni的金属活动性由强到弱的顺序是 。

-
(1) 实验开始时,应先(选填“通CO”或“加热”),其原因是。
-
(2) A处玻璃管中反应的化学方程式为。
-
(3) B处试管中产生的现象是,该装置还有一个不足之处是。
-
(1) “在金属活动顺序里,位于前面的金属能把位于后面的金属从其盐溶液里置换出来”,金属钠排在金属铜的前面。有的同学据此推测:钠能从蓝色硫酸铜溶液中把铜置换出来。
教师按照下列顺序进行演示实验,并记录实验现象:
步骤一:将硫酸铜溶液倒入培养皿中
步骤二:用镊子将一小块金属钠放入培养皿中
现象1:金属钠成小球状在液体表面游动
现象2:金属小球逐渐变小至消失,在小球游动的轨迹下面只有蓝色絮状难溶物出现
①由以上实验现象得出结论:因为反应中没有色的物质 生成,所以金属钠(填:“能” 或“不能”)把铜从硫酸铜溶液中置换出来。
②对实验涉及的物质进行分析:硫酸铜溶液中溶剂为水,溶质为(填化学式),钠与硫酸铜溶液反应后培养中皿所含元素有: Na、 Cu、 H、O、 (填元素 符号)五种元素。查阅资料得知:“ 蓝色絮状难溶物”是一种学过的碱,该物质的名称是。
-
(2) 有的同学又产生新的疑问:钠能否与水发生反应?生成物是什么?教师为解答学生的疑惑,又设计并进行如下实验。同时记录有关现象:
步骤一:向盛有蒸馏水的烧杯中滴入几滴酚酞试液并搅拌均匀
步骤二:用镊子将一小块金属钠放入烧杯中
现象:钠在液体表面成小球状游动并发出“嘶嘶”声响。小球周围有“蒸汽”产生,有时有火星出现,液体中出现红色。
请结合上面所示信息,回答下列问题:
①用手触摸反应后烧杯外壁,感觉烫手,说明钠与水发生的是 (填:“吸 热”或“放热”)反应。
②从现象中可以断定:液体中出现红色说明反应后液体显性,结合液体中所含元素,继而推断有(填化学式)生成。另外,钠与水反应还生成一种可燃性气体单质。请写出钠与水反应的化学方程式:。

-
(1) 生成氢气g;
-
(2) 所用稀硫酸的溶质质量分数是多少?(写出计算过程,计算结果保留到0.1%)
-
(1) 按金属的活动性顺序,铝比锌。但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究铝与酸反应的规律,小强用相同 质量、相同形状的光亮铝片设计如下实验。

实验一

实验二

实验三

实验四
实验 现象
铝表面产生气 泡很小且慢
铝表面产生大量气 泡
铝 表 面 产 生 大 量气泡
铝 表 面 产 生 大 量 气泡且快
-
(2) 比较实验三、实验四说明铝与酸反应产生氢气的速率,与有关。
-
(3) 比较实验一、实验二说明铝与酸反应产生氢气的速率,可能与、(填粒子符号)和温度、金属与酸液接触面积等多种因素有关。
-
(4) 写出实验二中发生反应的化学方程式。
-
(5) 小芳将长条状铝片的一端放在酒精灯火焰上灼烧片刻,轻轻摇动铝条,受热一端 会左右摇晃,却不像蜡烛那样滴落。为究其原因,小芳查阅资料得知:铝的熔、沸点分别是660℃、2460℃;氧化铝的熔、沸点分别为 2054℃、2980℃。请解释上述实验现象:。

-
(1) 实验a中,金属R表面有银白色固体物质析出,实验b中,锌表面有黑色固体物质析出。比较R、Zn、Ag的活动性强弱。
-
(2) 图c是实验a中反应的微观示意图。根据图c分析实验a中溶液增加的离子是,减少的离子是(填离子符号)。
-
(3) 写出实验a中发生的化学反应方程式(用含R的符号表示),该反应类型为。

-
(1) H2SO4是由元素组成。
-
(2) H2SO4的相对分子质量是,其中S、O元素的质量比为。
-
(3) 稀硫酸恰好完全反应时,生成氢气的质量为g。
-
(4) 求该铁粉样品中铁的质量分数(写出计算过程结果保留1位小数)

-
(1) 为了避免装置A中玻璃管在加热时发生爆炸,加热前应进行的操作是。装置A玻璃管中发生反应的化学方程式是。
-
(2) B处发生反应的化学方程式为。
-
(1) 【提出假设】三种金属的活动性顺序可能为①Zn>Ni>Cu;②Zn>Cu>Ni;③。
-
(2) 【查阅资料】小军同学查阅资料可知镍是略带黄色的固体,能与酸反应以及部分含镍化合物在水中的溶解性和颜色如下表:
OH-

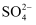
Cl-
Ni2+
不溶
可溶
可溶
可溶
颜色
蓝绿色
绿色
绿色
蓝绿色
【设计实验】在相同的温度下,取大小、厚度相同的这三种金属薄片,用砂纸打磨,其目的是;再分别投入到等体积等浓度的足量的稀盐酸中,观察实验现象。
-
(3) 【记录现象】请你帮助小军把实验现象填写完整。
金属
Ni
Zn
Cu
与稀盐酸反应的现象
产生气泡缓慢,金属逐渐溶解,溶液。
产生气泡较快,金属逐渐溶解
-
(4) 【得出结论】原假设中(填序号)成立,写出镍与稀盐酸反应的化学方程式(镍元素在化合物中显+2价)。
-
(5) 【拓展应用】上述实验选择稀盐酸完成了探究,得出了三种金属的活动性顺序。请你再选择另一类别的试剂设计实验,同样也能验证这三种金属的活动性顺序,你所选择的试剂是(限选三种试剂)。
- 下列民族与其民族节日的组合,正确的是( ) A.藏族——开斋节
- (随州中考)据图分析,下列说法正确的是()A.大象之间的“交谈”有时用超声波,声音很小,人类听不见但大象们能听清B.静谧
- (6分)已知碳有两种常见的同位素126C、136C;氧有三种常见的同位素168O、178O、188O。(1)由这五种微粒
- 改变,变化
- Electric Shock Injuries caused by electric shock are fairly
- He ______ his paper to see if there are any obvious mistakes
- 使反应4NH3(g)+3O2(g)===2N2(g)+6H2O在2 L的密闭容器中进行,半分钟后N2的物质的量增加了0.
- 一木块重4N,浮在水面上,有一半体积浸没在水中,那么木块全部浸没在水里受到的浮力是 A、8N B、6
- (2014•郴州)生物兴趣小组探究“细菌对植物遗体的分解作用”,提出了甲、乙两个探究方案如下: (每套培养皿中放等量来自
- (2011年湖南怀化,25题)汽车给人们的出行带来便捷,但也给“低碳生活”造成影响,其燃料汽油属于
- 已知圆C的半径为,圆心在轴的正半轴上,直线与圆C相切,则圆C的方程为 A. B. C.
- 在绕地球做匀速圆周运动的航天飞机外表面,有一隔热陶瓷片自动脱落,则( ) A.陶瓷片做平抛运动 C.
- 三氧化二铋(Bi2O3)俗称铋黄,是制作防火纸的材料之一.三氧化二铋属于()A. 氧化物 B. 酸 C. 碱 D. 盐
- 关于中国社会主义革命和建设的思想,是在新的历史条件下取得的重大理论成果,标志着思想发展到新的高度。集中体现其社会主义革命
- Living in _______ ever increasinglyfast-paced world, we are
- (08年长春外国语学校期末物理文)(4分)已知质量为m的物体从高处自由下落,经时间t,在t时间内重力对物体做功的平均功率
- 【原创】1.下列各句中,没有错别字且加点字的注音全都正确的一项是( ) A.G20大会摒(bìng)弃各国相互搏弈
- 对本文中第⑧⑨句议论的用意理解不正确的一项是[ ] A.赞扬我军英勇无畏、所向披靡的英雄气概 B.揭露国民党反动
- 阅读下面的文字,回答15―18题。我的精神家园王小波我十三岁时,常到我爸爸的书柜里偷书看。那时候政治气氛紧张,他把所有不
- 如图,,半径为1cm的切于点,若将在上向右滚动,则当滚动到与也相切时,圆心移动的水平距离是__________cm.



