第三节 化学反应中的有关计算 知识点题库
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,且没有二次污染。高铁酸钾与水反应的化学方程式是:4K2FeO4+l0H2O=4Fe(OH)3+8KOH+3X ↑。以下有关说法正确的是( )
A . X 的化学式是 O3
B . 铁元素化合价前后没有发生改变
C . 高铁酸钾可以长久敞口放置
D . 高铁酸钾与少量水反应后水体的酸碱度改变
用溶质质量分数为5%的NaOH溶液中和50g的稀硫酸,反应过程中溶液的酸碱度变化如图所示。请计算稀硫酸中溶质的质量分数。

我国古代典籍中有“银针验毒”的记载,其反应原理之一是4Ag+2H2S+O2═2X+2H2O.则X的化学式为()
A . S
B . SO2
C . Ag2S
D . SO3
氯碱工业是基本化学工业之一,工业上用电解饱和NaCl溶液的方法来制取重要化工原料。其反应的化学方程式是:2NaCl+2H2O  2X+H2↑+Cl2↑,则X的化学式为( )
2X+H2↑+Cl2↑,则X的化学式为( )
 2X+H2↑+Cl2↑,则X的化学式为( )
2X+H2↑+Cl2↑,则X的化学式为( )
A . NaH
B . NaClO
C . Na2O2
D . NaOH
以下是实验室制取气体的常用仪器,回答下列问题。

-
(1) 标号为a的仪器名称是;
-
(2) 用大理石和稀盐酸反应制取CO2 , 并用排水法收集。
①该反应的化学方程式为;
②若要制取两瓶CO2(总质量为4.4g),所用7.3%的盐酸至少g;
③组装制取装置时,需选择上图中的a、b、h、i、k、l、m和;
④实验室制取下列气体时,可选用制取二氧化碳装置的是(填序号)
A、锌粒和稀硫酸制取氢气
B、加热无水醋酸钠与碱石灰固体制取甲烷
C、硫化亚铁与稀硫酸常温反应制取易溶于水的硫化氢气体
-
(3) 实验室用KClO3制取O2:
①若用排水法收集O2 , 当观察到现象时,说明已收集满。
②反应过程中MnO2在固体混合物中质量分数变化情况,正确的是(填序号)
A、先逐渐变小,最后不变
B、先逐渐变大,最后不变
C、始终不变
某实验小组用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示。

-
(1) 在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质有。
-
(2) 计算Na2CO3溶液中溶质的质量分数。(计算结果精确到0.1%)(反应的方程式:Na2CO3+CaCl2=CaCO3↓+2NaCl)
某工厂化验室用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液80 g,洗涤后的溶液呈中性。这一定量石油产品中含H2SO4的质量是多少?
我县石灰石资源丰富,化学兴趣小组的同学为了测定该石灰石中碳酸钙的质量分数,用托盘天平称取了5份石灰石样品,分别加入各盛有200.0克稀盐酸的烧杯中充分反应(假设杂质不反应),得如下实验数据:
|
实验编号 |
1 |
2 |
3 |
4 |
5 |
|
石灰石样品的质量/g |
12.5 |
25.0 |
37.5 |
50.0 |
62.5 |
|
生成CO2的质量/g |
4.4 |
8.8 |
13.2 |
17.6 |
17.6 |
分析上述实验数据并回答:
-
(1) 实验编号为的实验数据表明反应物恰好完全反应。
-
(2) 计算反应物恰好完全反应后溶液中溶质的质量分数?
一定条件下,A B C D四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表,有关说法正确的是( )
| 物质 | A | B | C | D |
| 反应前物质质量/g | 6 | 10 | 25 | 40 |
| 反应后物质质量/g | 14 | 待测 | 42 | 15 |
A . 该反应为化合反应
B . B一定是该反应的催化剂
C . 待测值为0
D . 参加反应的A和C的质量比为8∶17
一定质量的碳酸钙高温煅烧一段时间后生成二氧化碳
22g,测得剩余固体中碳元素的质量分数为6%。计算:
-
(1) 根据化学方程式计算,参加反应的碳酸钙的质量。
-
(2) 剩余固体的质量。
下列图像能正确表示对应关系的是( )
A . 高温煅烧石灰石  B . 等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应
B . 等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应  C . 一定温度下,向一定量的饱和石灰水中加入生石灰
C . 一定温度下,向一定量的饱和石灰水中加入生石灰  D . 向硫酸铜和稀硫酸的混合溶液中,滴加氢氧化钠溶液
D . 向硫酸铜和稀硫酸的混合溶液中,滴加氢氧化钠溶液 
 B . 等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应
B . 等质量的碳酸钙与足量溶质质量分数相同的稀盐酸反应  C . 一定温度下,向一定量的饱和石灰水中加入生石灰
C . 一定温度下,向一定量的饱和石灰水中加入生石灰  D . 向硫酸铜和稀硫酸的混合溶液中,滴加氢氧化钠溶液
D . 向硫酸铜和稀硫酸的混合溶液中,滴加氢氧化钠溶液 
在一个密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如下图刻度纸所示(例如:d的质量为2g)。

在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度的移动来表示,且记录在同一张刻度纸上:刻度线I向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向左移动8格。下列说法错误的是( )
A . 反应结束后c的质量为6g
B . 该反应不属于分解反应
C . a、b变化的质量比一定为9:17
D . 参加反应的a、d的质量之比一定为9:8
某实验小组为测定铜和氧化铜的混合物中铜元素的含量,取20 g该固体混合物,向其中逐滴加入稀H2SO4,测得剩余固体的质量与加入稀H2SO4的质量关系如图所示。回答下列问题:

-
(1) 该固体混合物中铜元素的质量为;
-
(2) 计算稀H2SO4中溶质的质量分数(写出计算过程)。
向盛有 10g49%稀硫酸的烧杯中加入5.6g的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。分析错误的是( )
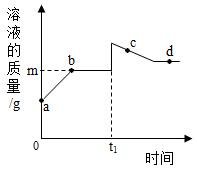
A . a→b 点,溶液的 pH 逐渐增大
B . c 点时,溶液中有两种溶质
C . d 点固体,加入盐酸有气泡产生
D . m=12.7g
硝酸铅[Pb(NO3)2]受热分解的化学方程式为:2Pb(NO3)2  2PbO+4X↑+O2↑,则X的化学式为( )
2PbO+4X↑+O2↑,则X的化学式为( )
 2PbO+4X↑+O2↑,则X的化学式为( )
2PbO+4X↑+O2↑,则X的化学式为( )
A . NO
B . N2
C . NO2
D . N2O5
质量守恒定律对科学发展具有重大意义。
-
(1) 用如图所示的2个实验装置进行验证质量守恒定律的实验,其中不能达到实验目的是(填序号),其原因是。

-
(2) A图是测定红磷燃烧前后质量的变化情况,用来验证质量守恒的实验,试回答:红磷燃烧的化学方程式是。
化学兴趣小组向一包NaCl和Na2CO3的固体混合物中,加入如图所示稀盐酸至恰好不再产生气泡,操作过程如图所示:

-
(1) 上述实验过程中发生反应的化学方程式为;
-
(2) 根据已知条件列出求解与稀盐酸反应的物质的质量(x)比例式;
-
(3) 用36.5%的浓盐酸配制上述稀盐酸,所需浓盐酸的质量为;
-
(4) 向溶液A中加入58.4g水后,所得不饱和溶液A的溶质质量分数为。
利用电子秤进行如图所示的称量活动。经过一段时间后,活动1和活动2的电子秤示数都减小了。

-
(1) 活动1的电子秤示数减小,从微粒的角度解释其原因是。
-
(2) 活动2中电子秤示数减小的部分(填“大于”“等于”或“小于”)蜡烛燃烧后生成物的总质量。
阅读下列资料,完成下列小题:尿素[CO(NH2)2]作为一种中性肥料,易溶于水,经过土壤中的脲酶作用,水解成碳酸铵或碳酸氢铵后,才能被农作物吸收利用。工业上常用氨气和二氧化碳为原料,通过反应 直接合成尿素。
直接合成尿素。
 直接合成尿素。
直接合成尿素。
-
(1) 下列关于尿素的说法,正确的是( )A . 由3种元素组成 B . 30g尿素中含氮元素的质量为14g C . 氢、氮元素的质量比为2:1 D . 尿素属于复合肥
-
(2) 对于反应
 , 下列有关说法正确的是( )
A . X的化学式为H2O2 B . 该反应属于置换反应 C . CO2的分子模型为
, 下列有关说法正确的是( )
A . X的化学式为H2O2 B . 该反应属于置换反应 C . CO2的分子模型为 D . 无机物可以转变为有机物
D . 无机物可以转变为有机物
实验室欲测定一瓶标签破损的稀盐酸的溶质质量分数。现取10g稀盐酸样品,滴入几滴无色的酚酞溶液。然后将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示。试回答:

-
(1) b点时溶液中的溶质为 ;
-
(2) c点时溶液的颜色为;
-
(3) 计算稀盐酸的溶质质量分数。(写出计算过程)
最近更新
- 下列气体发生装置,当加入适当的块状固体和液体时不具有随开随关功能的是( )
- —The workers are made allday. —What a hard life they
- 13、关于测定亚硝酸盐含量的操作,错误的是 ( ) A质量浓度为4 mg/mL的对氨基苯磺酸溶液呈酸性
- 奖器有个小球,其中个小球上标有数字,个小球上标有数字,现摇出个小球,规定所得奖金(元)为这个小球上记号之和,求此次摇奖获
- 超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导材料物质YBa2C
- 有两个互成角度的共点力,夹角为θ,它们的合力F随θ变化的关系如图3-5-4所示,那么这两个力的大小分别是( ) 图
- 下图表示某细胞在生长过程中细胞器的变化l曲线,该细胞可能为A.肾小管管壁细胞
- 如图所示的电路中,电源电压恒定,闭合开关S后,滑动变阻器的滑片P向左移动的过程中,下列说法正确的是()A.电流表A1示数
- 两会公布2019 年国家完善优抚安置制度体系落实退役军人待遇保障完善退役士兵基本养老、基本医疗保险接续政策 , 增加对转
- 突变是DNA结构的改变,这种改变可以通过复制传递到后代,且一般是不可逆的。
- (本小题满分12分,(I)小问5分,(II)小问7分) 在数列中,=1,,其中实数。 求的通项公式; 若对一切有,求c的
- 读图完成:(1)判断气压值Pl、P2、P3的大小关系是________;从气压状况上讲,此系统为________,从气流
- DNA的粗提取与鉴定实验中有三次过滤: ⑴过滤用蒸馏水稀释过的鸡血细胞液 ⑵过滤含粘稠物的0.14mol/LNaCl溶液
- 阅读下面的文言文,完成1~5题。 胡宿,字武平,常州晋陵人。宿为人清谨忠实,内刚外和。登第,为扬子尉。县大水,民被溺,令
- _________ the flight to New York will be delayed is ________
- 某学生做电磁感应现象的实验,其连线如图所示,当他接通、断开开关时,电流表的指针都没有偏转,其原因是 A.开关位置接错 B
- 先化简,再求值:,其中.
- 灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知 ①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g)
- 化学元素在岩石圈中存在的基本单元是 A.矿产 B.矿物 C.岩石 D.地壳
- 已知二氯苯的同分异构体有三种,从而可推知四氯苯的同分异构体的数目是( ) A.1 B.2



