高考二轮复习知识点:原电池工作原理及应用3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
一种镁氧电池如图所示,电极材料为金属镁和吸附氧气的活性炭,电解液为KOH浓溶液。下列说法错误的是( )
A . 电池总反应式为:2Mg + O2 +2H2O =Mg(OH)2
B . 正极反应式为:Mg -e- =Mg2 +
C . 活性炭可以加快O2在负极上的反应速率
D . 电子的移动方向由a经外电路到b
|
|
| 2. 单选题 | 详细信息 |
|
为提升电池循环效率和稳定性,科学家近期利用三维多孔海绵状Zn(3D−Zn)可以高效沉积ZnO的特点,设计了采用强碱性电解质的3D−Zn—NiOOH二次电池,结构如下图所示。电池反应为Zn(s)+2NiOOH(s)+H2O(l)
 ZnO(s)+2Ni(OH)2(s)。下列说法错误的是( ) ZnO(s)+2Ni(OH)2(s)。下列说法错误的是( )
A . 三维多孔海绵状Zn具有较高的表面积,所沉积的ZnO分散度高
B . 充电时阳极反应为Ni(OH)2(s)+OH−(aq)−e−=NiOOH(s)+H2O(l)
C . 放电时负极反应为Zn(s)+2OH−(aq)−2e−=ZnO(s)+H2O(l)
D . 放电过程中OH−通过隔膜从负极区移向正极区
|
|
| 3. 多选题 | 详细信息 |
|
一种可充放电的铝离子电池工作原理如图所示,电解质为
 离子液体, 离子液体,  在电池反应后转化为 在电池反应后转化为  和 和  。下列说法正确的是( ) 。下列说法正确的是( )
A . 若
 从电极表面脱落,则电池单位质量释放电量减少
B . 该电池放电时,正极反应为 从电极表面脱落,则电池单位质量释放电量减少
B . 该电池放电时,正极反应为  C . 为提高电池效率,可以向
C . 为提高电池效率,可以向  电极附近加入适量 电极附近加入适量  水溶液
D . 充电时电池负极的反应为 水溶液
D . 充电时电池负极的反应为 
|
|
| 4. 多选题 | 详细信息 |
|
2019年诺贝尔化学奖颁给了为锂离子电池发展作出突出贡献的三位科学家,他们创造了一个可充电的世界。Garmet型固态电解质被认为是锂电池最佳性能固态电解质。某Garmet型可充电锂电池放电时工作原理如图所示,下列说法正确的是( )
(电池总反应为: LixC6+LisxLaZrTaO
A . 放电时,b极为负极
B . 充电时,固态电解质中Li+移向a极
C . 放电时,a极反应LiLaZrTaO-xe-=xLi++LinxLaZrTaO
D . 充电时,若转移0.01mol电子,b极质量减少0.07 g
|
|
| 5. 综合题 | 详细信息 |
|
央广网消息:2020年大庆油田生产天然气46.6亿立方米,实现了“十连增”,在大战大考中交出了“当好标杆旗帜、建设百年油田”的新答卷。天然气的主要成分甲烷是一种重要的化工原料,广泛应用于民用和化工业生产中。回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
Li-CuO二次电池的比能量高、工作温度宽,性能优异,广泛应用于军事和空间领域。
|
|
| 7. 综合题 | 详细信息 |
|
LiFePO4是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3 , 还含有少量MgO、SiO2等杂质)来制备,工艺流程如图:
|
|
| 8. 综合题 | 详细信息 |
|
硫酸铅广泛应用于制造铅蓄电池、白色颜料以及精细化工产品3PbO·PbSO4·H2O(三盐)等。工业生产中利用方铅矿(主要成分为PbS,含有FeS2等杂质)制备PbSO4的工艺流程如下:
已知:①PbCl2难溶于冷水,易溶于热水。 ②PbCl2(s)+2Cl-(aq) ③Ksp(PbSO4)=1.08×10-8 , Ksp(PbCl2)=1.6×10-5
|
|
| 9. 综合题 | 详细信息 | ||||||||||
|
我国天然气储量丰富,天然气是重要的化工原料,先与氧气转化为合成气再进一步可催化转化为甲醇和二甲醚。回答下列问题:
|
|||||||||||
| 10. 综合题 | 详细信息 |
|
|
- 甘肃省天水市秦州区2020-2021学年高一下学期化学期中考试试卷
- 辽宁省六校2021-2022学年高三上学期化学开学考试试卷
- 冲刺2021高考化学押题训练(十一)非金属及其化合物
- 河南省南阳市六校2021-2022学年高一下学期4月份期中联考化学试题
- 山东省泰安肥城市2020-2021学年高二上学期化学期中考试试卷
- 江苏省苏州八校联盟2021-2022学年高三上学期化学第一次月考试卷
- 浙江省宁波市六校2021-2022学年高二下学期期中联考化学试题
- 2021年高考理综化学真题试卷(全国甲卷)
- 冲刺2021高考化学押题训练(十二)常见有机物
- 黑龙江省大兴安岭呼玛县高级中学2020-2021学年高二上学期化学第三次月考试卷
- 山东省日照市五莲县2020-2021学年高二上学期化学期中考试试卷
- 北京市海淀区2021-2022学年高三上学期期中考试化学试题
- 下图表示在呼吸过程中肺容量的变化曲线。当肺容量由a变化到b,肋间外肌和膈肌的舒缩状况分别是( )A.收缩、舒张
- 下面是四种粒子的结构示意图,用序号填空: (1)电子层排布相同的是 ;(2)属于同种元素的
- —How do you like this dress? —It’s beautiful, and it fits me
- 填补下列名句的空缺处或按要求填空。 (每空1分) (1)几处早莺争暖树,___________________
- (10分)请按要求填空:(1)请写出相应的化学符号或名称:①2个铁原子 ▲ ;②+2价的钙元素 ▲ ;③CO3
- 位于广州市老城区中已有多年历史的广州水泥厂已经停产,等待搬迁。以下有关说法正确的是 A.广州水泥厂对环境的影响主要是污染
- He is famous both ______ a novelist and a poet but he is mor
- Do you want ______ with me? A.go to school
- 下列各句中,加点的熟语使用不恰当的一项是( )A、作者自以为写得出神入化,但从现在看起来,是连新奇气息也没有的。B、他们
- When you'relearning to drive,________agood teacher makes a b
- 二项式(1+sinx)6的展开式中二项式系数最大的一项的值为 ,则x在[0,2π]内的值为________.
- 动物激素调节的特点是() A.激素是细胞的组成物质,种类多、含量极微 B.激素分子弥散在体液中,对全身细胞都起作用 C
- 质量为48kg的人,如果他每只鞋底的面积为160cm2,他站立时对地面的压力是_______N,他走路时对地面的压强是_
- —Are you sure you can do well in the final exam?—___________
- 月出于东山之上, 。 ,水光接天。(苏轼《赤壁赋》)
- 纪录片《舌尖上的中国》介绍了我国不同地域、不同民族、不同风貌的有代表性的饮食文化。该片在电视台播放后引起了极大关注,产生
- 26.(7分)有一小块不溶于水的复合地板材料(比量筒口稍大),已知它的密度比水小,哓梅同学想探究它受浮力的大小,以及想知
- 据报道,东北A乡镇一农民把自己生产的余粮卖给了B乡镇,因为该农民没有把余粮卖给A乡镇粮食部门,结果被A乡镇粮食部门以“倒
- 阅读下面的文言文,完成小题。 虞翻字仲翔,会稽余姚人也,太守王翔命为功雷,孙策征会稽,朗拒战败绩,亡走浮海。翻追随营
- 蛋白质发生的下列过程中,可逆的是( ) A、盐析 B、变性 C、煮熟 D、加入浓硫酸



 LiLaZrTaO+6C)
LiLaZrTaO+6C)
 2CO(g)+2H2(g),CH4和CO2的分压均为20 kPa,加入催化剂Ni/α-Al2O3 , 分别在T1℃和T2℃下进行反应,测得CH4转化率随时间变化如图1所示。
2CO(g)+2H2(g),CH4和CO2的分压均为20 kPa,加入催化剂Ni/α-Al2O3 , 分别在T1℃和T2℃下进行反应,测得CH4转化率随时间变化如图1所示。 
 ,T2℃下,上述反应0~2min内平均反应速率v(CH4)=kPa·min-1。(分压=总压×物质的量分数)
,T2℃下,上述反应0~2min内平均反应速率v(CH4)=kPa·min-1。(分压=总压×物质的量分数)

 CuSO4溶液
CuSO4溶液  Cu2(OH)2CO3沉淀
Cu2(OH)2CO3沉淀  CuO
CuO


 形式存在,写出水解形成TiO2·xH2O相应反应的离子方程式。
形式存在,写出水解形成TiO2·xH2O相应反应的离子方程式。
 ,则电极材料中n(Fe2+):n(Fe3+)=。
,则电极材料中n(Fe2+):n(Fe3+)=。

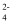 (aq) △H>0
(aq) △H>0

 CH3OCH3(g)+H2O(g),T2℃时,向5L恒容密闭容器中充入1molCO(g)和2molH2(g),发生该反应,达到平衡时,测得容器内总压强为p,CO的体积分数为25%,则T2℃时,反应的平衡常数Kp=(用含p的代数式表示Kp , 分压=总压×物质的量分数)。
CH3OCH3(g)+H2O(g),T2℃时,向5L恒容密闭容器中充入1molCO(g)和2molH2(g),发生该反应,达到平衡时,测得容器内总压强为p,CO的体积分数为25%,则T2℃时,反应的平衡常数Kp=(用含p的代数式表示Kp , 分压=总压×物质的量分数)。






