从巩固到提高 高考化学二轮微专题08 卤族元素
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
I2的一种制备方法如图所示:
下列说法正确的是:( )
A . “富集”时发生的离子方程式为
 B . 转化反应为
B . 转化反应为 , 说明 , 说明 的还原性大于 的还原性大于 C . 通入过量Cl2 , 氧化产物只有一种
D . 制备的I2可直接用于加碘盐
C . 通入过量Cl2 , 氧化产物只有一种
D . 制备的I2可直接用于加碘盐
|
|
| 2. 实验探究题 | 详细信息 |
|
KMnO4是一种常用的氧化剂。某实验小组利用氯气氧化K2MnO4制备KMnO4并对其性质进行探究。
资料:①锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:3 ②酸性条件下的氧化性:KMnO4>KIO3>I2
|
|
| 3. 单选题 | 详细信息 |
|
海水综合利用符合可持续发展的原则,其联合工业体系(部分)如图所示,下列说法中错误的是( )
A . ①中可采用蒸馏法或者电渗析法
B . ②中可通过电解熔融态的氯化镁制金属镁单质
C . ③中生成1mol Br2 , 共消耗标准状况下Cl2 22.4L
D . ④的产品可生产盐酸、漂白液、漂白粉等
|
|
| 4. 单选题 | 详细信息 |
|
新制氯水中没有的微粒是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 5. 综合题 | 详细信息 |
|
卤族元素在自然界中主要以卤化物形式存在,完成下列填空:
|
|
| 6. 实验探究题 | 详细信息 | ||||||||||||
|
四氯化锡(SnCl4)可用作媒染剂和有机合成的氯化催化剂。实验室可按下图装置(部分夹持装置略去)制备SnCl4。
已知:①SnCl2和SnCl4的部分物理性质:
②Sn能与HCl反应生成SnCl2 , 无水SnCl4遇水易水解生成SnO2·xH2O ③Sn与Cl2加热条件下生成SnCl4和SnCl2 回答下列问题:
|
|||||||||||||
| 7. 单选题 | 详细信息 |
|
下列关于Cl2性质的说法正确的是( )
A . 可与NaOH溶液反应
B . 是无色无味的气体
C . 能使干燥的有色布条褪色
D . 密度比空气小
|
|
| 8. 实验探究题 | 详细信息 |
|
某小组同学利用一定浓度的HCl溶液和MnO2制备Cl2 , 并进行有关实验。
|
|
| 9. 单选题 | 详细信息 |
|
三氟化氯(ClF3)可应用于航天工业,是一种很强的氧化剂和氟化剂,它能与大多数有机和无机材料甚至塑料反应,可以使许多材料不接触火源就燃烧。下列分析错误的是( )
A . 可以代替H2O2充当火箭推进剂中的氧化剂
B . 能与一些金属反应生成氯化物和氟化物
C . 三氟化氯可用于清洁化学气相沉积的反应舱附着的半导体物质
D . ClF3与水按照1:2反应生成两种强酸
|
|
| 10. 单选题 | 详细信息 |
|
NaClO是家用消毒液的有效成分,可通过Cl2与NaOH反应制得。NaClO能与CO2反应生成HClO。常温下ClO2为黄绿色有毒气体,易溶于水。ClO2体积分数大于10%或其水溶液在温度过高时可能发生爆炸,与碱反应生成ClO
 和ClO 和ClO 等。实验室制备ClO2的反应原理为2KClO3+H2C2O4+H2SO4=2ClO2↑+2CO2↑+K2SO4+2H2O。下列说法正确的是( ) 等。实验室制备ClO2的反应原理为2KClO3+H2C2O4+H2SO4=2ClO2↑+2CO2↑+K2SO4+2H2O。下列说法正确的是( )
A . 新制氯水需存放在带玻璃塞的棕色试剂瓶中
B . 可用广泛pH试纸测定新制氯水的pH值
C . NaClO与CO2反应的离子方程式为NaClO+CO2+H2O=HClO+Na++HCO
 D . 使用NaClO消毒时,可用盐酸酸化
D . 使用NaClO消毒时,可用盐酸酸化
|
|
- 高中化学人教版(2019)必修第一册第一章第三节 氧化还原反应
- 2016-2017学年山东省淄博市淄川一中高二下学期期中化学试卷
- 云南省昭通市水富县云天化中学2016-2017学年高二上学期化学期末考试试卷(理科)
- 四川省蓬安县第二中学2019-2020学年高一下学期化学开学考试卷
- 山西省太原市2017-2018学年高考理综-化学三模考试试卷
- 2016-2017学年广东省肇庆市高一上学期期末化学试卷
- 人教版化学高二选修3第三章第一节晶体的常识同步练习
- 人教版高中化学选修五 第二章第一节:脂肪烃
- 吉林省松原市扶余市第一中学2019-2020学年高一下学期化学期中考试试卷
- 吉林省辽源市普通高中2016-2017学年高一上学期化学期中考试试卷
- 河南省郑州市2017-2018学年高三化学一模考试试卷
- 黑龙江省齐齐哈尔市拜泉四中2019-2020学年高三上学期化学第四次月考试卷
- 下列各项中的“黄色”不属于因发生化学反应而产生的是 (
- “环境”对做学问并不会有很大的影响,古今有不少学者都是在喧闹的环境中写出伟大著作的,陶潜说:“_____________
- 21.图中①~④表示某细胞的部分细胞器。下列有关叙述正确的是( )A.该图一定是高倍光学显微镜下看到的结构 B.此细
- 某同学平常走路步行40 m,需40 s的时间,现在这个同学用6 min 30 s的时间沿操场跑道走完一圈,那么跑道的周长
- “蚁穴溃堤”这一成语主要提示了生物对环境造成的影响。( )
- 2008年11月15日,20国集团领导人金融市场和世界经济峰会在美国首都华盛顿举行。会议发表的宣言指出,在世界经济和国际
- 今年4月以来,冰岛南部埃亚菲亚德拉冰川附近火山多次大规模喷发,火山熔岩不仅融化了部分冰川,导致山洪暴发、道路桥梁被毁,腾
- 当水壶中的水烧开时,壶盖会被顶起,从能量转化的观点看,这是水蒸气的_________能转化为壶盖的 能
- 关于重力的大小,以下说法中正确的是 A.重力是物体本身具有的力,大小与物体的质量成正比B.静止在水平面上的物体对水平面的
- 记者要为名志愿者和他们帮助的位老人拍照,要求排成一排, 位老人相邻但不排在两端,不同的排法共有( ) A.1440种
- 据英国《自然》杂志报道,科学家最近研制成了以锶原子做钟摆的“光晶格钟”,成了世界上最精确的钟。已知一种锶原子相对原子质量
- 元素X、Y、Z原子序数之和为36,X、Y在同一周期,X+与Z2-具有相同的核外电子层结构。下列推测不正确的是A.同周期元
- 今年我国西南地区地区特大干旱历史罕见。为缓解旱情,政府组织实施了多次人工降雨。利用碘化银进行人工降雨就是利用高炮或飞机,
- 阅读下面的内容,完成下面3题 躬身实践低头做事最为重要 人的一生离不开做事。只有通过做事,才能锻造出一个人的能力之剑。
- 在安装直流电动机模型的实验中,为了改变电动机的转动方向,可采取的措施是 A.改变磁场的强弱 B.改变电流的大小C.只改变
- The film star walked to his car, ______ a crowd of journalis
- 下图是山地不同部位的等高线示意图,四图中属于山谷的是 ( ) A、B、C、D、
- Jack was once a common name, ,I think, that is seldom c
- 金属
- This________was conducted to findout how many people prefer

 +2H2O=2
+2H2O=2  +MnO2↓+4OH-
+MnO2↓+4OH-

 ,写出生成
,写出生成 

 的晶体类型;
的晶体类型; 的简单离子半径大小;
的简单离子半径大小; 最外层电子的电子云形状为。
最外层电子的电子云形状为。 主要用于氯碱工业,写出阳极的电极反应。
主要用于氯碱工业,写出阳极的电极反应。
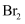 ,并用纯碱吸收。纯碱吸收
,并用纯碱吸收。纯碱吸收  ,吸收
,吸收  时,转移电子为mol。
时,转移电子为mol。
 和
和  ,即有
,即有  晶体析出。结合速率与平衡理论解释
晶体析出。结合速率与平衡理论解释  ,发生反应:
,发生反应:  ,配平上述方程式。
,配平上述方程式。







