高考二轮复习知识点:电解池工作原理及应用1
高考二轮复习知识点:电解池工作原理及应用1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
 为阿伏加德罗常数的值。下列说法正确的是( ) 为阿伏加德罗常数的值。下列说法正确的是( )
A .
 , ,  完全反应转移的电子数为 完全反应转移的电子数为  B . 用电解粗铜的方法精炼铜,当电路中通过的电子数为
B . 用电解粗铜的方法精炼铜,当电路中通过的电子数为  时,阳极应有 时,阳极应有  转化为 转化为  C . 常温下,
C . 常温下,  的 的  溶液中,水电离出的 溶液中,水电离出的 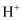 数为 数为  D .
D .  浓度为 浓度为  的 的  溶液中,阴离子数为 溶液中,阴离子数为 
|
|
| 2. 综合题 | 详细信息 | |||||||||||||||||||||||||||
|
镍钛钯废靶材含钛55%、镍25%、钯18%和杂质铝2%。从镍钛钯废靶材回收有关金属的工艺流程如下:
已知:I.常温下,钛与钯均不溶于盐酸。 II.PdCl 回答下列问题:
|
||||||||||||||||||||||||||||
| 3. 综合题 | 详细信息 |
|
铜是重要的金属,广泛应用于电气、机械制造、国防等领域,铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
|
|
| 4. 综合题 | 详细信息 |
|
除去废水中Cr(Ⅵ)的方法有多种。请按要求回答下列问题。
|
|
| 5. 多选题 | 详细信息 |
|
现有一种安全、高效的双极制氢系统,该系统能够从阳极低电压醛氧化和阴极析氢反应中得到氢气;其工作原理如图所示。下列说法正确的是( )
A . 电压越高,阳极制氢速率越快
B . 电解一段时间后,阴极室的pH不变
C . 制得1mol氢气,理论上有1molOH-透过交换膜
D . 阳极反应为2R-CHO+4OH--2e-=2R-COO-+H2↑+2H2O
|
|
| 6. 多选题 | 详细信息 |
按下图装置进行电解(氯化钠足量),若乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量,下列叙述错误的是( )
A . E表示生成金属钠的物质的量
B . E表示消耗水的物质的量
C . F表示溶解铜的物质的量
D . F表示生成氯气的物质的量
|
|
| 7. 多选题 | 详细信息 |
某工业碱性废水中含 |
|
| 8. 多选题 | 详细信息 |
应对新冠肺炎疫情时所采取的措施是对环境进行彻底消毒,二氧化氯( |
|
| 9. 综合题 | 详细信息 |
丙烯是重要的有机化工原料之一,丙烷直接脱氢制丙烯 |
|
| 10. 综合题 | 详细信息 |
金属锌具有储量丰富、电池理论容量高、氧化还原电位低、对环境友好等诸多优势;锌的化合物在防腐、电镀、医学、纺织等领域有诸多应用。
|
|
高中化学 试卷推荐
- 广东省揭阳市2017-2018学年高二下学期化学期末考试试卷
- 江苏省扬州市2018-2019学年高二下学期化学期末考试试卷
- 江苏省无锡市普通高中2017-2018学年高二上学期化学期末考试试卷
- 专题27:苯、芳香烃
- 2016-2017学年湖北省四地七校高二下学期期中化学试卷
- 山东省德州市2017-2018学年高一下学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题24 水的电离和溶液的酸碱性
- 2019年高考化学真题分类汇编专题04:元素周期表及周期律
- 2015-2016学年浙江省温州市平阳二中高一上学期期中化学试卷
- 2020高考化学常考知识点专练 10:流程题
- 宁夏吴忠市吴忠中学2018-2019学年高一上学期化学期末模拟试卷
- 云南省玉溪一中2018-2019学年高一上学期化学期末考试试卷
最近更新
- 0.4的相反数是 ,倒数是 ,绝对值是 。
- Eleven leatherback turtles(凌皮龟) are swimming across the Paci
- (1)一阻值约为30kΩ的电阻R,欲用伏安法较准确地测出它的阻值,备选器材有:A、电源(E=16V,r=2Ω)
- 27.下图为特异性免疫发生的过程图解,有关叙述不正确的是 A.通过基因疗法改造血友病女患者的①,其儿子仍患血友病
- 下列句子中,加点成语使用不恰当的一句是 A.没有人仅因富甲一方而被长久纪念,相反,人们念念不忘的,大都是超脱于物质利益的
- 右图是我国东部某山地地形剖面图及自然带垂直分布图,读图完成下面试题。该山地位于 A.华南热带湿润地区
- 若用半径为9,圆心角为的扇形围成一个圆锥的侧面(接缝忽略不计),则这个圆锥的底面半径是 。
- 棱长为a的正方体内有一个球,与这个正方体的12条棱都相切,则这个球的体积应为 ( )A. 43 B
- 现有X、Y、Z三种金属,只有Y能与盐酸反应,X与ZNO3溶液不反应,三者活动性强弱顺序是() A.X>Y>Z B.Y>
- 当太阳直射点如下图A所示时,下列关于北京说法正确的是 ( ) A.昼短
- 长城是众多访华外国政要“青睐”的标志性景点。尼克松、里根、克林顿、布什、奥巴马、撒切尔、伊丽莎白等外国政要访华时都游览过
- 化学与人类生活密切相关。下列说法正确的是( ) A.苯酚有一定毒性,不能作消毒剂和防腐剂 B.凡含有食品添加剂的食
- Throughout the world, boys and girls prefer to play with dif
- 下列国际组织与其英文缩写的搭配,不正确的是()。 A.欧洲联盟——APEC B.世界贸易组织——
- 如图所示,在超市内倾角为θ的电梯斜面上有一车西瓜随电梯匀速向上运动,在箱子的中央有一只质量为m的西瓜,则在该西瓜随箱一起
- 研究证明,在活的生物体中C的放射性同位素14C的含量保持不变,当此生物体死去后,14C会在其体内不断衰变而减少。因此,考
- 有人说中国是资源大国,又有人说中国是个资源小国。下列说法正确的是() A.自然资源总量和人均占有量都很丰富 B.自然资源
- (每空2分,共8分)鲫鱼能在光线很弱的水中游泳,但不会和水中的石块或其他物体碰撞。其原因是什么?请你设计一个探究实验来验
- 】下列句子没有语病的一句是( )A、增加质量是语文教学改革的当务之急。B、我们没有理由不珍惜今天的幸福生活。C、能否
- 已知氧化性Br2>Fe3+。FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为: a Fe2++b Br-+cC

 在溶液中存在配位平衡:PdCl
在溶液中存在配位平衡:PdCl PdCl4(aq)+2Cl-(aq) △H>0
PdCl4(aq)+2Cl-(aq) △H>0
 晶体中S原子的杂化方式为,
晶体中S原子的杂化方式为,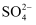 的立体构型为。
的立体构型为。
 , 其配体的电子式为;下列有关说法正确的是。
, 其配体的电子式为;下列有关说法正确的是。 分子和
分子和 分子之间形成氢键
分子之间形成氢键
 , 阿伏加德罗常数值为NA , 则该晶胞的棱长为cm。
, 阿伏加德罗常数值为NA , 则该晶胞的棱长为cm。
 与熟石灰除Cr(Ⅵ)法:向酸性废水中加入
与熟石灰除Cr(Ⅵ)法:向酸性废水中加入 沉淀(常温下
沉淀(常温下 ;设
;设 时沉淀完全)。
时沉淀完全)。

 、
、 离子能发生交换均生成
离子能发生交换均生成 (s)。其反应可表示为(以
(s)。其反应可表示为(以 。
。

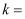 。
。 。已知:
。已知: 。
。


 , 利用下列装置可将其转化为FeS。下列说法正确的是
, 利用下列装置可将其转化为FeS。下列说法正确的是


 , 黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备
, 黄绿色易溶于水的气体)是一种安全稳定、高效低毒的消毒剂。工业上通过惰性电极电解氯化铵和盐酸的方法制备


 是一条绿色生产丙烯的途径。
是一条绿色生产丙烯的途径。

 恒压下,主反应的
恒压下,主反应的 随温度变化如图1所示,
随温度变化如图1所示, 0(填”、“<”或=”),判断的理由是。
0(填”、“<”或=”),判断的理由是。
 在不同温度下的平衡体积分数如图2所示,图中表示
在不同温度下的平衡体积分数如图2所示,图中表示 的体积分数的曲线为(填“a”或“b”),
的体积分数的曲线为(填“a”或“b”), 时,
时, 的体积分数为。
的体积分数为。
 工艺说法正确的是
工艺说法正确的是
 不变
不变
 , 相比
, 相比
 。
。 离子选择双隔膜电池如图所示。放电结束后对左侧电极片进行紫外测试,可观测到在765nm处有一个较强的吸收峰,在615nm处有一个肩峰,与标准
离子选择双隔膜电池如图所示。放电结束后对左侧电极片进行紫外测试,可观测到在765nm处有一个较强的吸收峰,在615nm处有一个肩峰,与标准 图像吻合。(注:
图像吻合。(注: 最终转化为
最终转化为 )。
)。
 电极质量减少g。
电极质量减少g。 的浓溶液可形成配合酸
的浓溶液可形成配合酸 , 因此
, 因此 的
的 的酸。根据以上信息,请写出
的酸。根据以上信息,请写出 的化学方程式。
的化学方程式。
 难溶于水,在强碱溶液中发生反应
难溶于水,在强碱溶液中发生反应 , 下图是二价锌在水溶液中的存在形式与pH的关系,其中c为
, 下图是二价锌在水溶液中的存在形式与pH的关系,其中c为
 。
。 的溶液中加入等体积
的溶液中加入等体积 的HCl后,体系中的Zn元素主要以(写微粒符号)形式存在。
的HCl后,体系中的Zn元素主要以(写微粒符号)形式存在。


