新疆阿勒泰地区2023届高考素养调研第一次模拟考试理科综合化学试题
新疆阿勒泰地区2023届高考素养调研第一次模拟考试理科综合化学试题
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 常温下22.4L NH3含有的中子数为7NA
B . 常温下1L pH=13的Ba(OH)2溶液中OH-的数目为0.2NA
C . 将50mL 12mol/L盐酸与足量
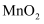 共热,转移的电子数为0.3NA
D . 56g C3H6和C4H8的混合气体中含有的氢原子数为8NA 共热,转移的电子数为0.3NA
D . 56g C3H6和C4H8的混合气体中含有的氢原子数为8NA
|
|
| 2. 单选题 | 详细信息 |
化学与生产、生活、环境等密切相关。下列说法正确的是
A . 向天然水中加入明矾可起到杀菌消毒的作用
B . 淀粉、纤维素在人体内最终的水解产物均为CO2和H2O
C . 用风能发电可减少温室气体排放
D . C919国产大飞机风挡结构部分使用的有机玻璃属于硅酸盐材料
|
|
| 3. 单选题 | 详细信息 |
利用下列装置(夹持部分略)和试剂进行实验,能达到实验目的的是
A .
 制备SO2
B . 制备SO2
B .  制备并收集少量NO
C . 制备并收集少量NO
C .  配制NaCl溶液
D . 配制NaCl溶液
D .  观察铁的析氢腐蚀 观察铁的析氢腐蚀
|
|
| 4. 单选题 | 详细信息 |
有机物M是合成抗过敏药物色甘酸钠的中间体,结构简式如图。下列关于该有机物的说法正确的是
A . 分子中只含有醚键、酯基两种官能团
B . 能与NaOH溶液反应
C . 苯环上的一氯取代物有4种
D . 所有碳原子不可能共平面
|
|
| 5. 单选题 | 详细信息 |
W、X、Y、Z为原子序数依次增大的短周期主族元素,W、Z同主族,Y单质可用作光电池,X的周期序数等于主族序数,Z原子的最外层电子数等于最内层电子数的3倍,下列叙述错误的是
A . 工业上采用熔融电解法冶炼X的单质
B . 含X或Y的某些盐可用于制备胶体
C . 简单离子的半径:Z>W>X
D . YW2和ZW2都是酸性氧化物,都不与酸反应
|
|
| 6. 单选题 | 详细信息 |
我国科学家近期开发了一种高性能的水系锰基锌电池。 其工作原理如图所示,已知该装置工作一段时间后,K2SO4溶液的浓度增大。下列说法正确的是
A . 电子流向:Zn电极→b膜→a膜→MnO2电极→负载→Zn电极
B . 负极的电极反应式为MnO2+2e-+4H+=Mn2++2H2O
C . a膜为阴离子交换膜,b膜为阳离子交换膜
D . 装置工作一段时间后,正极区溶液的pH降低
|
|
| 7. 单选题 | 详细信息 |
相同温度和压强下,研究Cl2分别在不同浓度的盐酸和NaCl溶液中的溶解度(用溶解Cl2的物质的量浓度表示)变化如图所示。
已知氯气溶解存在以下过程: ①Cl2(aq) + H2O(1) ②Cl2(aq) + Cl-(aq) ③HClO(aq) 下列说法错误的是
A . 随着NaCl浓度的增大,Cl2溶解度减小,溶液中
 减小
B . 随着盐酸浓度的增大,反应①被抑制,反应②为主要反应从而促进Cl2溶解
C . a点时,c(H+) >c(Cl-)>c( 减小
B . 随着盐酸浓度的增大,反应①被抑制,反应②为主要反应从而促进Cl2溶解
C . a点时,c(H+) >c(Cl-)>c( ) > c(ClO-)
D . b点时,c(Na+) + c(H+) = c(Cl-) + c( ) > c(ClO-)
D . b点时,c(Na+) + c(H+) = c(Cl-) + c( ) + c(OH-) + c(ClO-) ) + c(OH-) + c(ClO-)
|
|
| 8. 综合题 | 详细信息 | ||||||||||||||||||
为保护环境,充分利用钴资源,一种以废旧钴酸锂电池材料(正极材料主要含有LiCoO2、铝箔及金属钢壳)回收钴酸锂的工艺流程如下:
已知一定条件下,部分金属阳离子形成氢氧化物的pH如下表:
请回答下列问题:
|
|||||||||||||||||||
| 9. 实验探究题 | 详细信息 |
2022年11月,神舟十五号载人飞船发射任务取得圆满成功。肼(N2H4)可作火箭发射的燃料,具有强还原性,实验室用NH3与Cl2合成N2H4的装置如图所示,请回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
为实现“碳达峰”及“碳中和”,二氧化碳甲烷化技术是CO2循环再利用最有效的技术之一。请回答下列问题:
|
|
高中化学 试卷推荐
- 河南省郑州市2020-2021学年高二下学期化学期末考试试卷
- 山西省临汾市2020-2021学年高一下学期化学期末考试试卷
- 吉林省长春市农安县2020-2021学年高一上学期化学期中考试试卷
- 山东省临沂市2021年高考化学二模试卷
- 山东省济南市2021-2022学年高三下学期第二次模拟化学试题
- 浙江省十校联盟2020-2021学年高三上学期化学10月月考试卷
- 广东省中山市2020-2021学年高一上学期化学期末考试试卷
- 浙江省嘉兴市2021-2022学年高一上学期期末检测化学试题
- 山东省聊城市2022届高三二模化学试题
- 人教版化学高二选修5第二章第三节卤代烃同步练习
- 2019年高考化学模拟卷(卷I)
- 2015-2016学年天津市五区县高一下学期期末化学试卷
最近更新
- 爱因斯坦说:“人只有献身于社会,才能找出那实际上是短暂而有风险的生命的意义”。这主要在强调 A.人生价值是个人价值与社会
- 如图是某电场区域的电场线分布,A、B、C是电场中的三个点,下列说法正确的是( )A. A点的电场强度最大 B. B点的电
- ---Listen, what is the noise? ---Oh, the young man ne
- 右图是a、b两种物质的溶解度曲线.室温时,将盛有a、b饱和溶液的试管分别放入烧杯内的水中,均无晶体析出.当向烧杯内的水中
- 如图所示,电动势为E、内阻为r的电池与定值电阻R0、滑动变阻器R串联,已知R0=r,滑动变阻器的最大阻值是2r。当滑动变
- 近代中国第一个留美学生容闳认为,干王的见闻较之其他诸王和领导人广阔些,甚至超过了洪秀全。容闳作出这一判断的主要依据是
- 下列关于生物大分子的叙述错误的是 ( ) A.细胞中氨基酸种类和数量相同的蛋白质不一定是同一
- 先化简,再求值:x2y﹣(xy﹣x2y)﹣2(﹣xy+x2y)﹣5,其中x=﹣1,y=2.
- 木炭还原氧化铜和一氧化碳还原氧化铜的实验装置如下图所示。下列说法正确的是 A.术炭、一氧化碳与氧化铜的反应都属于置换反应
- 群落演替的总趋势是() A.物种多样性的增加和群落稳定性的提高 B.物种多样性的减少和群落稳定性的降低 C.物种多样性的
- 下列各项属于文化遗产的是( ) ①中国的长城 ②九寨沟自然风景区 ③埃及的金字塔 ④司马迁的《史记》 A.①
- 关于天然放射现象,以下叙述正确的是( ) A.若使某放射性物质的温度升高,其半衰期将减小 B.β衰变所释放的电子是原
- 《科学》杂志评出“饿死肿瘤”研究新进展为2004年十大科技突破之一。临床试验结果显示,一种抑制肿瘤血管生长的药物与传统化
- —Mike,is this Tom’s pencil?—Oh,yes,it is !A.mineB.he
- 为了延长种子的寿命、应将种子保存在什么环境() A.高温潮湿 B.高温干燥 C.低温潮湿 D.低温干燥
- Passport Control(护照验证处)If you are arriving at London Heathro
- 在室温下,向一定量的稀氨水中逐滴加入物质的量浓度相同的稀盐酸,直至盐酸过量。请回答下列问题。 (1)在实验过程中水的电离
- Mrs. Brown lives in a small town in Australia. There is a bi
- 阅读下面的文字,完成小题。 人是能够思考的动物,因此现代人类的动物分类学名称是“智人”。然而思考的能力须经过训练始得发展
- 潮菜在世界饮食文化中占有一席之地,常被视为精品,但在异国他乡落的潮菜酒楼,很多菜色要按照当地的饮食爱好进行巧妙的调味。这



 H+(aq) + Cl-(aq) + HClO(aq) K1= 4.2×10-4
H+(aq) + Cl-(aq) + HClO(aq) K1= 4.2×10-4


 CH4(g) + 2H2O(g)
CH4(g) + 2H2O(g)
 )
)





