高考二轮复习知识点:化学平衡的影响因素2
高考二轮复习知识点:化学平衡的影响因素2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是
A . 根据曲线数据计算可知Ksp(AgCl)的数量级为10-10
B . 曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl)
C . 相同实验条件下,若改为0.0400 mol·L-1 Cl- , 反应终点c移到a
D . 相同实验条件下,若改为0.0500 mol·L-1 Br- , 反应终点c向b方向移动
|
|
| 2. 单选题 | 详细信息 |
|
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
下列说法错误的是:( )
A . 生成CH3COOH总反应的原子利用率为100%
B . CH4→CH3COOH过程中,有C-H键发生断裂
C . ①→②放出能量并形成了C一C键
D . 该催化剂可有效提高反应物的平衡转化率
|
|
| 3. 单选题 | 详细信息 |
|
实验测得
 溶液、 溶液、  溶液以及 溶液以及  的pH随温度变化的曲线如图所示。下列说法正确的是( ) 的pH随温度变化的曲线如图所示。下列说法正确的是( )
A . 随温度升高,纯水中
 B . 随温度升高,
B . 随温度升高,  的溶液的 的溶液的  减小
C . 随温度升高, 减小
C . 随温度升高,  的溶液的pH变化是 的溶液的pH变化是  改变与水解平衡移动共同作用的结果
D . 随水温升高, 改变与水解平衡移动共同作用的结果
D . 随水温升高,  溶液和 溶液和  溶液的pH均降低,是因为 溶液的pH均降低,是因为  、 、  水解平衡移动方向不同 水解平衡移动方向不同
|
|
| 4. 单选题 | 详细信息 |
|
反应
 , ,  在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( ) 在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
A . 增大容器容积
B . 升高反应温度
C . 分离出部分氢气
D . 等容下通入惰性气体
|
|
| 5. 多选题 | 详细信息 | ||||||||||||
|
一定温度下,向容积为2 L的密闭容器中充入一定量的气体A和气体B,发生反应: 2A(g)+B(g)
 2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是( ) 2C(g),反应过程中测定部分数据见下表(表中t1<t2),下列说法正确的是( )
A . 在0~t1 min内的平均反应速率为v(C)=0.088/t1 mol•L-1•min-1
B . 其他条件不变,起始时向容器中充入0.10 mol C和0.010 mol B,平衡时n(A)=0.012 mol
C . 保持其他条件不变,升高温度,平衡时c(A)=0.0070 mol•L-1 , 则反应的ΔH>0
D . 相同温度下,起始时向容器中充入0.15mol A和0.090mol B,平衡时A转化率大于88%
|
|||||||||||||
| 6. 单选题 | 详细信息 |
|
已知
 呈粉红色, 呈粉红色,  呈蓝色, 呈蓝色,  为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: 为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:  ,用该溶液做实验,溶液的颜色变化如下: ,用该溶液做实验,溶液的颜色变化如下: 以下结论和解释正确的是( )
A . 等物质的量的
 和 和  中σ键数之比为3:2
B . 由实验①可推知△H<0
C . 实验②是由于c(H2O)增大,导致平衡逆向移动
D . 由实验③可知配离子的稳定性: 中σ键数之比为3:2
B . 由实验①可推知△H<0
C . 实验②是由于c(H2O)增大,导致平衡逆向移动
D . 由实验③可知配离子的稳定性: 
|
|
| 7. 单选题 | 详细信息 |
|
一定条件下:
  。在测定 。在测定  的相对分子质量时,下列条件中,测定结果误差最小的是( ) 的相对分子质量时,下列条件中,测定结果误差最小的是( )
A . 温度
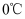 、压强 、压强  B . 温度
B . 温度  、压强 、压强  C . 温度
C . 温度  、压强 、压强  D . 温度
D . 温度  、压强 、压强 
|
|
| 8. 多选题 | 详细信息 |
|
催化剂存在下,在1 L的恒容密闭容器中充入0.1 molCO和0.3mol H2发生反应CO(g)+3H2(g)
 CH4(g)+H2O(g)。反应相同时间,CO的转化率与反应温度的关系如图所示。下列说法一定正确的是( ) CH4(g)+H2O(g)。反应相同时间,CO的转化率与反应温度的关系如图所示。下列说法一定正确的是( )
A . 升高温度,CO(g)+3H2(g)
 CH4(g)+H2O(g)的化学平衡常数增大
B . 图中X点所示条件下,延长反应时间能提高CO的转化率
C . 图中Y点所示条件下,改用性能更好的催化剂能提高CO的转化率
D . T1 ℃,CO(g)+3H2(g) CH4(g)+H2O(g)的化学平衡常数增大
B . 图中X点所示条件下,延长反应时间能提高CO的转化率
C . 图中Y点所示条件下,改用性能更好的催化剂能提高CO的转化率
D . T1 ℃,CO(g)+3H2(g)  CH4(g)+H2O(g)的化学平衡常数K>1 CH4(g)+H2O(g)的化学平衡常数K>1
|
|
| 9. 多选题 | 详细信息 |
|
T℃时,在密闭容器中进行的反应:COCl2(g)⇌CO(g)+Cl2(g)△H=108kJ·mol-1 , 在4min、10min、14min时均只改变影响平衡的一个条件,各物质的浓度变化如图所示:
下列说法正确的是( )
A . 4min时改变的条件是:降低体系的温度
B . 10min时改变的条件是:向体系中再充入Cl2
C . 14min时改变的条件是:增大容器的体积
D . 若T℃时,起始向2L的恒容密闭容器中充入COCl2、Cl2、CO均为0.20mol,则达到平衡前,v正>v逆
|
|
| 10. 多选题 | 详细信息 |
|
三个容积相同的恒容密闭容器中各自充入1 mol CO和一定量的H2 , 分别在T1、T2、T3温度下发生如下反应:CO(g)+2H2(g)
 CH3OH(g)△H<0。当反应达到平衡状态时,测得CO的转化率与投料比[ CH3OH(g)△H<0。当反应达到平衡状态时,测得CO的转化率与投料比[  ]的关系如下图所示。下列说法正确的是( ) ]的关系如下图所示。下列说法正确的是( )
A . H2的平衡转化率:a>b>c
B . 上述三种温度之间大小关系为T1>T2>T3
C . a点状态下再通入0.5 mol CO和0.5 mol CH3OH,平衡向正方向移动
D . c点状态下再通入1 mol CO和4 mol H2 , 新平衡中CH3OH的体积分数增大
|
|
高中化学 试卷推荐
- 吉林长春市榆树高级中学2019-2020学年高二下学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题27 化石燃料与有机化合物
- 北京市丰台区2018-2019学年高二上学期化学期中考试试卷
- 湖南省株洲市2017-2018学年高考理综-化学二模考试试卷
- 北京市东城区2015-2016学年高一上学期化学期末考试试卷
- 2016年上海市闵行区高考化学一模试卷
- 2015-2016学年四川省资阳市高一上学期期末化学试卷
- 福建省龙岩市2017-2018学年高考理综-化学4月模拟考试试卷
- 2015-2016学年广东省茂名市高州中学高二下学期期末化学试卷
- 2016-2017学年河南省焦作市高二上学期期中化学试卷
- 天津市河北区2020年高考化学二模试卷
- 高中化学人教版 必修1 第四章第三节硫和氮的氧化物 二氧化硫和三氧化硫
最近更新
- 孙中山领导的辛亥革命实现了20世纪中国第一次历史性巨变,因为这次革命()A、结束了帝国主义在中国的殖民统治 B、
- 马克思在《<黑格尔法哲学批判>导言》中写道:“路德战胜了信神的奴役制,只是因为他用信仰的奴役制代替了它。”“
- —Whydo you want to work for our company? —Thisis the job tha
- He can’t help __ housework, for he is busy __ for the examin
- 几种短周期元素的原子半径及主要化合价如下表: 元素代号 X Y Z W 原子半径/pm 160 143 70 66 主要
- To the great ______ of the youngwriter, his first book sell
- 以下学校某选修课学习小组对艺术楼附近湖泊进行的测定。 步骤1:取两个相同的透明玻璃瓶,分别编号为1号、2号。 步骤2:用
- 下列金属的活动性最弱的是() A.Mg B.Zn C.Cu D.Ag
- 已知:2CH3COCH3(1)CH3COCH2COH(CH3)2(1)。取等量CH3COCH3分别在0℃和20℃下反应,
- .图6中的人物是在19世纪末我国的一次变法运动中被杀害的,这次变法的主 要内容有 ①鼓励私人兴办工矿企业
- 下列各组词语中,有错别字的一组是( ) A、云蒸霞蔚/蔚然成风 博闻强识/一文不名 从中斡旋/剑戟乱舞
- 设满足约束条件的最大值为12,则的最小值为________.
- 由两个氨基酸分子缩合脱掉1个水分子可以生成二肽,丙氨酸和苯丙氨酸混合,在一定条件下生成的二肽分子的种类是( ) A
- Tom wants to study at ___________university in Europe, but h
- 如图所示,光滑绝缘斜面的底端固定着一个带正电的小物块P,将另一个带电小物块Q在斜面的某位置由静止释放,它将沿斜面向上运动
- 材料一、二、三是昆明和贵阳的气候资料,据此回答下列问题。 (材料一)四季分配示意图 (材料二
- 卤代烃在醚类溶剂中与Mg反应可制得格氏试剂,格氏试剂在有机合成方面用途广泛。设R为烃基,已知: 试回答下列问题:(1)C
- 下列有关实验现象的描述中,正确的是 A.铁丝在空气中燃烧时,火星四射,生成黑色固体四氧化三铁 B.红磷在氧气中燃烧时
- 空山新雨后, 。 , 。 ,
- He saidhis sister had passed the entrance examination of col










