高考二轮复习知识点:晶胞的计算5
高考二轮复习知识点:晶胞的计算5
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
NaCl晶体结构如图所示,现测知NaCl晶体中Na+与Cl﹣平均距离为a cm,该晶体密度为ρg•cm﹣3 , 则阿伏加德罗常数可表示为( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 2. 单选题 | 详细信息 |
|
SiO2是合成“中国蓝”的重要原料之一。如图是SiO2晶胞中Si原子沿z轴方向在xy平面的投影图(即俯视投影图,O原子略去。),Si原子旁标注的数字是Si原子位于z轴的高度,则SiA与SiB的距离是( )
A .
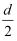 B .
B . 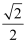 d
C . d
C . 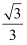 d
D . d d
D . d
|
|
| 3. 多选题 | 详细信息 |
|
M的硫化物有MS和M2S两种。已知:二者晶胞中
 的位置如图1所示,M离子位于硫离子所构成的四面体中如图2所示(○表示M离子,●表示 的位置如图1所示,M离子位于硫离子所构成的四面体中如图2所示(○表示M离子,●表示  )。下列说法错误的是( ) )。下列说法错误的是( )
A .
 的排列方式与ZnS中 的排列方式与ZnS中  相似
B . 在MS晶胞中如果A处 相似
B . 在MS晶胞中如果A处  的坐标为(0,0,0),一个 的坐标为(0,0,0),一个  的坐标为( 的坐标为(  ),则在( ),则在(  )处也存在 )处也存在  C . MS晶胞中,距离
C . MS晶胞中,距离  最近的 最近的  为4个
D . MS和M2S晶胞的俯视图均为 为4个
D . MS和M2S晶胞的俯视图均为 
|
|
| 4. 综合题 | 详细信息 |
|
金属羰基配位化合物在催化反应中有着重要应用。HMn(CO)5是锰的一种简单羰基配位化合物,其结构示意图如下。
回答问题:
|
|
| 5. 单选题 | 详细信息 |
|
单质硫和氢气在低温高压下可形成一种新型超导材料,其晶胞如图。下列说法错误的是( )
A . S位于元素周期表p区
B . 该物质的化学式为
 C . S位于H构成的八面体空隙中
D . 该晶体属于分子晶体
C . S位于H构成的八面体空隙中
D . 该晶体属于分子晶体
|
|
| 6. 综合题 | 详细信息 |
|
铁单质及其化合物的应用非常广泛。
|
|
| 7. 单选题 | 详细信息 |
|
某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
A . 该晶胞的体积为a3×10-36cm-3
B . K和Sb原子数之比为3∶1
C . 与Sb最邻近的K原子数为4
D . K和Sb之间的最短距离为
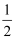 apm apm
|
|
| 8. 多选题 | 详细信息 |
|
普鲁士蓝晶胞的
 结构如图所示(K+未标出),下列说法正确的是( ) 结构如图所示(K+未标出),下列说法正确的是( )
A . 化学式可以表示为KFe2(CN)6
B . 每一个立方体中平均含有24个π键
C . 一个晶胞中K+的个数为4个
D . 每个Fe3+周围与之相邻的Fe2+有12个
|
|
| 9. 多选题 | 详细信息 |
|
晶胞是描述晶体结构的基本单元。下列示意图中(不同的小球代表不同的原子或离子)可以表示化学式为AB2型化合物晶胞的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 10. 综合题 | 详细信息 |
|
氮元素是地球上含量丰富的一种元素,不仅是制造农药、医药的重要元素,也是构成蛋白质的重要元素。根据所学知识回答以下问题。
|
|
高中化学 试卷推荐
- 江苏省淮安市2015-2016学年高一下学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题30 物质的分离、提纯和检验
- 河南省南阳市2016-2017学年高二下学期化学期末考试试卷
- 河南省商丘市2019-2020学年高一下学期化学期末考试试卷
- 2017年高考化学备考复习专题十五:油脂、糖类、蛋白质和核酸
- 高中化学人教版(2019)必修第一册第三章第一节铁及其化合物
- 吉林省长春汽车经济技术开发区第六中学2019-2020学年高一下学期化学期末考试试卷
- 专题22:有机化合物的命名
- 山东省济南市2017-2018学年高考理综-化学二模考试试卷
- 2016-2017学年江苏省泰州市姜堰区高二上学期期末化学试卷(必修)
- 2015-2016学年天津市静海县六校联考高二下学期期中化学试卷
- 2019年高考化学真题分类汇编专题01:化学与生活
最近更新
- 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:则下列说法正确的是A.放电时:电子流动方向由A经
- 有关下列四幅图的叙述,正确的是()A.甲图中共有8种核糖核苷酸 B.乙图所示的化合物中不含糖类物质 C.组成丙物质的单糖
- 对于0£x£100,用[x]表示不超过x的最大整数,则[x]+[x]的不同取值的个数为( )。A.267B.2
- 如图2所示,甲卫星绕地球做椭圆运动,其轨道近地点为a,远地点为b,已知乙卫星过a点做圆周运动的速率为v,则甲卫星(
- 已知:一个碳原子上连有两个羟基时,易发生下列转化:请根据下图作答: (1)A的核磁共振氢谱中出现 组峰;E
- 对比太平天国运动和义和团运动的异同。
- Look at the timetable. Hurry up! Flight 4026 ______ off at 1
- 常温下能用铁罐或铝罐贮存的是 (
- 谷氨酸的R基为-C3H5O2,在一个谷氨酸分子中,含有碳和氧的原子数分别是( ) A.4,4 B.5,4
- 如图甲为电热毯的电路图,把电热毯接在U=311sin100πtV的电源上,电热毯被加热到一定温度后,通过装置P使输入电压
- 下列说法中正确的是() A.用煮沸的方法可以区分硬水和软水 B.用灼烧的方法可以鉴别羊毛和涤纶 C.催化剂在化学反应前后
- 是双曲线的两个焦点,点P在双曲线上且满足, 则 ————
- “忽如一夜春风来,千树万树梨花开”是指 A.天气 B.气候
- 质量为m的体操运动员,双臂竖直悬吊在单杠下,当他如图增大双手间距离时 A.每只手臂的拉力将减小 B.每只手臂的拉力可能等
- My little dog is lost. All of my friends are helping me to _
- 物体甲的速度与时间图象和物体乙的位移与时间图象分别如图所示,则这两个物体的运动情况是( )
- 填写下列名篇名句中的空缺 (任选5空)。 (1)曲终收拔当心画,四弦一声如裂帛。________,______。(白居易
- A traveler was staying in an Egyptian village.One day, she h
- Itwas in the lab ______ was taken charge of by Pro. Harris
- 下列各项中,属于食物链的是 ( ) A、阳光→草→兔




 中碳原子的杂化轨道类型是,写出一种与具有相同空间结构的-1价无机酸根离子的化学式。
中碳原子的杂化轨道类型是,写出一种与具有相同空间结构的-1价无机酸根离子的化学式。

 ,b点锰原子坐标为
,b点锰原子坐标为  ,则c点锰原子坐标为。
,则c点锰原子坐标为。


 、
、  、
、  。某同学按如下步骤完成实验:
。某同学按如下步骤完成实验: 
 ;
;  ,向溶液Ⅱ中加入NaF后,溶液颜色由红色转变为无色。若该反应是可逆反应,其离子方程式为,平衡常数为(用K1和K2表示)。
,向溶液Ⅱ中加入NaF后,溶液颜色由红色转变为无色。若该反应是可逆反应,其离子方程式为,平衡常数为(用K1和K2表示)。

 离子的空间构型为
离子的空间构型为




