高考二轮复习知识点:热化学方程式2
高考二轮复习知识点:热化学方程式2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
标准状态下,气态分子断开1mol化学键的焓变为键焓.已知H﹣H,H﹣O和O=O键的键焓△H分别为436kJ•mol﹣1、463kJ•mol﹣1和495kJ•mol﹣1 . 下列热化学方程式正确的是( )
A . H2O(g)═H2(g)+
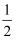 O2(g)△H=﹣485kJ•mol﹣1
B . H2O(g)═H2(g)+ O2(g)△H=﹣485kJ•mol﹣1
B . H2O(g)═H2(g)+ 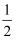 O2(g)△H=+485kJ•mol﹣1
C . 2H2(g)+O2(g)═2H2O(g)△H=+485kJ•mol﹣1
D . 2H2(g)+O2(g)═2H2O(g)△H=﹣485kJ•mol﹣1 O2(g)△H=+485kJ•mol﹣1
C . 2H2(g)+O2(g)═2H2O(g)△H=+485kJ•mol﹣1
D . 2H2(g)+O2(g)═2H2O(g)△H=﹣485kJ•mol﹣1
|
|
| 2. 综合题 | 详细信息 |
|
(14分)近期发现,H2S是继NO、CO之后第三个生命体系气体信号分子,它具有参与调解神经信号传递、舒张血管减轻高血压的功能.回答下列问题:
|
|
| 3. 单选题 | 详细信息 |
|
1mol碳在氧气中完全燃烧生成气体,放出393kJ的热量,下列热化学方程式表示正确的是( )
A . C(s)+O2(g)→CO2(g)+393kJ
B . C + O2→ CO2+393kJ
C . C (s) + O2 (g)→CO2 (g)-393kJ
D . C (s) +1/2O2 (g) → CO(g) +393kJ
|
|
| 4. 单选题 | 详细信息 |
|
图分别表示红磷、白磷燃烧时的能量变化,下列说法中正确的是( )
A . 白磷比红磷稳定
B . 白磷燃烧产物比红磷燃烧产物稳定
C . 1mol白磷转变为红磷放出2244.7kJ的热量
D . 红磷燃烧的热化学方程式:4P(s)+5O2(g)=P4O10(s)△H=-2954kJ⋅mol−1
|
|
| 5. 单选题 | 详细信息 |
|
已知:2H2(g)+O2(g)→2H2O (g)+ 483.6 kJ,2H2(g)+O2(g)→2H2O (l)+ 571.6 kJ;图中示意正确的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 6. 单选题 | 详细信息 |
|
肼(N2H4)在不同条件下分解产物不同,200℃时在Cu表面分解的机理如图。已知200℃时:反应Ⅰ:3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1反应Ⅱ:N2H4(g)+H2(g)2NH3(g)ΔH2=-41.8 kJ·mol-1
下列说法错误的是( )
A . 图所示过程①是放热反应
B . 反应Ⅱ的能量过程示意图如图所示
C . 断开3 mol N2H4(g)的化学键吸收的能量大于形成1 molN2(g)和4 mol NH3(g)的化学键释放的能量
D . 200℃时,肼分解生成氮气和氢气的热化学方程式为N2H4(g)=N2(g)+2H2(g)ΔH=+50.7 kJ·mol-1
|
|
| 7. 单选题 | 详细信息 |
|
已知在25 ℃、1.01×105 Pa下,1mol氢气在氧气中燃烧生成气态水的能量变化如下图所示,下列有关说法正确的是( )
A . H2O分解为H2与O2时放出热量
B . 热化学方程式为:2H2(g) + O2(g) = 2H2O(g) ΔH = -490 kJ·mol-1
C . 甲、乙、丙中物质所具有的总能量大小关系为甲>乙>丙
D . 乙→丙的过程中若生成液态水,释放的能量将小于930 kJ
|
|
| 8. 单选题 | 详细信息 |
|
以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
相关反应的热化学方程式为: 反应I:SO2(g) + I2(g) + 2H2O(l) = 2HI(aq) + H2SO4(aq) ΔH1 =﹣213 kJ·mol-1 反应II:H2SO4(aq) = SO2(g) + H2O(l) + 反应III:2HI(aq) = H2(g) + I2(g) ΔH3 = +172 kJ·mol-1 下列说法错误的是:( )
A . 该过程实现了太阳能到化学能的转化
B . SO2和I2对总反应起到了催化剂的作用
C . 总反应的热化学方程式为:2H2O(l) = 2H2 (g)+O2(g) ΔH = +286 kJ·mol-1
D . 该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变
|
|
| 9. 单选题 | 详细信息 |
|
通过以下反应均可获取H2。下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)=2H2(g)+O2(g) ΔH1=+571.6 kJ·mol-1 ②焦炭与水反应制氢:C(s)+H2O(g) =CO(g)+H2(g) ΔH2=+131.3 kJ·mol-1 ③甲烷与水反应制氢:CH4(g)+H2O(g) =CO(g)+3H2(g) ΔH3=+206.1 kJ·mol-1
A . 反应①中电能转化为化学能
B . 反应②为放热反应
C . 反应③使用催化剂,ΔH3减小
D . 反应CH4(g)=C(s)+2H2(g)的ΔH=+74.8 kJ·mol-1
|
|
| 10. 单选题 | 详细信息 |
|
根据下图所得判断正确的是( )
已知:H2O(g) = H2O(l) △H =﹣44 kJ/mol
A . 图 1 反应为吸热反应
B . 图 1 反应使用催化剂时,会改变其△H
C . 图 2 中若 H2O 的状态为液态,则能量变化曲线可能为①
D . 图 2 中反应为 CO2(g) + H2(g) = CO(g) + H2O(g) △H = + 41 kJ/mol
|
|
高中化学 试卷推荐
- 2016-2017学年湖北省四地七校高二上学期期中化学试卷
- 人教版高中化学选修五 第三章 烃的含氧衍生物——单元综合检测题
- 2016-2017学年陕西省延安市实验中学大学区校际联盟高二上学期期中化学试卷(B)
- 吉林省吉林市第三中学2018-2019学年高一下学期化学期中考试试卷
- 河南省周口市2016-2017学年高二下学期化学期末考试试卷
- 2017年高考化学备考复习专题十一:水溶液中的离子平衡
- 2016-2017学年吉林省吉林油田实验中学高二上学期期中化学试卷
- 天津市五校联考2016-2017学年高一上学期化学期末考试试卷
- 黑龙江省牡丹江市绥芬河高级中学2019-2020学年高一上学期化学期末考试试卷
- 陕西省西安市2019-2020学年高一上学期化学期末考试试卷
- 湖南省武冈市2017-2018学年高二下学期理综-化学模拟考试试卷
- 山东省德州市2019-2020学年高二下学期化学期末考试试卷
最近更新
- 英国资产阶级革命、美国独立战争、俄国1861年改革、日本明治维新的共同作用是() A.推翻了殖民统治
- “温室效应”是全球关注的环境问题之一,二氧化碳是目前大气中含量最高的一种温室气体,实现碳循环、促进CO2转化为有机物和
- 化简
- What exactly does the sign_______? A. stand for
- 在映射,,且,则与A中的元素对应的B中的元素为( ) A. B. C. D.
- 第二学期期末考试试卷
- 由于受金融危机的影响,某店经销的甲型号手机今年的售价比去年每台降价500元.如果卖出相同数量的手机,那么去年销售额为8万
- 人体缺少钙、铁等元素会影响身体健康。下列补充化学元素的做法错误的是() A.大量服用含碘药物预防甲状腺肿大 B.使用铁制
- 在香水玫瑰的花色遗传中,红花、白花为一对相对性状,受一对等位基因的控制(用R、r表示)。从下面的杂交实验中可以得出的正确
- 如图3-13所示,质量为m的等边三棱柱静止在水平放置的斜面上.已知三棱柱与斜面之间的动摩擦因数为μ,斜面的倾角为30°,
- 元宵节是我国主要的传统节日,因历代这一节日有观灯习俗,故又称灯节。元宵节风俗的形成有一个较长的过程,据一般的资料与民俗传
- 函数的图象大致是() A B C
- 下列家庭实验中不涉及化学变化的是 A.用少量食醋除去水壶中的水垢 B.用糯米、酒曲和水制甜酒酿 C.用
- 据《剑桥中国史》记载:第一个五年计划是一个令人吃惊的成功。国民收入年平均增长率为8.9%,农业和工业产量的增长率每年分别
- 函数f(x)=x3-3x+1在闭区间[-3,0]上的最大值、最小值分别是( ) A.1,-1
- 一位运动员在跳马比赛中,不幸摔倒而造成下肢截瘫,可能摔伤的部位是:( )A、大脑 B、小脑 C
- 时人评说:“举秀才不知书,举孝廉父别居。寒素清白浊如泥,高第良将怯如鸡。”对这番话,下列理解与史实相符的是 A.东汉察举
- --- How about eight o’clock outside the cinema?--- That ____
- 点M(1,2)关于x轴对称的点的坐标为: A.(—1,2) B.(-1,-2) C.(1,-2) D.
- 恩格斯说:“推动哲学家前进的,绝不像他们所想象的那样,只是纯粹思想的力。 恰恰相反,真正推动他们前进的,主要是自然科学和





 O2(g) ΔH2 = +327 kJ·mol-1
O2(g) ΔH2 = +327 kJ·mol-1



