福建省厦门市2021-2022学年高一下学期期末考试化学试题
福建省厦门市2021-2022学年高一下学期期末考试化学试题
教材科目:化学
试卷分类:高一下学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高一下学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
厦门中学生助手将铜催化剂与富勒烯(C60)相关联实现常压下合成乙二醇。下列说法正确的是( )
A . C60为有机高分子化合物
B . 反应①反应类型为加成反应
C . 反应②中碳氧键未发生变化
D . C60 - Cu/SiO2可加快反应②反应速率
|
|
| 2. 单选题 | 详细信息 |
|
下列化学用语或模型正确的是( )
A . 氮气的电子式:
|
|
| 3. 单选题 | 详细信息 |
|
下列有关元素周期律的说法正确的是( )
A . 离子半径:K+>Ca2+>Al3+
B . 元素原子得电子能力:P>S>Cl
C . 碱性:Be(OH)2>Ca(OH)2
D . 热稳定性:CH4>NH3
|
|
| 4. 单选题 | 详细信息 |
|
一种高活性有机物中间体分子结构如图。下列有关该物质说法错误的是( )
A . 分子式为C10H12O2
B . 含有两种官能团
C . 苯环上的一氯代物有4种
D . 1mol该有机物与足量金属Na反应可产生H2 22.4L(标况下)
|
|
| 5. 单选题 | 详细信息 |
|
厦门中学生助手的下列实验能达到目的的是( )
A . 图A是米酒蒸馏
B . 图B是除甲烷中的乙烯
C . 图C是制备乙酸乙酯
D . 图D是分离乙醇和溴水
|
|
| 6. 单选题 | 详细信息 |
|
厦门中学生助手在一定条件下,向密闭容器中充入18O2和SO2发生反应
 。下列说法正确的是( ) 。下列说法正确的是( )
A . 反应一段时间后,含有18O的分子只有O2和SO3
B . 达到平衡后,反应生成的SO3不再分解
C . 反应混合物中SO2、O2的物质的量之比为2:1时,说明反应已达平衡状态
D . 当SO3的消耗速率等于O2消耗速率的2倍时,说明反应已达平衡状态
|
|
| 7. 单选题 | 详细信息 |
|
根据下列信息判断N2和O2反应生成NO时的能量变化。下列说法正确的是( )
A . NO(g)分解为N2(g)与O2(g)时需要释放能量
B . N2(g)和O2(g)反应生成1molNO(g)时放出能量630kJ
C . 断开氧氧键形成1mol氧原子需要吸收能量498kJ
D . 1mol N2(g)的能量高于1mol NO(g)
|
|
| 8. 单选题 | 详细信息 |
|
化学研究小组设计了一款低成本、高性能的铁—氢气电池,装置如图,其总反应式为:
 。下列说法错误的是( ) 。下列说法错误的是( )
A . 负极反应式为
 B . 工作一段时间后,电解质溶液的pH降低
C . 理论上生成
B . 工作一段时间后,电解质溶液的pH降低
C . 理论上生成 时,外电路中有1 mol电子发生转移
D . 工作时,电解质溶液中的K+向Pt/C电极移动 时,外电路中有1 mol电子发生转移
D . 工作时,电解质溶液中的K+向Pt/C电极移动
|
|
| 9. 单选题 | 详细信息 |
|
L、M、Q、R、X、Y为短周期主族元素,L、M、Q、R、X元素原子半径与最外层电子数的关系如图,原子序数Y=M+X。下列说法错误的是( )
A . 位于第二周期的元素有M、Q
B . 元素R的氢化物稳定性大于Y元素氢化物
C . L与X形成的化合物为离子化合物
D . Q元素最高价氧化物对应水化物酸性强于M
|
|
| 10. 单选题 | 详细信息 |
|
五硼酸铵晶体(NH4B5O8∙4H2O)主要用于电讯器材的制造。化学研究小组采用硼镁矿(主要成分为Mg2B2O5∙H2O),还有少量的(CaO、SiO2等杂质)制备NH4B5O8∙4H2O晶体并对其进行热重分析,其制备流程及热重曲线如图所示。下列说法正确的是( )
A . “操作X”为蒸发结晶至质量不再变化
B . “沉硼”时,温度越高,沉硼率越高
C . NH4B5O8∙4H2O晶体中
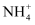 的结合程度比H2O牢固
D . 400 ~ 500℃热分解失去一个结晶水 的结合程度比H2O牢固
D . 400 ~ 500℃热分解失去一个结晶水
|
|
高中化学 试卷推荐
- 山西省晋中市2021年高考化学三模试卷
- 广东省省名校联盟2020-2021学年高三下学期化学开学考试试卷(新高考)
- 湖南省益阳市2021-2022学年高二上学期期末考试化学试题
- 湖北省鄂西六校2021-2022学年高二下学期期中联考化学试题
- 上海市浦东新区2021年高考化学二模试卷
- 上海市宝山区2022届高三年级下学期二模考试化学试题
- 江西省抚州市2021-2022学年高一上学期期末学业质量检测化学试题
- 广东金太阳大联考2021-2022学年高三上学期化学开学考试试卷
- 湖北省武汉市蔡甸区高中2020-2021学年高一下学期化学5月月考试卷
- 安徽省芜湖市2020-2021学年高二上学期期末教学质量监测化学试题
- 辽宁省凌源市 2021-2022学年高二下学期开学考试化学试题
- 河北省邢台市2020-2021学年高一下学期期末考试化学试题
最近更新
- 下列各组词语中加点字的读音,完全正确的一组是() A.吝啬(sè) 自诩(yǚ) 糟粕(pò) 残羹冷炙(zhì)
- During the World Cup in Brazil, football became thehot topic
- 下列选项对公式认识正确的是() A. 公式E=k可以用来求平行板电容器两极板间的匀强电场的电场强度,其中Q为一极
- 图为某生态系统中的食物网,根据图回答有关问题:(1) 图中生产者是__________________,该食物网中共有5
- The performance _______ nearly three hours, but few people l
- 锌铜原电池装置如图所示,其中阳离子交换膜只允 许阳离子和水分子通过,下列有关叙述正确的是()A.铜电极上发生氧化反应 B
- 硝化细菌的碳源、氮源、能源依次是 ( ) A.葡萄糖、氨、葡萄糖
- 衡量一个国家或地区城市化水平高低的重要标志是( ) A.城市的用地规模 B.城市的人口数量 C.城市的数量
- He has the habit of ________ useful information while readin
- 图1为“某半岛局部区域等高线地形图(单位:米)”,读图完成 1~2 题。1.T1107公路有多处弯曲,不合理之处最可能是
- “鸟宿池边树,僧推月下门”这句诗描述了和尚在月光下轻轻推开寺门的美妙情景,该和尚在伸肘时,其肱二头肌和肱三头肌分别属于
- 依次填入下面一段文字横线处的语句,衔接最恰当的一组是 ( )
- 改革开放以来,我国城乡居民储蓄大幅度增加。据统计,到2007年底,我国城乡居民储蓄存款余额已超过172534亿元。据此完
- 下列示意图中,能表示阴离子的是() A. B. C. D.
- 下列各处名胜、按纬度由高向低,依次排列的是:() A.岳阳楼、日月潭、秦兵马俑、悬空寺B.秦兵马俑、岳阳楼、日月潭、悬空
- It’s hard to finish the work in a day. You’d better ____ you
- .设函数f1(x)=,f2(x)=x-1,f3(x)=x2,则f1(f2(f3(2 013)))=.
- 2.下列各组词语中没有错别字的一组是 A.暮蔼 杳无音讯 欺侮 瞻仰 B.磨蹭 哀声叹气 癖好 哆嗦 C.
- ---Who’s ___________ boy in red, do you know? ---Oh. He’s __
- 下图是某细胞进行有丝分裂的简图,据图回答:(“[ ]”内填序号,“ ”上按要求填数字、文字或字母)(1)图示作










