高考二轮复习知识点:电镀
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在化学能与电能的转化过程中,下列叙述正确的是( )
A . 电解饱和食盐水时,阳极得到Cl2和NaOH(aq)
B . 教材所示的铜﹣锌原电池在工作时,Zn2+向铜片附近迁移
C . 电镀时,电镀槽里的负极材料发生氧化反应
D . 原电池与电解池连接后,电子从原电池负极流向电解池阳极
|
|
| 2. 综合题 | 详细信息 |
|
某研究性学习小组将甲、乙、丙装置连接如图,除G、H外所有电极均为惰性电极。电解一段时间后,D电极质量增加。试回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
|
已知:①甲为 CH4 和
O2 形成的燃料电池,电解质为固体电解质,能传导 O2-。
②乙中为 100 mL NaCl 溶液(足量),滴有酚酞,丙为 CuSO4 溶液。 ③若 c、d 为惰性电极,通电时 c 电极附近首先出现红色。 请回答下列问题:
|
|
| 4. 实验探究题 | 详细信息 |
|
如下图所示的装置,C、D、E、F都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答以下问题:
|
|
| 5. 单选题 | 详细信息 |
|
某二次电池装置如图所示,锂、充有催化剂的碳纳米管为电极,电解质能传导Li+。放电时生成的Li2CO3和C附着在电极上,充电时可使Li2CO3转化为Li、CO2和O2。下列说法错误的是( )
A . 放电时,电流从电极Y经外电路流向电极X
B . 充电时,电极X接外电源的正极发生氧化反应
C . 充电时,电极Y的电极反应式为2Li2CO3-4e-=2CO2↑+O2↑+4Li+
D . 应用该电池电镀铜,若析出64gCu,理论上消耗标况下33.6LCO2
|
|
| 6. 综合题 | 详细信息 |
|
Ni常被镀在金属制品上以保护金属不生锈。
|
|
| 7. 单选题 | 详细信息 |
|
如下图所示,某同学设计了一个燃料电池并探究铜的精炼原理和电镀原理。下列说法正确的是( )
A . 一段时间后,甲装置中溶液 pH升高
B . 电解一段时间后,乙、丙装置中 CuSO4溶液的浓度均不变
C . 通入氧气的一极为正极,发生的电极反应为
 D . 丙装置中实现铁片上镀铜,b 应为铁片
D . 丙装置中实现铁片上镀铜,b 应为铁片
|
|
| 8. 综合题 | 详细信息 | ||||||||||
|
某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中含有
 70.0%及一定量的 70.0%及一定量的  、 、  、 、  和有机物,镍及其化合物的化学性质与铁的类似,但 和有机物,镍及其化合物的化学性质与铁的类似,但  的性质较稳定)。回答下列问题: 的性质较稳定)。回答下列问题: 已知:部分阳离子以氢氧化物的形式完全沉淀时的
|
|||||||||||
| 9. 单选题 | 详细信息 |
|
利用如图所示装置模拟电解原理在工业生产中的应用,下列说法正确的是( )
A . 氯碱工业中,X电极上的反应式是4OH--4e-=2H2O+O2↑
B . 电解精炼铜时,Z溶液中的Cu2+浓度不变
C . 在铁片上镀铜时,每转移2mol电子,Y极增重64g
D . 制取金属铝时,Z是熔融的氯化铝
|
|
| 10. 综合题 | 详细信息 |
|
某小组以软锰矿、闪锌矿为原料,尝试在铁钉表面镀锌及制取高纯
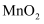 。流程如下: 。流程如下: 已知:①矿粉的主要成分是 ②酸浸时反应之一: ③ 请回答:
|
|
- 江苏省扬州市2020-2021学年高三下学期化学开学考试试卷
- 山西省吕梁市2020-2021学年高二下学期期末考试化学试题
- 山东省青岛胶州市2020-2021学年高一下学期化学期中考试试卷
- 河南省洛阳市2020-2021学年高三上学期化学期中考试试卷
- 四川省宜宾市2022届普通高中高考适应性考试理科综合化学试题
- 陕西省渭南市大荔县2020-2021学年高一上学期期末考试化学试题
- 湖北省石首市2021-2022学年高二下学期期中考试化学试题
- 山东省潍坊市2020-2021学年高一上学期化学期末考试试卷
- 陕西省宝鸡市2021年高考化学5月模拟试卷
- 浙江省名校新高考研究联盟(Z20联盟)2020-2021学年高三上学期化学第二次月考试卷
- 广东省汕头市潮阳区2020-2021学年高二上学期化学期末考试试卷
- 备考2021年高考化学二轮专题 第2讲 非金属元素及其化合物
- 人体下丘脑不能完成的生理功能是 A.体温调节 B.水平衡调节 C.内分泌调节 D.血液pH值的调节
- 2013年3月14日,十二届全国人大一次会议审议通过了国务院机构改革和职能转变方案。这表明全国人大具有 A.立法权
- 下列有关“电”的说法正确的是 A.摩擦起电的实质是创造了电荷 B.运动的电荷一定形成电流 C.电路两端有电压就一定有电
- 依次填入各句横线上的成语,与句意最贴切的一组是( ) ①同学们,清除垃圾,搞好校园环境卫生,这是我们
- 下列实验操作正确的是()A.滴加液体 B.稀释浓硫酸 C.蒸发 D.熄灭酒精灯
- 新文化运动最主要的成果是( )A.动摇了封建思想的统治地位 B.民主和科学思想得到弘扬C.为五四运动的爆
- 如图是验证水生绿色植物光合作用的实验装置图,锥形瓶内装天然水和新鲜水草,瓶口用带有导管的橡皮塞塞紧,烧杯内为30℃左右的
- 乙两位同学同时为校文化艺术节制作彩旗.已知甲每小时比乙多做5面彩旗,甲做60面彩旗与乙做50面彩旗所用时间相等,问甲、乙
- .如图1,是一张关于“2009年中央政府投资预算”的新闻图片.请你根据图1给出的信息,解答下列问题 (1)2009年中央
- 下列各句中,没有语病的一项是( ) A.甘肃舟曲灾情牵动着我们的心,每一个有良知的中国人都应该关注和参与救助行动,因
- 设M=(-1)(-1)(-1),且a+b+c=1(其中a,b,c∈R+),则M的取值范围是…()A.[0,)B.[,1
- 农业一直是历代中国政府关注的重要问题之一,民本思想在我国政治、经济、思想史上,可谓源远流长。据此回答下题。 国家对农业进
- 俄罗斯人爱好的艺术是( ) A交响乐、芭蕾舞 B京剧、桑巴舞 C油画、摇滚乐
- 针对国内有效需求不足而居民的银行储蓄节节上升的趋势,许多专家呼吁国家应尽快完善社会保障制度,使居民老有所养,病有所医。通
- 一本好书,可以驱走人们的烦恼,可以净化人们的心灵,可以陶冶人们的情操。莫等待,莫犹豫,赶快到书籍的海洋尽情遨游吧!(4分
- 有人说,多党合作好比是交响乐团,在作曲的时候,大家都可以提意见,各民主党派都应积极参与,最后公认由中国博采众长来定谱。可
- 2010年3月13日,政协全国十一届三次会议上,政协委员们就经济发展、民生保障、文化教育等建言献策,会议提案组共计共收到
- 在△中,若,则△的形状为( ) A. 等腰三角形 B. 直角三角形 C.等腰直角三角形
- 关于曲线运动,以下说法中正确的是( ) A.物体的速度方向时刻在改变 B.物体的速度大小时刻在改变 C.物
- 某高等植物种群以严格的自花传粉方式繁殖。aa频率在逐年降低,原因是aa个体的生活力比较弱,平均每代约有3%的aa个体不能








 如下表所示。
如下表所示。



 的目的是,反应的离子方程式为
的目的是,反应的离子方程式为
 。滤液C
。滤液C  溶液D
溶液D 
 在强碱溶液中用
在强碱溶液中用  氧化,可制得碱性镍镉电池电极材料—
氧化,可制得碱性镍镉电池电极材料—  ,该反应的离子方程式是
,该反应的离子方程式是

 等。
等。 。该生产过程中,
。该生产过程中,  不反应。
不反应。 可换成
可换成 
 固体、足量稀
固体、足量稀  标准溶液滴定剩余
标准溶液滴定剩余  至终点。
至终点。 


