近三年高考化学真题分类汇编:化学键与物质的性质(2022年)
近三年高考化学真题分类汇编:化学键与物质的性质(2022年)
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | |||||||||||||||||||
|
回答下列问题:
|
||||||||||||||||||||
| 2. 综合题 | 详细信息 |
|
[化学——选修3:物质结构与性质]
卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
|
硒(
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(  )效应以来, )效应以来,  在发光材料、生物医学等领域引起广泛关注。一种含 在发光材料、生物医学等领域引起广泛关注。一种含  的新型 的新型  分子 分子  的合成路线如下: 的合成路线如下:
|
|
| 4. 单选题 | 详细信息 |
|
下列说法错误的是( )
A . 氢键、离子键和共价键都属于化学键
B . 化学家门捷列夫编制了第一张元素周期表
C . 药剂师和营养师必须具备化学相关专业知识
D . 石灰石是制造玻璃和水泥的主要原料之一
|
|
| 5. 实验探究题 | 详细信息 |
|
[选修3:物质结构与性质]
铁和硒(
|
|
| 6. 综合题 | 详细信息 |
|
|
| 7. 单选题 | 详细信息 |
 、 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在 键、 键、 键。下列说法错误的是( ) 键。下列说法错误的是( )
A .
 的熔点高于 的熔点高于 B . 晶体中所有化学键均为极性键
C . 晶体中所有原子均采取
B . 晶体中所有化学键均为极性键
C . 晶体中所有原子均采取 杂化
D . 晶体中所有原子的配位数均相同 杂化
D . 晶体中所有原子的配位数均相同
|
|
| 8. 多选题 | 详细信息 |
 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是( ) 是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是( )
A . 每个
 晶胞中 晶胞中 个数为x
B . 每个 个数为x
B . 每个 晶胞完全转化为 晶胞完全转化为 晶胞,转移电子数为8
C . 每个 晶胞,转移电子数为8
C . 每个 晶胞中0价Cu原子个数为 晶胞中0价Cu原子个数为 D . 当
D . 当 转化为 转化为 时,每转移 时,每转移 电子,产生 电子,产生 原子 原子
|
|
| 9. 综合题 | 详细信息 |
|
研究笼形包合物结构和性质具有重要意义。化学式为
 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为 。回答下列问题: 。回答下列问题:
|
|
| 10. 多选题 | 详细信息 |
|
已知
 , ,  的酸性比 的酸性比 强。下列有关说法正确的是( ) 强。下列有关说法正确的是( )
A . HCl的电子式为
 分子中只有σ键
D . 分子中只有σ键
D .  的酸性比 的酸性比 强 强
|
|
高中化学 试卷推荐
- 安徽省黄山市2020-2021学年高一上学期期末考试化学试题
- 安徽省江淮名校宣城2020-2021学年高一上学期期末考试化学试题
- 广西百色市2020-2021学年高二上学期期末教学质量调研测试化学试题
- 广西贵港市2020-2021学年高二上学期期末教学质量监测化学试题
- 广西桂林市2020-2021学年高二上学期期末质量检测化学试题
- 广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
- 广西来宾市2020-2021学年高二上学期期末教学质量检测化学试题
- 广西南宁市2020-2021学年高二上学期期末考试化学试题
- 广西钦州市2020-2021学年高二上学期期末教学质量监测化学试题
- 陕西省宝鸡市渭滨区2020-2021学年高二上学期期末考试化学试题
- 陕西省汉中市2020-2021学年高二上学期期末考试化学试题
- 广西北海市2020-2021学年高一上学期期末教学质量检测化学试题
最近更新
- 如图是模拟电化学反应装置图。下列说法正确的是A.开关K置于N处,则铁电极的电极反应式为:Fe-2e-===Fe2+ B.
- 12.下图为人体细胞所经历的生长发育各个阶段,图中①~⑦为不同的细胞,a~c表示不同的生理过程。下列叙述正确的是(
- 23. 洪仁玕在《资政新篇》中主张“外国有禁卖子为奴之例。家贫卖子,只顾眼前之便,不思子孙永为人奴,大辱祖考……故准富者
- 将状况相同的某种绿叶分成四等组,在不同温度下分别暗处理1 h,再光照1 h(光强相同),测其重量变化,得到如下表的数据。
- (5分)如图所示,质量为m的木块在量于水平桌面的木板上滑行,木板静止,它的质量M=3kg,已知木块与木板间,木板与桌面间
- (09年西城区抽样) 设向量a=(1, x-1),b=(x+1,3),则“x=2”是“a//b”的( )A. 充分但不
- 如图,火车匀速通过隧道(隧道长大于火车长)时,火车进入隧道的时间与火车在隧道内的长度之间的关系用图象描述大致是 A
- 在学校举行“阳光少年,励志青春”的演讲比赛中,五位评委给选手小明的评分分别为:90,85,90,80,95,则这组数据的
- The supermarket is______ the post office and the library. A.
- 梭伦改革对雅典民主政治的发展产生了重要影响。下列图片不能体现其影响的是 A.陶片放逐法 B.雅典人用石子投票表决
- 在建筑工地上有时需要将一些建筑材料由高处送到低处,为此工人们设计了一种如图所示的简易滑轨:两根圆柱形木杆AB和CD相互平
- 义和团运动教训了侵略者,使帝国主义认识到“无论欧美各国,皆无此脑力与兵力可以统治此天下生灵四分之一”,故瓜分一事,实为下
- 下列关于资源的叙述不正确的是( )A.自然界中水是循环的,可利用的淡水资源不会减少B.石油分馏可得到汽油、煤油等多
- 如图,AD是△ABC的外接圆直径,AD=,∠B=∠DAC,则AC的值为 ▲ .
- 在升降机中的水平底板上放一质量为60 kg的物体,如图4-6-10所示为升降机下降过程中的v-t图象,试通过计算作出底板
- 气体打火机使用一种有机化合物为燃料,这种燃料稍加压时易液化,减压时易气化,点燃能燃烧,它可能是 A.乙醇(沸点78.5℃
- 下列文学常识的表述不完全正确的一项是 ( ) A.《美丽的西双版纳》作者按总分
- 如图,已知∠ABC=∠DCB,下列所给条件不能证明△ABC≌△DCB的是() A.∠A=∠D B.AB=DC
- 阅读下面的文言文,完成下列各题。(每小题3分,共9分) 南越王尉佗者,真定人也,姓赵氏。秦时已并天下,略定杨越,置桂林、
- 读非洲气候分布图和非洲矿产分布图,回答下列问题:(1)在撒哈拉沙漠中埋藏着丰富的____________(矿产资源)。在
 b.
b. c.
c. d.
d.
 分子中,C的一个杂化轨道与
分子中,C的一个杂化轨道与 的
的 轨道形成
轨道形成 键,并且
键,并且 轨道与C的
轨道与C的 轨道形成3中心4电子的大
轨道形成3中心4电子的大 键
键 。
。 、一氯乙烯
、一氯乙烯 、一氯乙炔
、一氯乙炔 分子中,
分子中, 键长的顺序是,理由:(ⅰ)C的杂化轨道中s成分越多,形成的
键长的顺序是,理由:(ⅰ)C的杂化轨道中s成分越多,形成的 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为。解释X的熔点比Y高的原因。
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为。解释X的熔点比Y高的原因。
 晶体中
晶体中 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示), 主要分布在由
主要分布在由
 , 则
, 则 晶体的摩尔体积
晶体的摩尔体积
 (列出算式)。
(列出算式)。
 的沸点低于
的沸点低于  ,其原因是。
,其原因是。
 键
键 键为非极性共价键
键为非极性共价键 与
与 

 (填“>”或“<”)。
(填“>”或“<”)。
 )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。  的立体构型为。
的立体构型为。
 ,晶体密度为
,晶体密度为  ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 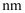 (列出计算式,
(列出计算式, 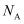 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 ;
; 分子
分子  离子(填“>”“<”或“=”),原因是。
离子(填“>”“<”或“=”),原因是。 是一种补铁剂。富马酸分子的结构模型如图所示:
是一种补铁剂。富马酸分子的结构模型如图所示:

 键与
键与  ,将
,将  转化为
转化为  ,反应过程如图所示:
,反应过程如图所示:


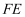 原子的配位数为;
原子的配位数为; 、
、  。阿伏加德罗常数的值为
。阿伏加德罗常数的值为  (列出计算式)。
(列出计算式)。 的还原性比
的还原性比 的强,原因是。
的强,原因是。


 原子的价电子排布式为,在元素周期表中位置为。
原子的价电子排布式为,在元素周期表中位置为。
 与
与 的配位数之比为;
的配位数之比为; ;晶胞中有d轨道参与杂化的金属离子是。
;晶胞中有d轨道参与杂化的金属离子是。
 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大
大 、
、 、
、 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。



