高考二轮复习知识点:微粒半径大小的比较2
高考二轮复习知识点:微粒半径大小的比较2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
汽车安全气囊中填充叠氮酸钠
 和硝酸钾 和硝酸钾  。汽车发生猛烈撞击时, 。汽车发生猛烈撞击时,  会迅速分解产生 会迅速分解产生  和Na,Na单质可与 和Na,Na单质可与  继续反应。完成下列填空: 继续反应。完成下列填空:
|
|
| 2. 综合题 | 详细信息 |
|
以硼砂、萤石和浓硫酸为原料可制取有机合成的原料三氟化硼。
反应原理为B2O3(S)+3CaF2(S)+3H2SO4(浓)⇌2BF3(g)+3CaSO4(S)+3H2O(l)。 请完成下列填空:
|
|
| 3. 综合题 | 详细信息 |
|
聚合氯化铝晶体([Al2(OH)nCl(6-n)•XH2O]m)是一种高效无机水处理剂。它的制备原理是调节AlCl3溶液的pH,通过促进其水解而结晶析出。
回答下列问题:
|
|
| 4. 综合题 | 详细信息 |
|
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
|
|
| 5. 综合题 | 详细信息 |
|
二氧化氯(ClO2)可以除去工业污水中的氰化物,反应的离子方程式为:2ClO2+2CN-=2CO2↑+N2↑+2Cl-
完成下列填空:
|
|
| 6. 综合题 | 详细信息 |
|
NaNO2
是一种白色易溶于水的固体,俗称工业盐,在漂白、电镀等方面应用广泛,完成下列填空:
|
|
| 7. 多选题 | 详细信息 |
|
Al、P、S、Cl是周期表中短周期主族元素。下列有关说法正确的是( )
A . 元素Al在周期表中位于第四周期ⅢA族
B . 元素P的简单气态氢化物的化学式为
 C . 原子半径
C . 原子半径  D . 最高价氧化物的水化物的酸性:
D . 最高价氧化物的水化物的酸性: 
|
|
| 8. 综合题 | 详细信息 |
|
碳酸锂是生产锂离子电池的重要原料。
|
|
| 9. 多选题 | 详细信息 |
|
W、X、Y、Z为原子序数依次减小的短周期主族元素,已知W与Y位于相邻主族,W、Y、Z的最外层电子数之和等于X的最外层电子数;由四种元素形成某化合物的结构如图。下列叙述正确的是( )
A . X与Z既可形成10电子分子也可形成18电子分子
B . 简单离子半径:
 C . Y的最高价氧化物对应水化物为强酸
D . 该化合物中各元素原子最外层均满足8电子稳定结构
C . Y的最高价氧化物对应水化物为强酸
D . 该化合物中各元素原子最外层均满足8电子稳定结构
|
|
| 10. 多选题 | 详细信息 |
|
近年来中国地质调查局在自然界中发现了新矿物——氟栾锂云母。该矿除含F和Li外,还含原子序数依次增大的W、X、Y、Z四种元素,已知它们的原子序数均不超过20,W、Y、Z的最外层电子数之和等于11,W的最低化合价为
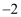 价,X在元素周期表中所处的族序数等于其周期序数。下列说法错误的是( ) 价,X在元素周期表中所处的族序数等于其周期序数。下列说法错误的是( )
A . X的金属性比Z的强
B . 原子半径:W>Y
C .
 中含离子键和共价键
D . X、Y的最高价氧化物对应的水化物均可与Z的最高价氧化物对应的水化物反应 中含离子键和共价键
D . X、Y的最高价氧化物对应的水化物均可与Z的最高价氧化物对应的水化物反应
|
|
高中化学 试卷推荐
- 陕西省榆林市第十二中学2020-2021学年高二下学期化学第二次月考试卷
- 广东省深圳市龙华区2020-2021学年高二上学期化学期末考试试卷
- 浙江省临海市西湖双语实验学校2020-2021学年高二下学期化学4月月考试卷
- 山西省柳林县2020-2021学年高一下学期化学期中考试试卷
- 吉林省松原市乾安县第七中学2020-2021学年高二上学期化学第一次月考试卷
- 天津市河东区2022届高三一模化学试题
- 2021高考真题汇编-有机化学
- 河南省开封市2021年高考化学一模试卷
- 吉林省洮南市第一中学2020-2021学年高二上学期化学期中考试试卷
- 山西省朔州市怀仁市2020-2021学年高二下学期期末考试化学试题
- 2021年高考化学真题试卷(河北卷)
- 浙江省温州环大罗山联盟2020-2021学年高一下学期化学期中考试试卷
最近更新
- 下列有关仪器用途说法不恰当的是 A.温度计代替玻璃棒用于搅拌 B.烧杯用于较多量试剂的反应容器 C.
- 2009年上半年,国内多个省市惊现以HD90、HB90等编号开头的百元假钞,对此,央行联手多个国家机关,迅速采取措施
- 甲、乙、丙、丁是由H+、Na+、Al3+、Ba2+、OH—、Cl—、HCO3—离子中的两种组成,可以发生如图转化,
- 在一堂物理活动课上,同学们正以“假如失去……”为主题展开讨论.下列是由四位同学提出的具有代表性的观点,你认为错误的是A.
- 求数列的前2n项和,
- 突触小泡膜上分布有一种SB蛋白,在突触小泡与突触前膜接触后它可以引发膜的融合进而使神经递质释放。此过程中
- 如图2所示,将质量为m=0.1kg的物体用两个完全一样的竖直弹簧固定在升降机内,当升降机以4m/s2的加速度加速向上运动
- 十一届全国人大代表亮相时有“三喜”,一喜工人农民代表多了,政府官员少了;二喜首次有了农民工代表;三喜各少数民族都有本民族
- 史载,上海轮船招商局每年结账后,均在《申报》和《北华捷报》等媒体上公布信息;开平煤矿章程规定,“进出煤铁银钱数目,每日有
- 表是某个水壶的铭牌,从铭牌中可知,在额定电压下通过电水壶的电流是 A(保留一位小数即可),1min内消耗的
- 读某区域图,一架飞机在当地时间0时30分从甲地起飞时,太阳正好在地平线上。朝正西飞行,到达乙地时再一次看见太阳在西北地平
- Leaders of the European Union say they will help Greece as i
- 为了得到较纯净的氮气,某同学采用燃烧法除去一瓶空气中的氧气,下列物质中最适宜选用的是 A.红磷 B.硫粉
- 按课文默写。(6分) (1)少壮不努力, 。
- 如下图,AB是半圆O的直径,C是AB延长线上一点,CD切半圆于D,CD=4,AB=3BC,则AC的长是 。
- 图1是某县参加2011年高考的学生身高条形统计图,从左到右的各条形图表示学生人数依次记为A1、A2、…A10(如A2表示
- 2003年5月21日,中国登山队把五星红旗又一次插上了世界的屋脊,登山运动员登顶之所以困难的主要原因是随着海拔的增高,大
- 染色体、DNA、基因的关系是 ( )A.人体细胞中染色体数目一定,每条染色体中有一个DNA分子,DNA
- 在等腰梯形ABCD中,且AD=,∠B=45°.直角三角板含角的顶点E在边BC上移动,一直角边始终经过点A,斜边与CD 交
- 按照图所示的电路图,将图12中各元件连接起来。(用笔画线表示导线,导线不许交叉)
 、
、  、
、  按照离子半径由大到小的顺序排列
按照离子半径由大到小的顺序排列  填离子符号
填离子符号 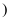 。
。
 的金属性强于Na,用一个事实说明。
的金属性强于Na,用一个事实说明。



 ,若标准状况下生成
,若标准状况下生成  氮气,转移的电子数目为
氮气,转移的电子数目为  。
。 晶体比
晶体比  晶体熔点低的原因。
晶体熔点低的原因。
 ;
; 。
。 、氨水和液溴制备
、氨水和液溴制备  。除生成
。除生成  ,。
,。
 ,放电时,负极为(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有
,放电时,负极为(填写化学式)。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有  气体(标准状况)产生时,该电池消耗锂的质量为。
气体(标准状况)产生时,该电池消耗锂的质量为。




