从巩固到提高 高考化学二轮微专题04 侯氏制碱法
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列说法正确的是( )
A . 步骤①是指蒸发结晶
B . 步骤⑤是先通CO2再通NH3
C . 在步骤②、③、④中,溴元素均被氧化
D . 制取NaHCO3的反应是利用其溶解度在常温下小于NaCl和NH4HCO3
|
|
| 2. 实验探究题 | 详细信息 |
|
化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO3 , 进一步处理得到产品Na2CO3和NH4Cl,实验流程如图:
回答下列问题:
|
|
| 3. 综合题 | 详细信息 |
|
对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝(
 )、钼( )、钼(  )、镍( )、镍(  )等元素的氧化物,一种回收利用工艺的部分流程如下: )等元素的氧化物,一种回收利用工艺的部分流程如下:
|
|
| 4. 单选题 | 详细信息 |
|
某科研小组利用有机胺(TBA)参与联合生产碳酸氢钠和二氯乙烷的工艺流程如图所示。
下列说法错误的是( )
A . 过程①中的TBA替代了侯德榜制碱法中的氨气
B . 过程②的反应为
 C . 理论上每产生
C . 理论上每产生  需要 需要  D . 流程中可循环利用的物质是TBA、CuCl
D . 流程中可循环利用的物质是TBA、CuCl
|
|
| 5. 单选题 | 详细信息 |
|
现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下:
有关说法错误的是( )
A . 反应Ⅰ原理为CO2 + NH3 + NaCl + H2O → NaHCO3↓ + NH4Cl
B . 向饱和NaCl溶液中先通入足量的CO2 , 再通入足量的NH3
C . 反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱
D . 往母液中通入氨气,加入细小的食盐颗粒并降温,可使氯化铵析出
|
|
| 6. 单选题 | 详细信息 |
|
侯德榜为我国的制碱工业做出了突出贡献。侯氏制碱法流程如下:
下列说法不正确的是( )
A . 精制饱和食盐水的操作依次为:取样、溶解、沉淀、过滤、蒸发浓缩、冷却结晶、过滤、洗涤、烘干
B . 该生产工艺制得纯碱的同时也得到了化学肥料
C . 吸氨操作的目的是把溶液中的碳酸氢盐转化为碳酸盐并增大铵根离子的浓度
D . 盐析环节中加入NaCl,对析出氯化铵起到了促进作用
|
|
| 7. 单选题 | 详细信息 |
|
侯德榜是我国近代化学工业的奠基人之一,他将氨碱法和合成氨工艺联合起来,发明了“联合制碱法”。氨碱法中涉及的反应有:
反应Ⅰ: 反应Ⅱ: 下列制取少量
A . 制取
 B . 除去
B . 除去 中 中 C . 制取
C . 制取 D . 制取
D . 制取
|
|
| 8. 单选题 | 详细信息 |
|
“侯氏制碱法”是我国化学家侯德榜为世界制纯碱工业做出的突出贡献。某实验小组模拟制纯碱的工艺流程及实验装置(部分夹持装置省略)如图所示,下列叙述正确的是( )
A . 装置①中的试管中应盛放氯化铵固体
B . 装置②的球形干燥管中应盛放碱石灰
C . 装置②和装置③之间应该增加盛有饱和碳酸钠溶液的洗气瓶
D . 装置①可以用装置③代替,但不可用装置④代替
|
|
| 9. 实验探究题 | 详细信息 |
|
化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟侯氏制碱法制备NaHCO3 , 进一步 得到产品Na2CO3和NH4Cl两种产品,并测定碳酸钠中碳酸氢钠的含量。过程如下:
|
|
| 10. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
|
纯碱是重要的化工原料。我国科学家侯德榜发明的“侯氏制碱法”打破了西方对我国的技术封锁。某实验小组同学利用下图装置,模拟“侯氏制碱法”的部分流程。
已知:NaCl、NH4HCO3、NaHCO3、NH4Cl四种盐在不同温度下的溶解度如下表所示:
回答下列问题:
|
|||||||||||||||||||||||||||||||||||||||||
- 2023年高考化学模拟卷(全国乙卷)
- 广西北海市2021-2022学年高一下学期期末检测化学试题
- 河南省林州市2021-2022学年高一下学期期末考试化学试题
- 河南省平顶山市2021-2022学年高一下学期期末调研化学试题
- 湖南省郴州市2021-2022学年高一下学期期末考试化学试题
- 湖南省岳阳市临湘市2021-2022学年高一下学期期末教学质量检测化学试题
- 江苏省南通市如东县、海安市2021-2022学年高一下学期期末考试化学试题
- 江苏省宿迁市2021-2022学年高一下学期期末考试化学试题
- 江苏省盐城市2021-2022学年高一下学期期末考试化学试题
- 江西省赣州市2021-2022学年高一下学期期末考试化学试题
- 江西省景德镇市2021-2022学年高一下学期期末质量检测化学试题
- 江西省南昌市2021-2022学年高一下学期期末调研检测化学试题
- 对任意实数,有, 则的值为 .
- (08年海拉尔二中阶段考试五理) .
- Do you forget to turnoff the lights and heaters when you go
- 豌豆植株的细胞中,A.C.T.U四种碱基参与合成的核苷酸种类有( ) A、3种 B、4种
- 如图是甲、乙两射击运动员的10次射击训练成绩(环数)的折线统计图,观察图形,甲、乙这10次射击成绩的方差,之间的大小关系
- ,芳草萋萋鹦鹉洲。(崔颢 《黄鹤楼 》)
- 【2013年·内蒙古省包头市】 【试题】6.按要求完成下面的对联题。(任选一题3分) (1)上联:为人要勤,勤能
- (坐标系与参数方程选做题) 若直线(t为参数)与直线垂直,则常数k=__▲__.
- 紫杉醇是一种新型抗癌药,其分子式为C47H51NO14,它是由如下的A酸与B醇生成的一种酯。 B.R-OH(R是一个含
- 2010年3月,全国政协第十一届三次会议和全国人大第十一届三次会议在京举行。回答下题。 在今年的全国政协全体会议上,梁季
- 已知圆锥的母线长是5cm,侧面积是15πcm2,则这个圆锥底面圆的半径是 cm.
- 常见金属R与硝酸银溶液反应的化学方程式为R+3AgNO3==3Ag+R(NO3)3,有关该反应的说法正确的是 A.反应后
- 根据短文内容,从短文后的选项中选出能填入空白处的最佳选项,选项中有两项为多余选项。 Today, we willtalk
- 小华想知道学校旗杆的高度,他发现旗杆上的绳子垂到地面还多了1 m,当他把绳子的下端拉开距旗杆底部5 m后,发现绳子的末端
- 设等差数列的前项和为,若,则 A7 B. 6 C. 5 D. 4
- --When shall we meet again next week? ---_____ day ispossibl
- 20.仿照下面的例句,另选两个话题,各写一个有哲理的句子,句式与示例相同。(6分) 真正的善良,不是眼泪,而是伸过去的一
- 2009年是新世纪以来我国经济发展最为困难的一年,而文化产业逆势而上,呈现着“繁花似锦”的繁荣景象。 某校高三(1)班同
- 若是偶函数,且当的解集是 A.(-1,0)
- 函数的定义域是() A.[2,3) B.(3,+∞) C.[2,3)∩(3,+∞


 B.
B.  C.
C.  D.
D.  E.
E. 

 已知:25℃时,
已知:25℃时,  的
的  ,
,  ;
;  ;
;  ;该工艺中,
;该工艺中,  时,溶液中
时,溶液中  的形态存在。
的形态存在。 生成,其中
生成,其中 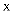 为。
为。
 为7.0。
为7.0。  的离子方程式为。
的离子方程式为。 也会沉淀。为避免
也会沉淀。为避免  (列出算式)时,应停止加入
(列出算式)时,应停止加入  溶液。
溶液。 和
和  ,
,  ,可析出
,可析出  (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止
(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止  刻蚀液与下层
刻蚀液与下层  (砷化镓)反应。
(砷化镓)反应。 
 和
和  和
和 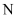 同族。在
同族。在 




 的实验原理和装置能达到实验目的的是( )
的实验原理和装置能达到实验目的的是( )






