湖北省部分普通高中联盟2022-2023学年高二下学期期中联考化学试题
湖北省部分普通高中联盟2022-2023学年高二下学期期中联考化学试题
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
NA为阿伏加德罗常数的值。下列说法错误的是( )
A . 23gCH3CH2OH中sp3杂化的原子数为NA
B . 0.5molXeF4中氙的价层电子对数为3NA
C . 1mol[Cu(H2O)4]2+中配位键的个数为4NA
D . 标准状况下,11.2LCO和H2的混合气体中分子数为0.5NA
|
|
| 2. 单选题 | 详细信息 |
|
某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
A . 该晶胞的体积为a3×10-36cm-3
B . K和Sb原子数之比为3∶1
C . 与Sb最邻近的K原子数为4
D . K和Sb之间的最短距离为
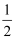 apm apm
|
|
| 3. 单选题 | 详细信息 |
|
某立方卤化物可用于制作光电材料,其晶胞结构如图所示。下列说法错误的是( )
A .
 的配位数为6
B . 与 的配位数为6
B . 与 距离最近的是 距离最近的是 C . 该物质的化学式为
C . 该物质的化学式为 D . 若
D . 若 换为 换为 , 则晶胞棱长将改变 , 则晶胞棱长将改变
|
|
| 4. 单选题 | 详细信息 |
氢氟酸是芯片加工的重要试剂,可通过反应
|
|
| 5. 单选题 | 详细信息 |
有反应P4+16H2O+10CuSO4=10Cu+4H3PO4+10H2SO4。下列说法正确的是( )
A . 第一电离能大小:I1(P)<I1(S)
B . 电负性大小:χ(O)< χ(S)
C . 离子半径大小:r(P3-)>r(S2-)
D . 酸性强弱:H3PO4>H2SO4
|
|
| 6. 单选题 | 详细信息 |
下列物质的分子中既有σ键,又有π键的是( )①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2
A . ①②③
B . ③⑤⑥
C . ①③⑥
D . ③④⑤⑥
|
|
| 7. 单选题 | 详细信息 |
下列分子或离子的中心原子为
|
|
| 8. 单选题 | 详细信息 |
下列说法正确的是( )
A . CO2分子中σ键和π键的数目之比为
 B . SO2和CS2均为V形分子
C . NCl3分子中的键角为
B . SO2和CS2均为V形分子
C . NCl3分子中的键角为 D . SiF4和
D . SiF4和 的中心原子均为sp3杂化 的中心原子均为sp3杂化
|
|
| 9. 单选题 | 详细信息 |
|
|
| 10. 单选题 | 详细信息 |
下列关于氢键的说法正确的是( )
A . 由于氢键的作用,
 、 、 、 、 的沸点反常,且沸点高低顺序为 的沸点反常,且沸点高低顺序为 B . 氢键只能存在于分子间,不能存在于分子内
C . 水在1000℃以上才会部分分解是因为水中含有大量的氢键
D . 邻羟基苯甲醛的沸点低于对羟基苯甲醛的原因是前者不存在氢键
B . 氢键只能存在于分子间,不能存在于分子内
C . 水在1000℃以上才会部分分解是因为水中含有大量的氢键
D . 邻羟基苯甲醛的沸点低于对羟基苯甲醛的原因是前者不存在氢键
|
|
高中化学 试卷推荐
- 江西省宜春市2020年高考化学5月模拟试卷
- 浙江省杭州市八校联盟2018-2019学年高一上学期化学期中考试试卷
- 广东省深圳市罗湖区2017-2018学年高二上学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题15 元素周期表和元素周期律
- 人教版化学高二选修5第四章第二节糖类同步练习
- 天津市武清区2018-2019学年高一上学期化学期中考试试卷
- 安徽省合肥市2019-2020学年高二上学期期末考试化学试题
- 2015-2016学年北京市海淀区高三上学期期末化学试卷
- 安徽省皖西高中教育联盟2018-2019学年高三上学期理综-化学期末考试试卷
- 高中化学人教版(2019)必修第二册 第五章第二节 氮及其化合物
- 2015-2016学年福建省福州市福清市元洪中学高一上学期期中化学试卷
- 云南省昭通市昭阳区2019-2020学年高一上学期化学期中考试试卷
最近更新
- 一辆汽车以恒定的功率75kW在一条平直的公路上加速行驶,在20s内前进了500m,求牵引力在这段时间内所做的功.
- 将5.6g铁粉加到500mL 1mol/L稀硝酸中,充分反应后, (1)求所得溶液中NO3-的浓度是多少?(不考虑液体体
- 人们对房地产的开发,要遵循一定的原则,下列说法属于高走原则的是() A.选择城市中地势高的地段 B.选择城市的上风口
- 阅读下面两篇文章,完成小题。(12分)【甲文】①我们是一列树,立在城市的飞尘里。②许多朋友都说我们是不该站在这里的,这一
- 下列能预测一个国家或地区未来人口数量动态变化的是:A.人口密度 B.年龄组成 C.性别比例 D.出生率和死亡率
- 42、(5分)下图为光合作用过程示意图。请据图回答。
- 根据要求,用尺规作图: 在下列图形中,补充作图: (1)在AD的右侧作
- 下列叙述错误的是 A.我国夏季也有冷锋活动 B.我国的一些灾害性天气大多与锋面有关 C.我国夏季午后的雷阵雨,多是由冷锋
- 现有六种物质:①干冰②氢气③氯酸钾④盐酸⑤二氧化锰⑥石灰石. (1)其中属于氧化物的是 受热后能生成氧气的是 (填序
- 若甲、乙、丙三人的命中率为0.8,0.6,0.7,现三人各射击一次,则三人中恰有一个命中的概率为( )A.0.04
- 逻辑推理是一种重要的化学思维方法,以下推理合理的是() A.氧气可以供给人类呼吸,所以空气中氧气浓度越高越好 B.蜡烛燃
- 化学反应处于平衡状态时,下列说法正确的是()。 A.反应不再进行 B.反应物浓
- 《共同纲领》第二十五条:“对于国民政府与外国所订立的各项条款和协定,中华人民共和国中央人民政府加以审查,按其内容分别予以
- —What do you think about dress in the shop window? —Oh
- 已知sinA=0.501 8,求角A.(利用计算器 )
- 判断题:判断下列各题的正确与错误,请在答题卡上相应的方框内填涂,正确的涂A,错误的涂B(10小题,每题2分,共20分)。
- 选举权和被选举权是公民的基本政治权利。某校高三(8)班同学开展了以“如何保障公民的基本政治权利”为主题的探究活动。让我们
- 总书记指出:在改造客观世界的进程中,我们的主观世界可以得到磨炼和提高。我们的主观世界不断得到改造,就可以推动我们更好地改
- 从含有少量碘化钾的水溶液中提取单质碘的实验方法是() A.通入适量Cl2充分搅拌,加入酒精进行萃取 B.通入适量Cl2充
- 计算(m+3n)2-(3m+n)2的结果是( ) A.8(m-n)2 B.8(m+n)2 C.8n2+8m2 D.8


 制取。下列说法正确的是( )
制取。下列说法正确的是( )
 原子的电子排布式为
原子的电子排布式为
 的电子式为
的电子式为

 杂化,且杂化轨道容纳1对孤电子对的是( )
杂化,且杂化轨道容纳1对孤电子对的是( )
 、
、 、
、 、
、 、
、 、
、
 、
、
 为阿伏加德罗常数的值。下列说法错误的是( )
为阿伏加德罗常数的值。下列说法错误的是( )
 分子中,S的价层电子对数是
分子中,S的价层电子对数是
 中含有氢键的数目为
中含有氢键的数目为
 分子中含有的共价键数目为
分子中含有的共价键数目为
 晶体中,阴阳离子数目之和是
晶体中,阴阳离子数目之和是


