陕西省宝鸡市2022届高三第三次模拟检测理科综合化学试题
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 淀粉、油脂和蛋白质均能发生水解反应
B . 合成纤维和光导纤维都是新型无机非金属材料
C . 煤的干馏和石油的分馏均属于物理变化。
D . 常温下,铁制的容器不能盛装浓硝酸
|
|
| 2. 单选题 | 详细信息 |
|
我国科学家首次在实验室中实现从二氧化碳到淀粉的全合成,合成路径如下图所示。下列表示相关微粒的化学用语正确的是( )
A . 淀粉的分子式:
 B . DHA的最简式:
B . DHA的最简式: C . FADH的电子式:
C . FADH的电子式: 的比例模型: 的比例模型: |
|
| 3. 单选题 | 详细信息 |
|
NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 常温下,pH=13的NaOH溶液中含有OH-的数目为0.1NA
B . 在1L0.1mol·L-1CH3COONa溶液中,阴离子的总数等于0.1NA
C . 标准状况下,2.24LCH2Cl2含有的C-Cl键数目为0.2NA
D . 20gD2O中含有的质子中子和电子的数目均为10NA
|
|
| 4. 单选题 | 详细信息 |
|
我国科学家研究了不同含金化合物催化乙烯加氢[C2H4(g)+H2(g)=C2H6(g) △H=akJ·mol-1]的反应历程如下图所示,下列说法正确的是( )
A . 1molC2H4(g)与1molH2(g)具有的能量之和小于1molC2H6(g)的能量
B . 过渡态物质的稳定性:过渡态1>过渡态2
C . 该反应的焓变:ΔH=-129.6kJ·mol-1
D . 相应的活化能:催化剂AuF<催化剂AuPF

|
|
| 5. 单选题 | 详细信息 |
|
某100mL溶液可能含有K+、
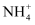 、Al3+、 、Al3+、 、 、 、Cl-中的若干种,取该溶液进行连续实验,实验过程如下图所示(所加试剂均过量,气体全部逸出):下列说法错误的是( ) 、Cl-中的若干种,取该溶液进行连续实验,实验过程如下图所示(所加试剂均过量,气体全部逸出):下列说法错误的是( )
A . 原溶液中一定含有
 、 、 , 无Al3+
B . 原溶液中一定存在K+ , 可能存在Cl-
C . 是否存在K+只有通过焰色反应才能确定
D . 若原溶液中不存在Cl- , 则c(K+)=0.1mol·L-1 , 无Al3+
B . 原溶液中一定存在K+ , 可能存在Cl-
C . 是否存在K+只有通过焰色反应才能确定
D . 若原溶液中不存在Cl- , 则c(K+)=0.1mol·L-1
|
|
| 6. 单选题 | 详细信息 |
|
用如图甲所示装置模拟对含高浓度Cl-的工业废水进行脱氮,该溶液中ClO-的浓度随时间变化的关系如图乙所示。一段时间后溶液中所有氮原子均转化为N2被脱去。下列说法正确的是( )
A . b电极应接外电源的正极
B . 电解过程中,a极附近溶液的pH降低
C . 理论上溶液中的
 先被脱尽
D . 开始时ClO-浓度增长较慢的原因一定是被Cl-还原 先被脱尽
D . 开始时ClO-浓度增长较慢的原因一定是被Cl-还原
|
|
| 7. 单选题 | 详细信息 |
|
25℃时,向25mL0.1mol·L-1邻苯二甲酸(H2A)溶液中加入KOH固体,混合溶液的pH随-lgc(HA-)以及-lgc(A2-)的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发)。下列有关叙述错误的是( )
A . 邻苯二甲酸的Ka1约为1.0×10-3
B . b点有关微粒浓度大小关系为(HA-)>c(A2-)>c(H2A)
C . 从b点到e点,水电离产生的c(H+)先增大后减小
D . c点c(K+)>3c(A2-)
|
|
| 8. 综合题 | 详细信息 | ||||||||||||||||||
|
硫酸锰(MnSO4·H2O)是一种粉色晶体,易溶于水,不溶于乙醇,是重要的微量元素肥料之一、工业上由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Si等元素的氧化物)制备硫酸锰的工艺如下图所示。回答下列问题:
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
|
|||||||||||||||||||
| 9. 实验探究题 | 详细信息 | ||||||||||||||||||||
|
实验室以苯甲酸和乙醇为原料制备苯甲酸乙酯,实验装置如图(加热及夹持装置已省略)。
反应原理:
实验步骤如下: 步骤1:在三颈烧瓶中加入12.20g苯甲酸、20mL环己烷、5mL浓硫酸、沸石,并通过分液漏斗加入60mL(过量)乙醇,控制温度在65~70℃加热回流2h。反应时“环己烷-乙醇-水”会形成共沸物(沸点62.6℃)蒸馏出来,再利用分水器不断分离除去水,回流环己烷和乙醇。 步骤2:反应一段时间,打开旋塞放出分水器中液体,关闭旋塞,继续加热维持反应。 步骤3:将三颈烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。 步骤4:用分液漏斗分离出有机层,水层用25mL乙醚萃取分液,然后合并至有机层。加入氯化钙,对粗产物进行蒸馏,低温蒸出乙醚后,继续升温,接收210~213℃的馏分,得到产品10.00mL。 请回答下列问题:
|
|||||||||||||||||||||
| 10. 综合题 | 详细信息 |
|
汽车尾气中含有氮氧化合物和CO,减少它们在大气中的排放是环境保护的重要内容之一、
|
|
- 浙江省绍兴市2022届高三选考科目适应性考试(二模)化学试题
- 浙江省温州市环大罗山联盟2021-2022学年高一下学期期中联考化学试题
- 广东省潮州市2020-2021学年高二上学期化学期末考试试卷
- 天津市东丽区2020-2021学年高一下学期化学期末考试试卷
- 浙江省杭州市八校联盟2020-2021学年高一下学期化学期中考试试卷
- 安徽省马鞍山市2022届高三下学期第三次教学质量监测(三模) 理综化学试题
- 山东省菏泽市2022届高三二模考试化学试题
- 辽宁省名校联盟2021-2022学年高三12月联合考试化学试题
- 上海市上交大附高2021-2022学年高二上学期化学9月月考试卷
- 江苏省苏州市姑苏区2020-2021学年高一上学期化学期中考试试卷
- 山东省滨州市无棣县2020-2021学年高一下学期化学期中考试试卷
- 河南省驻马店市环际大联考2021-2022学年高二下学期期中考试化学试题
- 磨砺意志 完善自我2011年10月22日中国政府网:21日至22日,温家宝总理在广西南宁考察时指出: “每个大学生都要
- 下列物质放在敞口容器中一段时间后,质量明显减少的是 A.浓硫酸 B.浓盐酸 C.
- 某烷烃和烯烃混合气体的密度是1.07 g·L-1(标准状况),该烷烃和烯烃的体积比为4∶1,则这两种烃是( ) A
- 直线与抛物线都过点,且, (1)求抛物线顶点Q的坐标(用含a的式子表示); (2)试说明抛物线与直线有两个交点; (3)
- 收入的增长,一个是绝对增长,取决于微观领域内企业内部的机制,国家可以考虑为企业员工工资增长制定基本的导向,建立劳资双方
- (1)_________________________,我只躲到你的怀里。 (2)海日生残夜,
- 当____________时,分式有意义;
- 下列各句中,没有语病、句意明确的一句是( ) A.加拿大的一些矿井正在使用一个通过雷达进行勘测的裂纹识别系统,以检查
- 以直角坐标系的原点O为极点,x轴的正半轴为极轴建立极坐标系,已知点P的直角坐标为(1,-5),点M的极坐标为(4,).若
- 在区间上不是增函数的是( ) A. B. C. D.
- 【文段四】这里除了光彩,还有淡淡的芳香,香气似乎也是浅紫色的,梦幻一般轻轻地笼罩着我。忽然记起十多年前家门外也曾有过一大
- . ---__________ that he managed to get the information? -
- Honesty is ________ he is born with. A. that B. which
- 阅读下面的文言文,完成文后各题。 粱鼎,字凝正,益州华阳人。太平兴国八年进士甲科,解褐大理评事、知秭归县,再迁著作佐郎。
- 人体具有______块骨。 A. 600多 B. 206 C. 208 D. 602
- Sit down, Emma. You will only make yourself more tired, ___
- 2010年3月,在十一届全国人大三次会议上,中央确定国内生产总值预期增长目标为8%,并强调“好”字当头,引导各方面把工作
- 基础写作(共1小题,满分15分) 请根据以下的情景说明,使用5个规范的句子描述全部所给的内容。【情景说明】 你们学校学生
- 关于精子变形的叙述错误的是( ) A.细胞核变为精子头部的主要部分 B.高尔基体发育为头部的顶体 C.中心体演变为精
- 哺乳动物卵细胞形成的场所是( ) A.卵巢 B.输卵管 C.子宫 D.睾丸








 +H2O
+H2O


 的比值。(选填“增大”“不变”或“减小”)。
的比值。(选填“增大”“不变”或“减小”)。



