从巩固到提高 高考化学二轮微专题22 pH及相关计算
从巩固到提高 高考化学二轮微专题22 pH及相关计算
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 | |||||||||||||||
|
磁选后的炼铁高钛炉渣,主要成分有
 、 、  、 、  、MgO、CaO以及少量的 、MgO、CaO以及少量的  ,为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。 ,为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺下,有关金属离子开始沉淀和沉淀完全的pH见下表:
回答下列问题:
|
||||||||||||||||
| 2. 单选题 | 详细信息 |
|
下列说法错误的是( )
A . 升高HCl稀溶液温度,溶液中c(H+)不变
B . 常温,向醋酸钠溶液中滴加少量醋酸使其pH=7,则混合液中:c(Na+)=c(CH3COO-)
C . 向AgCl、AgBr的饱和溶液中加入少量AgNO3固体,溶液中氯离子浓度和溴离子浓度比不变
D . 25℃时,将0.1mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11.0
|
|
| 3. 综合题 | 详细信息 |
|
绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr—Fe—Al—Mg的深度利用和Na+内循环。工艺流程如图:
回答下列问题:
|
|
| 4. 单选题 | 详细信息 | ||||||||||||||||||||
|
为达到下列实验目的,对应的实验方法以及相关解释均正确的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 5. 单选题 | 详细信息 |
|
某同学拟用
 计测定溶液 计测定溶液  以探究某酸HR是否为弱电解质。下列说法正确的是( ) 以探究某酸HR是否为弱电解质。下列说法正确的是( )
A . 25℃时,若测得
 溶液 溶液  ,则HR是弱酸
B . 25℃时,若测得 ,则HR是弱酸
B . 25℃时,若测得  溶液 溶液  且 且  ,则HR是弱酸
C . 25℃时,若测得HR溶液 ,则HR是弱酸
C . 25℃时,若测得HR溶液  ,取该溶液 ,取该溶液  ,加蒸馏水稀释至 ,加蒸馏水稀释至  ,测得 ,测得  ,则HR是弱酸
D . 25℃时,若测得NaR溶液 ,则HR是弱酸
D . 25℃时,若测得NaR溶液  ,取该溶液 ,取该溶液  ,升温至50℃,测得 ,升温至50℃,测得  , ,  ,则HR是弱酸 ,则HR是弱酸
|
|
| 6. 多选题 | 详细信息 |
|
常温下,向
 某一元碱 某一元碱  溶液中逐滴加入 溶液中逐滴加入  的 的  溶液,溶液中 溶液,溶液中  中和率的变化如图所示。 中和率的变化如图所示。  为 为  的电离常数, 的电离常数,  下列说法正确的是( ) 下列说法正确的是( )
A . 溶液中水的电离程度从a点到d点逐渐增大
B . a点时,
 C . b点时,
C . b点时,  D . c点时,
D . c点时, 
|
|
| 7. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 体系的内能与温度等有关,只要温度不变,体系的内能不变
B . 反应
 能自发进行,它的 能自发进行,它的  , ,  C . 室温下,pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合后,所得溶液的pH大于7
D . 水与丙酮能完全互溶的原因是两种分子间能形成氢键
C . 室温下,pH=4的醋酸溶液和pH=10的氢氧化钠溶液等体积混合后,所得溶液的pH大于7
D . 水与丙酮能完全互溶的原因是两种分子间能形成氢键
|
|
| 8. 多选题 | 详细信息 |
|
化学上把由浓度相对较大的弱酸(弱碱)及其相应的盐组成的溶液,外加少量酸、碱而pH基本不变,称为缓冲溶液。弱酸及其盐组成的缓冲溶液的
 。现有25℃时,浓度均为0.10mol·L-1的CH3COOH和CH3COONa的缓冲溶液 。现有25℃时,浓度均为0.10mol·L-1的CH3COOH和CH3COONa的缓冲溶液  。下列有关说法正确的是( ) 。下列有关说法正确的是( )
A . 将该缓冲溶液加水稀释100倍,溶液的pH基本不变
B . 该缓冲溶液的pH=4.76
C . 该缓冲溶液中离子浓度大小顺序是:
 D . 人体血液存在H2CO3(CO2)和NaHCO3的缓冲溶液,可除掉人体代谢产生的酸、碱,保持pH基本不变
D . 人体血液存在H2CO3(CO2)和NaHCO3的缓冲溶液,可除掉人体代谢产生的酸、碱,保持pH基本不变
|
|
| 9. 综合题 | 详细信息 |
|
氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂等。一种用火法炼铜过程产生的铜转炉烟尘(除含铋的化合物之外,还有CuSO4、ZnSO4、CuS、Fe2O3、PbSO4及As2O3)制备高纯氯氧化铋的工艺流程如下:
已知:①BiOCl难溶于水; ②“浸铋”所得浸取液中含BiCl3、AsCl3等物质。 回答下列问题:
|
|
| 10. 综合题 | 详细信息 |
|
Co3O4在工业上有重要应用。利用原钴矿(主要含有Co2O3 , 还含有少量Cr2O3、NiO等杂质)制备Co3O4的工艺流程如下:
已知:①在含一定量Cl-的溶液中:Co2++4Cl-=CoCl ②CoCl ③Ksp[Co(OH)2]=1.0×10-15
|
|
高中化学 试卷推荐
- 高中化学苏教版(2019)必修第一册 专题1第一单元 物质及其反应的分类
- 2023年高考化学模拟卷(全国乙卷)
- 广西北海市2021-2022学年高一下学期期末检测化学试题
- 河南省林州市2021-2022学年高一下学期期末考试化学试题
- 河南省平顶山市2021-2022学年高一下学期期末调研化学试题
- 湖南省郴州市2021-2022学年高一下学期期末考试化学试题
- 湖南省岳阳市临湘市2021-2022学年高一下学期期末教学质量检测化学试题
- 江苏省南通市如东县、海安市2021-2022学年高一下学期期末考试化学试题
- 江苏省宿迁市2021-2022学年高一下学期期末考试化学试题
- 江苏省盐城市2021-2022学年高一下学期期末考试化学试题
- 江西省赣州市2021-2022学年高一下学期期末考试化学试题
- 江西省景德镇市2021-2022学年高一下学期期末质量检测化学试题
最近更新
- ......
- 在下图四个情形中,属于利用热传递改变物体内能的是
- 枯叶蝶生活在植物的枝叶之间,就像是一片枯叶,天敌很难发现它。这种适应性的形成是( ) A.自然选择的结果
- 【甲】 蜀相 杜甫 丞相祠堂何处寻,锦官城外柏森森。 映阶碧草自春色,隔叶黄鹂空好音。 三顾频烦天下计,两朝开济老臣心。
- 质量相同的水和食用油吸收相同的热量,的温度变化较大;质量相同的水和食用油升高相同的温度,吸收的热量较多.
- 不管以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳的量不变的是 A.乙烯(C2H4)和苯(C6H6)
- 阅读下面这首宋诗,然后回答问题。 绝句 石柔① 来时万缕弄轻黄,去日飞球②满路旁。 我比杨花更飘荡,杨花只是一春
- 关于某无色溶液所含离子的确定,下列判断正确的是 A.若加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl
- 从1,2,3,4,5,6六个数字中,选出一个偶数和两个奇数,组成一个没有重复数字的三位数,这样的三位数共有A.9个
- (·湖南省衡阳八中高三上第一次月考) 25._____ occurred to me that the murder h
- 如图,在△ABC中,∠BAC=90°,AB=AC,点D为边AC的中点,DE⊥BC于点E,连接BD,则tan∠DBC的值为
- 某同学分离纯化了甲、乙两种噬菌体的蛋白质和DNA,重新组合为“杂合”噬菌体,然后分别感染大肠杆菌,并对子代噬菌体的表现型
- 有____首赞美某种气体的诗,其中的几句是:“她营造了云雾缭绕的仙景;她驱散了炎炎夏日的暑气;她奋不顾身扑向烈火;她带给
- 捷克斯洛伐克社会民主工党向布尔什维克党祝贺,“你们摧毁了俄国资本主义和俄国资产阶级富丽堂皇的大厦。你们首先向全世界发出‘
- 棉花的纤维有白色的,也有紫色的;植株有抗虫的,也有不抗虫的。为鉴别有关性状的显隐性关系,有人做了以下两组杂交试验,结果如
- 函数的自变量的取值范围是 .
- 已知果蝇中,灰身与黑身是一对相对性状(用B-b表示);直毛与分叉毛是一对相对性状(用F-f表示),两对基因位于两对同源染
- 已知H2O2酶广泛存在于动物、植物组织中,它能催化H2O2的分解反应。锈铁钉上的Fe3+也能催化H2O2的分解。现有新鲜
- (05年江西卷)阅读下列文字,按要求作文“脸”是大家熟悉的字眼,其内涵是丰富的。平时我们常会想起与“脸”有关的情境,思考
- 复数的值是() (A)0 (B)1 (C) (D)





 的化学方程式。
的化学方程式。

 水解析出
水解析出  沉淀,该反应的离子方程式是。
沉淀,该反应的离子方程式是。

 Al(OH)
Al(OH)  :K=100.63 , Kw=10-14 , Ksp[Al(OH)3]=10-33)
:K=100.63 , Kw=10-14 , Ksp[Al(OH)3]=10-33)

 的体积
的体积
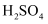 会与锌粒反应生成
会与锌粒反应生成  催化裂解
催化裂解
 裂解为分子较小的烷烃和烯烃,可以冷凝收集
裂解为分子较小的烷烃和烯烃,可以冷凝收集 溶液制备
溶液制备 


 ,和H2O2 , 并调节pH,生成FeAsO4沉淀,发生反应的离子方程式是。欲使溶液中
,和H2O2 , 并调节pH,生成FeAsO4沉淀,发生反应的离子方程式是。欲使溶液中  且不产生
且不产生  ,沉淀,应控制pH的范围为。(已知:
,沉淀,应控制pH的范围为。(已知:  ;
;  、
、  ,
,  ,计算结果保留2位小数)
,计算结果保留2位小数)
 ,该反应的发生使得电池的储能(填“增大”“减小”或“不变”)。
,该反应的发生使得电池的储能(填“增大”“减小”或“不变”)。