【备考2024年】从巩固到提高 高考化学微专题05 卤族与氮族及其应用
【备考2024年】从巩固到提高 高考化学微专题05 卤族与氮族及其应用
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
部分含氯物质的分类与相应化合价关系如图所示,下列说法错误的是( )
A . a的浓溶液与KMnO4反应制得b
B . b溶于水制得液氯
C . c可用于自来水消毒
D . 存在a→b→>d→a的转化关系
|
|
| 2. 单选题 | 详细信息 |
|
I2的一种制备方法如图所示:
下列说法正确的是:( )
A . “富集”时发生的离子方程式为
 B . 转化反应为
B . 转化反应为 , 说明 , 说明 的还原性大于 的还原性大于 C . 通入过量Cl2 , 氧化产物只有一种
D . 制备的I2可直接用于加碘盐
C . 通入过量Cl2 , 氧化产物只有一种
D . 制备的I2可直接用于加碘盐
|
|
| 3. 单选题 | 详细信息 | ||||||||||||
|
氯气及其化合物在生产、生活中应用广泛。实验室常用浓盐酸与
 共热[或用 共热[或用 (s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是 ( ) (s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是 ( )
A . A
B . B
C . C
D . D
|
|||||||||||||
| 4. 综合题 | 详细信息 |
|
卤族元素在自然界中主要以卤化物形式存在,完成下列填空:
|
|
| 5. 单选题 | 详细信息 |
|
三氟化氯(ClF3)可应用于航天工业,是一种很强的氧化剂和氟化剂,它能与大多数有机和无机材料甚至塑料反应,可以使许多材料不接触火源就燃烧。下列分析错误的是( )
A . 可以代替H2O2充当火箭推进剂中的氧化剂
B . 能与一些金属反应生成氯化物和氟化物
C . 三氟化氯可用于清洁化学气相沉积的反应舱附着的半导体物质
D . ClF3与水按照1:2反应生成两种强酸
|
|
| 6. 综合题 | 详细信息 |
|
养殖业废水中含有一定量的氨氮(以
 形式存在)污染物,通过沉淀法或折点氯化法处理后可使水中氨氮达到国家规定的排放标准。 形式存在)污染物,通过沉淀法或折点氯化法处理后可使水中氨氮达到国家规定的排放标准。
|
|
| 7. 单选题 | 详细信息 |
|
绿水青山是
 总书记构建美丽中国的伟大构想,某工厂拟综合处理含 总书记构建美丽中国的伟大构想,某工厂拟综合处理含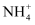 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程: 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如图流程:
下列说法错误的是( )
A . 固体1中主要含有CaCO3、CaSO3、Ca(OH)2
B . X可以是空气,但不能过量
C . 捕获剂所捕获的气体主要是CO、N2
D . 处理含
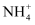 废水时,发生的反应为: 废水时,发生的反应为: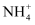 + + =N2↑+2H2O =N2↑+2H2O
|
|
| 8. 单选题 | 详细信息 |
|
部分含氮物质的分类与相应氮元素化合价关系如图所示。下列说法正确的是( )
A . a可使紫色石蕊试液变红
B . b的分子含有极性共价键,不含非极性共价键
C . 一定条件下,c、d、e之间存在转化关系:
 D . 实验室用e的浓溶液与
D . 实验室用e的浓溶液与 反应制备d,用排水法收集 反应制备d,用排水法收集
|
|
| 9. 实验探究题 | 详细信息 |
|
碘单质对动植物的生命极其重要,还可用于医药、照相、染料和系统监测等。某学习小组在实验室中从海藻和油井盐水生产母液中提取碘单质的主要步骤如图1所示:
已知:本实验条件下,氧化性:Cl2>IO 回答下列问题:
|
|
| 10. 单选题 | 详细信息 |
|
下列对氯及其化合物的说法正确的是( )
A . 因氯化铝溶液能导电,所以氯化铝是离子化合物
B . 用pH试纸测得氯水的pH=4
C . 随着氯元素化合价升高,氯的含氧酸酸性逐渐减弱
D . 次氯酸不如次氯酸盐稳定,故用次氯酸盐作为漂白剂的主要成分
|
|
高中化学 试卷推荐
- 山东省烟台市2021年高考化学二模试卷
- 湖北省八市2021年高考化学3月模拟试卷
- 福建省南平市浦城县2020-2021学年高二下学期化学期中考试试卷
- 湖北省武汉市武昌区2020-2021学年高二下学期化学期末考试试卷
- 河北省邯郸市2021年高考化学一模试卷
- 天津市滨海新区大港太平村中学2020-2021学年高二上学期化学期中考试试卷
- 黑龙江省齐齐哈尔市三立高级中学2021-2022学年高三上学期化学第一次月考试卷
- 2021高考真题汇编-物质结构与性质
- 山东省惠民县第二中学致远部2020-2021学年高二上学期化学10月月考试卷
- 2021年高考化学真题试卷(天津卷)
- 安徽省淮南市2021年高考化学二模试卷(4月)
- 湖南省百校联考(衡阳市二模)2022届髙三化学试题
最近更新
- 2010年3月,温家宝总理在政府工作报告中指出:“我们所做的一切都是要让人民生活得更加幸福,更有尊严、社会更加公正和谐。
- 阅读说明文,完成17-20题。(13分)塑料瓶装水真的“干净”吗①出门在外,口渴的时候我们都习惯
- 白炽灯泡的灯丝断开后,可把断头搭接起来继续使用,这时灯丝的( ) A.电阻变大,电流减小
- 一块物体m从某曲面上的Q点自由滑下,通过一粗糙的静止传送带后,落到地面P点,若传送带的皮带轮沿逆时针方向转动起来,使传送
- 关于速度、速度改变量、加速度,正确的说法是( )A.物体运动的速度改变量越大,它的加速度一定越大B.速度很大的物体
- 下图为《广州日报》1月26日刊登的反映我国某一历史时期社会现象的讽刺画,下列最有可能与此有关的是
- 下列关于物体运动的描述可能的是( )A.速度变化越来越快,加速度越来越小B.速度变化的方向为正,加速度的方向为负C
- 为了提醒人们爱护绿地和花草,保护环境,一些公园的草坪上立着“小草也有生命”的牌子。对此说法不正确的是( )A.人的生
- 阅读《文章千古说韩愈》,回答文后小题。(20分)韩愈为唐宋八大家之首,其文章写得好是真的。所以,我读韩愈其人是从读韩愈其
- He said he would pick me up home after work.He didn’t,______
- —Is David a man with goodmanners ? —I don’t think so . As
- 已知函数(Ⅰ)求的最小值; (Ⅱ)若对所有都有,求实数的取值范围.
- .右对右图的解读,不正确的是( ) A.它持续时间三百多年 B.葡萄牙是主要参与者 C.它促进了欧洲的
- 下列句子中没有语病的一项是 A.由于她这样好的成绩,得到了老师和同学们的赞扬。 B.为开阔学生视野,我们要开展丰富多彩的
- 若,且是第二象限的角,则=
- (2015中考广西南宁卷)阅读下面的材料,按要求作文。 日成一事,事不在大,把身边的小事做好。不在乎轰轰烈烈,而在乎精心
- 如图,在△ABC中,D、E在BC上,且BD=DE=AD=AE=EC,则∠BAC的度数是() A. 30°
- 明传奇剧之所以吸收南方各种民间音乐形成四大声腔的根本原因在于 ( ) A.南方商品经济发达,市民队伍较大 B.北
- 坚持与时俱进,就是党的全部理论和全部工作要 A、体现时代性 B、把握规律性 C、富于创造性 D、注重协调性
- 下图是工业上冶炼铝的工艺流程图:写出有关的化学反应方程式: ①_____________________________






 的晶体类型;
的晶体类型; 的简单离子半径大小;
的简单离子半径大小; 最外层电子的电子云形状为。
最外层电子的电子云形状为。 主要用于氯碱工业,写出阳极的电极反应。
主要用于氯碱工业,写出阳极的电极反应。
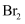 ,并用纯碱吸收。纯碱吸收
,并用纯碱吸收。纯碱吸收  ,吸收
,吸收  时,转移电子为mol。
时,转移电子为mol。
 和
和  ,即有
,即有  晶体析出。结合速率与平衡理论解释
晶体析出。结合速率与平衡理论解释  ,发生反应:
,发生反应:  ,配平上述方程式。
,配平上述方程式。
 和
和 , 将氨氮转化为
, 将氨氮转化为 沉淀除去。
沉淀除去。 , 除生成
, 除生成 沉淀外,还可能生成另一沉淀的化学式为。
沉淀外,还可能生成另一沉淀的化学式为。 溶液,将氨氮最终转化为
溶液,将氨氮最终转化为 除去。
除去。 时,
时, [即
[即 ]与水中余氯(即氧化性的氯,包括
]与水中余氯(即氧化性的氯,包括 、
、 、
、 、
、 等)含量关系如图-1所示。
等)含量关系如图-1所示。
 时发生反应的离子方程式为。
时发生反应的离子方程式为。 后迅速下降、
后迅速下降、 后下降变缓,其原因可能是。
后下降变缓,其原因可能是。 的质量,单位
的质量,单位 )。取
)。取 市售待测
市售待测 , 用乙酸-乙酸钠溶液控制稀释液
, 用乙酸-乙酸钠溶液控制稀释液 溶液充分反应后,滴加2~3滴淀粉溶液,用
溶液充分反应后,滴加2~3滴淀粉溶液,用 的标准
的标准 溶液滴定至终点,共消耗标准
溶液滴定至终点,共消耗标准 )。计算该市售
)。计算该市售


 >MnO2>I2
>MnO2>I2



