高考二轮复习知识点:原子晶体(共价晶体)
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
氮氧化铝(AlON)属于原子晶体,是一种超强透明材料,下列描述错的是( )
A . AlON和石英的化学键类型相同
B . 电解熔融AlON可得到Al
C . AlON的N元素化合价为﹣1
D . AlON和石英晶体类型相同
|
|
| 2. 单选题 | 详细信息 |
|
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A . 1.5 gCH3+含有的电子数为NA
B . 在1 L 0.1mol/L氯化铝溶液中阳离子总数大于0.1NA
C . 60g SiO2和12g金刚石中各含有4NA个Si—O键和4NA个C—C键
D . 标准状况下,11.2 L四氯化碳中含有的C—Cl键的个数为2NA
|
|
| 3. 综合题 | 详细信息 | |||||||||||||||
|
[化学一一选修3:物质结构与性质]碳族元素的单质和化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
|
||||||||||||||||
| 4. 综合题 | 详细信息 |
|
C、N和Si能形成多种高硬度材料,如Si3N4 , C3N4 , SiC.
|
|
| 5. 单选题 | 详细信息 |
|
原子晶体具有的性质是()
A . 熔点高
B . 易导热
C . 能导电
D . 有延展性
|
|
| 6. 单选题 | 详细信息 |
|
二氧化硅是制造光导纤维的重要原料,其晶体类型属于( )
A . 原子晶体
B . 离子晶体
C . 分子晶体
D . 金属晶体
|
|
| 7. 单选题 | 详细信息 |
|
金刚石的熔点为a℃,晶体硅的熔点为b℃,足球烯(分子式为C60)的熔点为c℃,三者熔点的大小关系是( )
A . a>b>c
B . b>a>c
C . c>a>b
D . c>b>a.
|
|
| 8. 综合题 | 详细信息 |
|
硅是构成矿物和岩石的主要成分,单质硅及其化合物具有广泛的用途。完成下列填空:
|
|
| 9. 综合题 | 详细信息 | ||||||||
|
绪(Ge)是半导体元素,应用广泛,回答下列问题:
|
|||||||||
| 10. 单选题 | 详细信息 |
|
硅是制作光伏电池的关键材料。在Si晶体中掺杂不同种类的元素,可形成多电子的n型或缺电子的p型半导体。n型和p型半导体相互叠加形成p-n结,此时自由电子发生扩散运动,在交界面处形成电场。下列说法正确的是( )
A . 1 mol Si晶体中含有的Si-Si键数目为4NA
B . 若在Si晶体中掺入P元素,可得n型半导体
C . p-n结中,n型一侧带负电,p型一侧带正电
D . 光伏电池的能量转化形式为:光能→化学能→电能
|
|
- 高中化学人教版(2019)2021-2022学年选择性必修3 5.1合成高分子的基本方法——一课一练
- 云南省名校联盟2021-2022学年高一下学期期中考试化学试题
- 山东省2021-2022学年高二10月“山东学情”联考化学试题(B)
- 北京首都师范大学第二附属中学2020-2021学年高三上学期化学10月月考试卷
- 辽宁省锦州市2022届高三第一次质量检测化学试题
- 河北省秦皇岛市宏远学校2020-2021学年高一上学期化学期末考试试卷
- 宁夏吴忠市2022届高三4月模拟联考(二模)理科综合化学试题
- 湖南省怀化市2021-2022学年高二上学期期末考试化学试题
- 福建省宁德市同心顺联盟2021-2022学年高一下学期期中联合考试化学试题
- 辽宁省丹东市2021-2022学年高二上学期期末教学质量监测化学试题
- 天津市和平区2022届高三第二次质量调查化学试题
- 安徽省宿州市北方中学2021-2022学年高一上学期化学第一次月考试卷
- 乡人种菜为业。每日晨起,担菜两筐,入城中,沿街唤卖。人以其索价不二,菜又肥美,故争买之。乡人得钱,易布与米,一家衣食,得
- 在“测量小灯泡功率”的实验,小灯泡额定电压为2.5V,额定功率不超过1W. (1)请你用笔画线代替导线,将图甲实物电路连
- 下列句子中没有语病的一句是 A.自从他进入象山中学的那一天起,就一直认真刻苦地学习。 B.能否培养学生的思维能力,是衡量
- 证明lg2是无理数.
- 如果函数为反比例函数,则的值是 ( ) A
- 人的双眼皮是显性性状(由显性基因A控制),单眼皮是隐性性状(由隐性基因a控制)。如果父母双方控制该性状的基因组成都是Aa
- 读图(阴影部分为黑夜),完成下题。此时,北京时间为( ) A.5时 B.
- 常温下能在浓HNO3中溶解的金属是( ) A.Al B.Ag
- 某知识竞赛的试题中出现了这样一组词语:“华清池、兵谏、联共抗日、和平解决”,由此判断,该题正确答案是 ( ) A.
- 下列各句中,没有语病的一句是()A.关于论文抄袭屡禁不绝的原因,人们有很多解释,诸如急功近利的学术风气,学术道德的沦丧,
- 新中国成立以来,农业为工业化做出了重要贡献。1950年至1979年,农业为工业建设提供的资金均为4500亿元。随着工业化
- 下列词语中,没有错别字的一项是(2分)A.玷污 物竟天择 苍海桑田 B.清洌 相得益章
- 秦始皇统一六国后,建立专制主义中央集权制度,其核心是 A.规定皇位世袭 B.建立三公九卿 C.推行郡县
- 开大收音机的音量旋钮是为了 A.增大声音的响度
- 如图所示,弧ab是半径为1 m、电阻不计的竖直金属圆环。Oa为轻质且电阻为0.1 Ω的金属杆,在a端固定一个质量为0.1
- 下列生物学研究选择的技术(方法)恰当的是 A.用3H示记的尿嘧啶核糖核苷酸研究DNA的复制 B.利用纸层析法提取叶绿体中
- 下列物质进入细胞的过程中,既不需要载体也不消耗能量的是 A.氨基酸 B.Na+
- I am looking forward to ______ your answer as soon aspossib
- 摩尔质量最大的化合物是 ( ) A. Cl2
- 在化学反应A + B D中,加入A、B、C三种物质各10g,加热至反应结束后,测 得A 已完全反应,生成D18g





 Si3N4+CO
Si3N4+CO 
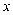 可能是(选填:“盐酸”“硝酸”或“硫酸”),理由是。
可能是(选填:“盐酸”“硝酸”或“硫酸”),理由是。 B.
B. 
 D.
D. 
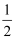 ,0,
,0,  ,
, 




