高考二轮复习知识点:原子核外电子的跃迁及应用
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
卤族元素的单质和化合物在生产生活中有重要的用途。
|
|
| 2. 综合题 | 详细信息 |
|
|
| 3. 综合题 | 详细信息 |
|
|
| 4. 单选题 | 详细信息 |
|
下列现象和应用与电子跃迁无关的是( )
A . 焰色反应
B . 石墨导电
C . 激光
D . 原子光谱
|
|
| 5. 综合题 | 详细信息 | ||||||
|
铜及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
|
|||||||
| 6. 综合题 | 详细信息 |
|
氟及其化合物用途非常广泛。回答下列问题:
|
|
| 7. 单选题 | 详细信息 |
|
下列说法错误的是( )
A . 高压钠灯可用于道路照明
B .
 可用来制造光导纤维
C . 工业上可采用高温冶炼黄铜矿的方法获得粗铜
D . 可用来制造光导纤维
C . 工业上可采用高温冶炼黄铜矿的方法获得粗铜
D .  不溶于水,可用作医疗上检查肠胃的钡餐 不溶于水,可用作医疗上检查肠胃的钡餐
|
|
| 8. 综合题 | 详细信息 |
|
硫及其化合物有许多用途。请回答下列问题。
|
|
| 9. 单选题 | 详细信息 |
|
下列现象和应用与电子跃迁无关的是( )
A . 石墨导电
B . 焰色反应
C . 原子光谱
D . 激光
|
|
| 10. 综合题 | 详细信息 |
|
铁是一种常见的金属,在生产生活中用途广泛。
|
|
- 云南省大理州祥云县2019-2020学年高二下学期化学期末考试试卷
- 2017年广西柳州市高考化学模拟试卷
- 2015-2016学年福建省莆田二十五中高一上学期第二次月考化学试卷
- 浙江省衢州市衢江区大洲中学2019-2020学年高一下学期化学开学考试卷
- 2016-2017学年河南省鹤壁市淇县一中高二上学期期中化学试卷
- 上海市松江区2020年高考化学二模试卷
- 2016年高考化学押题卷
- 高中化学鲁科版(2019)必修第二册 第1章 微项目 海带提碘与海水提溴
- 北京市东城区2017-2018学年高考理综-化学4月一模考试试卷
- 第23讲:有机物的结构、命名
- 浙江省十校联盟2019-2020学年高三下学期化学开学考试卷
- 吉林省长春市九台区师范高级中学2019-2020学年高二下学期化学期中考试试卷
- —Are all of you going tothe north this summer? —Not all. I
- 由于水的比热容比沙石或干泥土的比热容大,所以在沿海地区陆地表面的气温比海面的气温昼夜变化显著.因此() A.白天的海风多
- 公元649年6月16日,唐太宗李世民逝世,唐王朝宣布这一天是全国的忌日。后来,这一天也成为中国书法界的忌日,因为传说在这
- 上图为某大陆沿海某地区七月份等温线分布图。读图完成下题: 若仅从地形因素考虑,右面的四幅剖面图与左图中沿EF线地势起伏状
- 阅读下面一段文字,完成6——8题(9分) 十二生肖 对于一种古老的民俗文化 ————十二生肖的起源,历代学者众说纷纭。
- 从“千耦其耘到个体农耕”这一现象出现的主要原因是 A、石制工具 B、木
- 厨房里发生的下列变化为物理变化的是() A.天然气燃烧 B.铁锅生锈 C.开水沸腾 D.蔬菜腐烂
- 人类下列的哪一种细胞中,正常情况下,决定性别的染色体有可能是一个 A.初级精母细胞 B.次级精母细胞 C.神
- 掷一枚骰子,点数是3的倍数的概率是.
- 如图,P是Rt△ABC的斜边BC上异于B,C的一点,过P点作直线截△ABC,使截得的三角形与△ABC相似,满足这样条件的
- 铁、铜和铝有广泛的应用 (1)细铁丝在氧气中燃烧生成黑色固体物质的化学方程式式是 . (2)“湿法炼铜”的原理是硫酸铜溶
- 用NA表示阿伏加德罗常数的值,下列说法中正确的是() A.1molN2所含有的原子数为NA B.标准状况下,22
- 各种社会实际问题的解决,离不开公民的支持和参与。随着汽车消费的普及,道路拥挤、交通事故、尾气排放等一系列问题接踵而来,为
- 补写出下列句子中横线上的空缺部分。 ①如欲平治天下,当今之世, ?
- 情境假设:2011年3月,全国人大代表小张将出席第十一届全国人民代表大会第四次会议。阅读材料,并完成相关任务。年份 GD
- 爱国主义是对自己祖国的一种最深厚的感情,不同历史时期,爱国主义有不同的内容。下列中国近代著名人物中提出“实业救国”的是
- —They ________have prepared for the meeting more carefully.
- 如图所示用一把刻度尺和两块三角板测一枚硬币直径的示意图,由图示可得硬币的直径是 cm。
- _____ of the land in that district _____ covered with trees
- 在一个密闭容器中盛有11 g X气体(X的摩尔质量为44 g·mol-1)时,压强为1×104 Pa。如果在相同温度下,
 ,
, 


 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为  ),则N5- 中的大π键应表示为。
),则N5- 中的大π键应表示为。





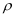 g•cm-3 , 阿伏加德罗常数的值为NA , 则晶胞中硫离子与铅离子最近的距离为nm
g•cm-3 , 阿伏加德罗常数的值为NA , 则晶胞中硫离子与铅离子最近的距离为nm 



