高考二轮复习知识点:化学平衡常数3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
升高温度,下列数据不一定增大的是( )
A . 化学反应中反应物的转化率
B . 化学平衡常数K
C . 盐类的水解常数Kb
D . 水的离子积常数Kw
|
|
| 2. 多选题 | 详细信息 |
|
硫化氢裂解制取氢气的反应为2H2S(g)
A . 该反应平衡常数随温度升高而增大
B . M点时容器内气体总压强比N的大
C . M点时,H2S的平衡转化率为50%
D . 维持M点温度不变,向容器中再充入0.2molH2S、0.2molH2、0.1molS2(g),则v(正) = v(逆)
|
|
| 3. 多选题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||
|
初始温度为t ℃,向三个密闭的容器中按不同方式投入反应物,发生如下反应:4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1 , 测得反应的相关数据如下: 2Cl2(g)+2H2O(g) ΔH=-116kJ·mol-1 , 测得反应的相关数据如下:
下列说法正确的是( )
A . 反应4HCl(g)+O2(g)
 2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
B . a>1, b>2
C . p2=1.6×105Pa,p3=4×105Pa
D . 若起始向容器Ⅰ中充入0.5 mol HCl、0.5 mol O2、0.5 mol Cl2和0.5 mol H2O,则反应向逆反应方向进行 2Cl2(g)+2H2O(l)的ΔH>-116 kJ·mol-1
B . a>1, b>2
C . p2=1.6×105Pa,p3=4×105Pa
D . 若起始向容器Ⅰ中充入0.5 mol HCl、0.5 mol O2、0.5 mol Cl2和0.5 mol H2O,则反应向逆反应方向进行
|
|||||||||||||||||||||||||||||||||||||||||
| 4. 多选题 | 详细信息 | ||||||||||||||||||||||||||||||||
|
一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+ O2(g) ⇌2SO3(g)(正反应放热),测得反应的相关数据如下:
下列说法正确的是( )
A . v1< v2 , c2< 2c1
B . K1> K3 , p2> 2p3
C . v1< v3 , α1(SO2 ) >α3(SO2 )
D . c2> 2c3 , α2(SO3 )+α3(SO2 )<1
|
|||||||||||||||||||||||||||||||||
| 5. 多选题 | 详细信息 |
|
常温下,现有0.1mol/L的NH4HCO3溶液。已知含氮或含碳各微粒的分布分数δ(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示(不考虑溶液中的CO2和NH3分子)。下列说法正确的是( )
A . 常温下
 B . 当溶液的pH=9时,溶液中存在下列关系:
B . 当溶液的pH=9时,溶液中存在下列关系: C .
C .  反应的平衡常数为K,则 反应的平衡常数为K,则 D . 往该溶液中逐滴滴加氢氧化钠时
D . 往该溶液中逐滴滴加氢氧化钠时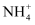 和HCO 和HCO 浓度逐渐减小 浓度逐渐减小
|
|
| 6. 综合题 | 详细信息 |
|
钪
 及其化合物具有许多优良的性能,被应用于航空航天、超导、核能等领域,以赤泥(含有 及其化合物具有许多优良的性能,被应用于航空航天、超导、核能等领域,以赤泥(含有 、 、 、 、 、 、 等)为原料提取 等)为原料提取 的流程如下: 的流程如下:
已知:① 请回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
氮氧化物的有效去除和资源的充分利用是当今社会的重要研究课题。
|
|
| 8. 综合题 | 详细信息 | ||||||||||||
|
将玉米秸秆进行热化学裂解可制备出以CO、
 、 、 、 、 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。 为主要成分的生物质原料气,对原料气进行预处理后,可用于生产甲醇、乙醇等燃料。
|
|||||||||||||
| 9. 综合题 | 详细信息 |
 的捕集与转化是当今科学研究的重要课题。以 的捕集与转化是当今科学研究的重要课题。以 为原料合成 为原料合成 涉及的主要反应如下: 涉及的主要反应如下:
I. II. I的反应历程可分为如下两步: ① ②
|
|
| 10. 单选题 | 详细信息 |
|
向AgCl悬浊液中滴加少量NaBr溶液,生成浅黄色的AgBr沉淀。T℃下,饱和溶液中-lg[c(Ag+)]与-lg[c(Xn-)](Xn-指Cl-、Br-、
 )的关系如图所示。下列说法正确的是( ) )的关系如图所示。下列说法正确的是( )
A . 曲线①表示AgCl的沉淀溶解曲线
B . 升高温度,曲线②向上方平行移动
C . T℃下,Ag2CO3的Ksp为10-9.7
D . T℃下,反应AgCl(s)+Br-(ag)⇌AgBr(s)+Cl-(aq)的平衡常数K=102.6
|
|
- 2016年新疆乌鲁木齐八十二中高考化学二模试卷
- 专题32:生物大分子
- 2015-2016学年湖南省邵阳市邵阳县石齐学校高二下学期第一次月考化学试卷
- 人教版化学高二选修2第一单元课题1化工生产中的基本问题同步练习
- 广东省陆丰市2018年11月高三第一次调研理综 (化学部分)
- 2016-2017学年湖北省宜昌市金东方高中高二上学期期末化学试卷
- 北京市昌平区2020年高考化学二模试卷
- 吉林省白城市第十四中学2019-2020学年高二上学期化学期末考试试卷
- 人教高中化学一轮复习:专题7常见的有机化合物
- 吉林省桦甸市第八中学2019-2020学年高三上学期化学第三次月考试卷
- 福建省清流一中2017-2018学年高二上学期化学期中考试试卷
- 安徽省阜阳三校2019-2020学年高二上学期化学12月月考试卷
- —Mum, you promised! —Well, ______. But it was you who didn’t
- China has got a good ______ for fighting against the flu wit
- 2015年10月5日,瑞典诺贝尔医学奖评委会宣布,我国著名药学家屠哟哟获得了诺贝尔生理学或医学奖,表彰她在研究青嵩素上
- “观乎天文,以察时变;观乎人文,以化成天下。天下成其礼俗,乃圣人用贲之道也。”其意是说,圣人通过观察天象,来了解时序的变
- 下面是我县某养鸡场2001~2006年的养鸡统计图: (8分)(1)从图中你能得到什么信息.(2)各年养鸡多少万只?(3
- 下列图示与对应叙述相符的是 甲 乙 丙
- In order to direct Qinghai quake relief work , President Hu
- 研究遗传规律的主要方法是( ) A.由基因表达出的性状推知的 B.仅从理论分析总结出来的 C.从显微镜观测到染色体的变
- 下面是按一定规律排列的一列数:第1个数:;第2个数:;第3个数:;……第个数:.那么,在第10个数、第11个数、第12个
- 下列区分物质的试剂或方法不正确的是 A.用水区分氯化钙和碳酸钙
- (3分)某元素原子结构示意图为右图,请回答:(1)该元素核电荷数为 。(2)图中X= 。
- 为防止美国微软公司垄断软件行业,美国联邦政府启动了对微软公司的反垄断调查。这反映了( )A、微软公司垄断危害了公众
- 《通典》记载:阳嘉元年,尚书令左雄改察举之制,待中张衡上疏日:自初举拳廉,到今二百年,必先孝行:行有馀力,乃草文法耳。今
- 下列各句中,加点的成语使用恰当的一句是 A、陈寅恪先生上课时旁征博引,还不时夹着所引史料的数种语言文字,这使得外语尚未过
- Adrian’s “Amazing Race” started early when his parents reali
- 已知函数的图象经过(0,1),则函数的图象必经过点 ;
- 如图,△ABC中,AB=AC,BD⊥AC于点D,CE⊥AB于点E,BD和CE交于点O,AO的延长线交BC于点F,则图中全
- 阅读材料,回答下列问题。 以“城市,让生活更美好”为主题的上海世博会将于2010年5月至10月在中国上海举行。目前已
- 水是宝贵的自然资源,请回答下列问题: (1)电解水的化学方程式是:________________________,通过
- 若,则__________。




 为磷酸酯萃取剂(密度小于水);②
为磷酸酯萃取剂(密度小于水);② 易水解。
易水解。 钪的浸出率开始下降,其原因是;滤渣的主要成分(填化学式)。
钪的浸出率开始下降,其原因是;滤渣的主要成分(填化学式)。
 是一种液态化合物,与水发生剧烈的非氧化还原反应,生成两种有刺激性气味的气体,化学反应方程式为:,“回流过滤”中
是一种液态化合物,与水发生剧烈的非氧化还原反应,生成两种有刺激性气味的气体,化学反应方程式为:,“回流过滤”中 转化成
转化成 ,
,  ,
,  。“沉钪”时,发生反应:
。“沉钪”时,发生反应: , 此反应的平衡常数
, 此反应的平衡常数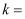 (用含a、b、c的代数式表示)。
(用含a、b、c的代数式表示)。
 5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1 , 则其正反应活化能为kJ•mol-1 (用含E逆的代数式表示)。
5N2(g) +6H2O(g)的逆反应活化能为 E逆 kJ•mol-1 , 则其正反应活化能为kJ•mol-1 (用含E逆的代数式表示)。


 )
) 的焓变
的焓变
 的物质的量之比为2:1
的物质的量之比为2:1 。将等物质的量的
。将等物质的量的 的体积分数随温度和压强的变化关系如图所示。
的体积分数随温度和压强的变化关系如图所示。


 (填“>”“<”或“=”,下同)。判断依据是。
(填“>”“<”或“=”,下同)。判断依据是。
 。
。 (Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea=
(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效能,进行了实验探究,依据实验数据获得下图所示曲线。在m催化剂作用下,该反应的活化能Ea= 。从图中信息获知催化效能较高的催化剂是(填“m”或“n”)。
。从图中信息获知催化效能较高的催化剂是(填“m”或“n”)。
 (主反应)
(主反应) (副反应)
(副反应) (反应速率较快)
(反应速率较快) (反应速率较慢)
(反应速率较慢) 。
。
 , 提高
, 提高 对反应I速率影响更大,其原因是。
对反应I速率影响更大,其原因是。
 合成
合成
 时,将
时,将 和
和 充入
充入 体积不变的密闭容器中,在有催化剂存在的条件下,只发生反应
体积不变的密闭容器中,在有催化剂存在的条件下,只发生反应 。若初始压强为
。若初始压强为 , 一段时间后反应达到平衡,平衡时产物的物质的量之和与剩余反应物的物质的量之和相等,则达到平衡时
, 一段时间后反应达到平衡,平衡时产物的物质的量之和与剩余反应物的物质的量之和相等,则达到平衡时 (保留两位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(保留两位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 , 温度T时,向
, 温度T时,向 恒容密闭容器中充入
恒容密闭容器中充入 , 反应过程中
, 反应过程中 的物质的量随时间变化如下图所示。实验测得
的物质的量随时间变化如下图所示。实验测得 ,
,  ,
,  为速率常数,只与温度有关,则T温度时
为速率常数,只与温度有关,则T温度时 (用含有m的代数式表示)。该反应在(“高温”或“低温”)下更易自发进行。
(用含有m的代数式表示)。该反应在(“高温”或“低温”)下更易自发进行。 




