高考二轮复习知识点:粗盐提纯
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下图为海水利用的部分过程。下列有关说法正确的是( )
A . 粗盐提取精盐的过程只发生物理变化
B . 用澄清的石灰水可鉴别Na2CO3产品是否含有NaHCO3
C . 在第②、④步骤中,溴元素均被还原
D . 制取NaHCO3的反应是利用其溶解度小于NaCl
|
|
| 2. 综合题 | 详细信息 |
|
NaClO3可用于制取二氧化氯、亚氯酸钠及高氯酸盐等。以原盐(主要成分为NaCl)为原料制备氯酸钠的工艺流程如下:
已知:Cr2O72-+H2O 回答下列问题:
|
|
| 3. 单选题 | 详细信息 |
|
为了除尽NaCl中所含杂质MgCl2、CaCl2和Na2SO4 , 先后向溶液中加入稍过量的NaOH、BaCl2和NaCO3 , 去除沉淀后再用盐酸调节pH=7。下列加入该三种试剂的先后顺序错误的是( )
A . NaOH、BaCl2、 Na2CO3
B . BaCl2、Na2CO3、 NaOH
C . NaOH、Na2CO3、BaCl2
D . BaCl2、NaOH、Na2CO3
|
|
| 4. 综合题 | 详细信息 |
|
小苏打是一种常用的食品添加剂。
|
|
| 5. 单选题 | 详细信息 |
|
用化学沉淀法去除粗盐中的杂质离子,包括粗盐溶解、加沉淀剂、过滤、调节pH、蒸发结晶等步骤。下列说法错误的是( )
A . 沉淀剂的添加顺序可以是NaOH溶液、BaCl2溶液、Na2CO3溶液
B . 向滤液中滴加盐酸,调节pH至滤液呈中性
C . 蒸发结晶时,当蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸干
D . 溶解、过滤、蒸发结晶等过程都使用玻璃棒搅拌溶液
|
|
| 6. 单选题 | 详细信息 |
|
粗盐(含泥沙、CaCl2、MgSO4等)提纯得到的NaCl溶液中仍含有少量K+ , 需进一步提纯才可得到试剂级氯化钠,实验装置如图所示(已知:NaCl+H2SO4(浓)
 HCl↑+NaHSO4).下列叙述错误的是( ) HCl↑+NaHSO4).下列叙述错误的是( )
A . 粗盐提纯实验需要NaOH溶液、BaCl2溶液、Na2CO3溶液、HCl溶液
B . 关闭止水夹K,打开分液漏斗活塞,若液体不滴落,证明a中气密性良好
C . 实验过程中,c中有固体析出
D . d中加入NaOH溶液吸收尾气
|
|
| 7. 综合题 | 详细信息 |
|
海洋是一个巨大的化学资源宝库。海水资源综合利用的部分过程如下图所示。
回答下列问题:
|
|
| 8. 多选题 | 详细信息 |
|
下列实验操作符合题意且能达到实验目的的是( )
A . 利用图甲装置蒸发氯化钠溶液获得食盐晶体
B . 利用图乙装置用
 固体和水制备氧气
C . 利用图丙装置用饱和 固体和水制备氧气
C . 利用图丙装置用饱和 溶液和蒸馏水制备 溶液和蒸馏水制备 胶体
D . 利用图丁装置除去 胶体
D . 利用图丁装置除去 中的 中的
|
|
| 9. 实验探究题 | 详细信息 |
|
严谨的实验设计能有效规避实验风险,能重复实验并得到相同的结果。由粗盐制备试剂级的NaCl的相关实验步骤和装置如下:
【粗盐的提纯】 第I步:称取20.0g粗盐(含MgCl2、CaCl2、Na2SO4杂质),用80mL水溶解,加入1.0mol/L BaCl2至观察不到明显沉淀为止,用倾析法分离,保留滤液。 第II步:向滤液中先后加入过量2.0mol/L NaOH、1.0mol/L Na2CO3 , 过滤,再用3.0mol/L HCl调节pH至1~2。 第III步,加热浓缩至溶液刚刚出现微晶膜。
|
|
| 10. 单选题 | 详细信息 |
|
下列实验操作中,错误的是( )
A . 粗盐提纯时,将称量的粗盐放入烧杯中加适量的水搅拌溶解
B . 硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C . 测定未知NaOH溶液浓度时,把量取的标准酸液加入湿润的锥形瓶中进行滴定
D . 配制0.1mol·L-1H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
|
|
- 河北省定州市2020-2021学年高二下学期化学期中考试试卷
- 吉林省白山市2020-2021学年高一下学期期末考试化学试题
- 河南省南阳市2020-2021学年高三上学期化学期中考试试卷
- 陕西省渭南市富平县2020-2021学年高一下学期期末考试化学试题
- 江苏省苏州市吴江区2020-2021学年高二上学期化学期中考试试卷
- 福建省泉州市2021-2022学年高三上学期化学开学考试试卷
- 广西梧州市2021年高考理综-化学3月模拟试卷
- 陕西省汉中市2021-2022学年高一下学期期中考试化学试题
- 上海市黄浦区2021年高考化学二模试卷
- 冲刺2021高考化学押题训练(七)电化学及其应用
- 黑龙江省西北部八校2021-2022学年高一下学期期中联考化学试题
- 广西柳州市2021年高考化学三模试卷
- ......
- _____ economic, political andcultural differences, it is di
- _____leaves the office last must close all the windows and t
- “阳光体育”活动在滨江学校轰轰烈烈第开展,为了解同学们最喜爱的体育运动项目,小李对本班50名同学进行了跳绳、羽毛球、篮
- 将①、②两个植株杂交,得到③,将③再作进一步处理,如下图所示。下列分析错误的是 A.由③到④过程一定发生了等位基因分离
- On his a_______, he was greatly welcomed by his fans.
- 、发起新文化运动的先进知识分子,试图冲破旧的思想牢笼,他们大都: A、信仰马克思主义 B、宣传社会主义 C、认同无
- In contrast to earlier decades, the whole journey of Shenzho
- 某电铃正常工作时的电压是6V,电阻是10,现手边有一电压是15V的电源,要使电铃正常工作应将这个电铃与_________
- 系好白毛巾、舞起红绸带、敲响红腰鼓…安塞腰鼓队是国庆庆典群众游行方阵中唯一的京外队伍,如图所示鼓声是由于鼓面产生的,然后
- 下列文字,依文意排列,顺序最恰当的选项是( ) 若乃升于高以望江山之远近, , , ,
- (2013重庆卷)2.题2图是单克隆抗体制备流程的简明示意图。下列有关叙述,正确的是A.①是从已免疫的小鼠脾脏中获得的效
- 某小组测酱油的密度,在烧杯中倒入适量的酱油,测出烧杯和酱油的总质量是82.4g,将烧杯中一部分酱油倒入量筒中,如甲图所示
- “还有几位‘大师’们捧着几张古画和新画,在欧洲各国一路的挂过去,叫做‘发扬国光’。” 这段文字使用的修辞方法有:____
- 下列句子中加点成语或俗语使用有误的一项是 A.以前的科幻电影中的许多设想,当时看起来是不可思议的,现在却不断变为现实。
- Mr. Johnson lived in the woods with his wife and children
- 生活中存在以下现象:(1)婴幼儿经常尿床,但随着年龄的增长,这种现象会明显减少;(2)由于过度惊恐而出现无意识排尿。以上
- 生物体的形态结构总是与其生活的环境相适应。下列有关叙述中错误的是 A.家鸽前肢演变为翼,适于空中飞翔 B.野兔神
- 2012年9月24日,四川省成都市申级人民法院对重庆市原副市长、公安局原局长王立军徇私枉法、叛逃、滥用职权、受贿案作出一
- 现存的每一种生物,都具有与其生活环境相适应的__________和__________。


 2CrO42-+2H+。
2CrO42-+2H+。


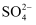 、
、 、
、 等可溶性杂质。为制得纯净的食盐晶体,操作简述如下:
等可溶性杂质。为制得纯净的食盐晶体,操作简述如下: 溶液、溶液;
溶液、溶液; 制取
制取 的化学方程式为
的化学方程式为
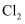 , 其目的是(用离子方程式表示)。
, 其目的是(用离子方程式表示)。 、
、

 已经除净的实验方法是。
已经除净的实验方法是。




