高考二轮复习知识点:氢键的存在对物质性质的影响1
高考二轮复习知识点:氢键的存在对物质性质的影响1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
硫酸铵[(NH4)2SO4]一种优良的氮肥(俗称肥田粉),适用于一般土壤和作物,能使枝叶生长旺盛,提高果实品质和产量,增强作物对灾害的抵抗能力,可作基肥、追肥和种肥,与氢氧化钙在加热的条件下可以生成氨气。根据所学知识回答下列问题:
|
|
| 2. 综合题 | 详细信息 |
|
铁和钴是两种重要的过渡元素。
|
|
| 3. 综合题 | 详细信息 | |||||||||
|
补铁剂常用于防治缺铁性贫血,其有效成分般为硫酸亚铁、琥珀酸亚铁、富马酸亚铁和乳酸亚铁等。回答下列问题:
|
||||||||||
| 4. 综合题 | 详细信息 |
|
三氟化氮(NF3)是一种无色、无臭的气体。三氟化氮在一定条件下与水蒸气能发生氧化还原反应,反应产物中生成酸 X、酸 Y 和一种无色气体(遇空气变成红棕色),其中酸 X 是一种弱酸,酸Y 为常见的含氧强酸。
|
|
| 5. 综合题 | 详细信息 | ||||||
|
过氧乙酸又名过醋酸
 ,是重要化工原料,也是一种绿色生态杀菌剂,其制法为 ,是重要化工原料,也是一种绿色生态杀菌剂,其制法为  。 。
|
|||||||
| 6. 推断题 | 详细信息 |
|
均由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原予的数目依次为2、3、4、6。A和C分子中的原子个数比为1∶1,B和D分子中的原子个数比为1∶2。D可作为火箭推进剂的燃料。请回答下列问题:
|
|
| 7. 综合题 | 详细信息 |
|
磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料。 LiFePO4可用FeCl3、NH4H2PO4、LiCl和苯胺(
|
|
| 8. 单选题 | 详细信息 |
|
某离子[Y2Z4XW2]-的结构如图,且所有原子最外层都达到8电子稳定结构,X、Y、Z、W位于同一短周期,X是其中原子序数最小的元素,W既是同周期也是同主族中原子半径最小的元素。下列说法正确的是( )
A . 该结构中的化学键均为极性共价键
B . Y和Z形成的化合物都是酸性氧化物
C . 皮肤上沾有强碱液,用大量水冲洗后,可以涂抹上稀H3XO3溶液
D . Z和W分别与氢元素形成的10电子化合物的沸点:后者高于前者
|
|
| 9. 单选题 | 详细信息 |
|
W、X、Y、Z是原子序数依次增大的短周期主族元素,W、Y分别与X形成的化合物均会导致酸雨。下列说法中一定正确的是( )
A . 简单离子半径中最大的是Z
B . 简单氢化物中熔沸点最高的是X
C . 氧化物对应水化物的酸性Z比Y强
D . W的氢化物分子含10个电子
|
|
| 10. 单选题 | 详细信息 |
|
据报道,75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活新型冠状病毒。对于上述化学药品的说法错误的是( )
A .
 能与水互溶
B . 能与水互溶
B .  通过氧化灭活病毒
C . 过氧乙酸与乙酸是同系物
D . 氯仿又叫三氯甲烷 通过氧化灭活病毒
C . 过氧乙酸与乙酸是同系物
D . 氯仿又叫三氯甲烷
|
|
高中化学 试卷推荐
- 2016年宁夏银川市长庆高级中学高考化学一模试卷
- 吉林长春市榆树高级中学2019-2020学年高二下学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题27 化石燃料与有机化合物
- 北京市丰台区2018-2019学年高二上学期化学期中考试试卷
- 湖南省株洲市2017-2018学年高考理综-化学二模考试试卷
- 北京市东城区2015-2016学年高一上学期化学期末考试试卷
- 2016年上海市闵行区高考化学一模试卷
- 2015-2016学年四川省资阳市高一上学期期末化学试卷
- 福建省龙岩市2017-2018学年高考理综-化学4月模拟考试试卷
- 2015-2016学年广东省茂名市高州中学高二下学期期末化学试卷
- 2016-2017学年河南省焦作市高二上学期期中化学试卷
- 天津市河北区2020年高考化学二模试卷
最近更新
- 激光打印机是常见的办公用品,它所用墨粉的主要成分是极细的碳粉。 (1)碳粉不具有的性质是 (填序号)。 A
- All the doctors in the hospital insisted that he_____ badly
- 英国学者约翰·W·梅森认为,如果把“冷战”时期重新定义为“长时期的和平”倒是颇为令人耳目一新的。作者对“冷战”重新定义的
- The English are well known for their politeness:it’s everywh
- . 保护环境是每个公民的责任。下列做法有利于环境保护的是 ( ) ①推广使用无磷洗涤
- 13.阅读下面这首宋诗,回答问题。 雨过至城中苏家 宋 黄庭坚 飘然一雨洒青春,九陌净无车马尘。 渐散紫烟笼帝阙,稍回晴
- 请依据以下信息写一则通知。(120词左右) 1) 活 动 英语演讲比赛(English-speaking Contest
- 2009年12月,《国务院关于推进海南_______建设发展的若干意见》发布,确定要将海南省建设成为世界一流的海岛休闲度
- 17.下列有关植物激素的叙述,正确的是 A.生长素既能疏花疏果,也能防止落花落果 B.脱落酸在植物的衰老阶段含量降低 C
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的以下作文。 文中共有10处语言错误,每句中最多有
- 公民购买商业保险是一种投资行为,对商业保险的正确认识有 ①可以分为人身保险和财产保险 ②包括医疗保险、养老
- In science fictions, aliens are _________(生物) from the outer
- 综观2010年国际形势,一方面国际社会动荡不安,地区矛盾加剧;另一方面和平与发展.①对话与合作仍然是国际关系中的主流。对
- 如图所示,一足够长倾角为θ的光滑斜面,一弹簧上端固定在斜面的顶端,下端与物体b相连,物体b上表面粗糙,在其上面放一物体a
- 某男子患钟摆型眼球震颤遗传病,他与正常女子结婚,他们的女儿均患此病,但儿子都正常,则此遗传病的遗传方式是 A.常染色体显
- 已知函数(,且)的图象上关于直线对称的点有且仅有一对,则实数的取值范围是( ) A. B. C.
- 对公式①P=和公式②P=UI,下列说法正确的是( ) A、要想计算同学爬楼的功率大小,应采用公式① B、要想计
- 已知变量x,y满足约束条件试求解下列问题. (1)z=的最大值和最小值; (2)z=的最大值和最小值; (3)z=|3x
- 1. 如图所示,当S闭合,甲、乙两表是电压表时,两表示数之比U甲:U乙=5:3;当S断开,甲,乙两表为电流
- 某中学(1)班的50名学生联名向市长写了一封热情洋溢的信,就培养市民的卫生和环保意识提了七条建议。这些年50名学生 ①工



 的原因。
的原因。
 与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。
与纸浆中的过氧乙酸以及过渡金属离子反应以提高漂白效率。硼氢化钠、硼氢化铝被认为是有机化学上的“万能还原剂”。 
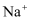 的配位数为。已知:硼氢化钠晶体的密度为
的配位数为。已知:硼氢化钠晶体的密度为  ,
,  代表阿伏加德罗常数的值,则a=nm(用含
代表阿伏加德罗常数的值,则a=nm(用含  、
、 





