湖南师大附中2015-2016学年高二下学期化学入学考试试卷
湖南师大附中2015-2016学年高二下学期化学入学考试试卷
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在一密闭容器中,反应aA(g)+bB(g)⇌mC(s)+nD(g)达到平衡后,保持温度不变,将容器体积减小为原来体积的
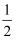 ,达到新的平衡时,D的浓度是原来的1.7倍,下列说法正确的是( ) ,达到新的平衡时,D的浓度是原来的1.7倍,下列说法正确的是( )
A . 物质B的转化率增大
B . 平衡向正反应方向移动
C . 物质A的体积分数增大
D . a+b>m+n
|
|
| 2. 单选题 | 详细信息 |
|
化学在生产和日常生活中有着重要的应用.下列叙述正确的是( )
A . 钢铁设备与直流电源正极相连可防腐
B . 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒
C . 开启啤酒瓶后,瓶中立刻泛起大量泡沫不能用勒夏特列原理解释
D . 废旧电池中的汞、锅、铅等重金属盐对土壤和水源会造成污染
|
|
| 3. 单选题 | 详细信息 |
|
在100mL H2SO4与CuSO4的混合液中,用石墨作电极电解,两极上均收集到2.24L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
A . 0.5 mol/L
B . 1 mol/L
C . 3 mol/L
D . 4 mol/L
|
|
| 4. 单选题 | 详细信息 |
|
一定温度下,下列叙述是可逆反应N2(g)+3H2(g)⇌2NH3(g),在定容密闭容器中达到平衡的标志的是( )
①NH3的生成速率与NH3的分解速率相等; ②单位时间内amolN2生成,同时生成3a mol H2; ③N2的浓度不再变化; ④混合气体的总压强不再变化; ⑤混合气体的平均摩尔质量不再变化; ⑥用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2; ⑦N2、H2、NH3的分子数目比为1:3:2; ⑧混合气体的密度不再变化.
A . ②⑤
B . ①③④⑤
C . ②⑥⑦⑧
D . ⑤⑥⑧
|
|
| 5. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 1 mol H2完全燃烧生成气态水,放出241.8 kJ热量,H2的燃烧热△H=-241.8 kJ/mol
B . 在稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3kJ/mo1
C . 热化学方程式中,化学式前面的化学计量数可表示微粒数,不可表示物质的量
D . 已知:C(金刚石,s)=C(石墨,s) △H<0,因此金刚石比石墨稳定
|
|
| 6. 单选题 | 详细信息 |
|
常温下,下列溶液中各组离子一定能大量共存的是( )
A . 加入铝粉有氢气生成的溶液中:Mg2+ , Cl- , NO3- , K+
B . 常温下,c(H+) =0.1 mol/L的溶液中:Na+ , AlO2-、S2-、 SO32-
C . 含有0.1 mol/LHCO3-的溶液:Na+ , Fe3+ , NO3- , SCN-
D .
 =0.1 mol/L的溶液:Na+ , K+ , CO32- , NO3- =0.1 mol/L的溶液:Na+ , K+ , CO32- , NO3-
|
|
| 7. 单选题 | 详细信息 |
|
用比表示阿伏加德罗常数的数值,下列说法正确的是( )
A . 1L1mol/L的氯化铁溶液中,若Cl-的数目为3 NA , 则Fe3+的数目为NA
B . 1 molN2和3 molH2在一定条件下充分反应,转移电子数目为6NA
C . 常温下,1L0.1mol/L的Na2S溶液中阴离子数目大于0.1 NA
D . 0.1 mol Cl2通入水中,转移电子的数目为0.1NA
|
|
| 8. 单选题 | 详细信息 |
|
反应CH2=CH2+ H2→CH3-CH3 , 有关化学键的键能如下:
则该反应的反应热△H为( )
A . +288.8kJ/mo1
B . -703.4 kJ/mo1
C . +125.4kJ/mo1
D . -125.4 kJ/mo1
|
|
| 9. 单选题 | 详细信息 |
|
在已经处于化学平衡状态的体系中,如果下列量发生变化,化学平衡一定会移动的是( )
A . 反应物和生成物的浓度改变
B . 反应体系的压强改变
C . 正、逆反应的速率改变
D . 反应物的转化率改变
|
|
| 10. 单选题 | 详细信息 |
|
下列有关实验操作的说法错误的是( )
A . 中和滴定盛待测液的锥形瓶中有少量水对滴定结果无影响,锥形瓶不能用待测液润洗
B . 酸式和碱式滴定管用蒸馏水洗净后还需用标准液或待测液润洗
C . 滴定时左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视锥形瓶中颜色变化
D . 滴定前仰视读数,滴定后平视刻度读数,被测待测溶液偏高
|
|
高中化学 试卷推荐
- 2016-2017学年江西省抚州市崇仁二中高二上学期期中化学试卷
- 浙江省温州十五校联合体2019-2020学年高二上学期化学期中考试试卷
- 陕西省汉中市2019-2020学年高三上学期化学第五次质量检测试卷
- 2016-2017学年江西省宜春三中高三上学期期中化学试卷
- 2015-2016学年河南省信阳市浉河区东双河一中高三下学期月考化学试卷(2月份)
- 辽宁省大连市2020年高考化学二模试卷
- 2016-2017学年湖南省株洲市醴陵二中、醴陵四中两校联考高一上学期期中化学试卷
- 2015年四川省攀枝花市米易中学高考化学模拟试卷(4)
- 2016-2017学年陕西省商洛市商州区中学高二上学期期中化学试卷
- 人教版化学高一必修1第三章第三节用途广泛的金属材料同步练习
- 安徽省A10联盟2016-2017学年高三下学期理综化学开学考试试卷
- 备考2020年高考化学二轮专题 05 无机非金属及其化合物
最近更新
- 证明辩证唯物主义时空观的科学依据是 A. 牛顿力学 B.能量守恒和转化定律 C. 达尔文进化论 D. 非欧几何和相对论
- 近些年来,自然灾害在全球范围频繁发生,自然灾害影响着人类生命安全,给人类造成极大经济损失,对自然环境也会产生极大的破坏。
- 下列反应的离子方程式正确的是 A锌片插入硝酸银溶液中:Zn+Ag+ = Zn2++Ag B碳酸氢钙溶液加到醋酸中:Ca(
- 下列关于教材中的各项说法错误的一项是( ) A.在化学反应中,反应物转化为生成物的同时,必然发生能量的变化 B.
- At Sam’s birthday party he had many guests, who were _______
- 本文的作者是____________,江苏高邮人。全文隐隐贯穿着这样一条思路:____________→________
- 2009年12月26日,世界上运营里程最长的高速铁路____铁路客运专线正式运营。至此,中国高速铁路运营总里程已突破28
- 在资产阶级革命时代,英国通过了《权利法案》、法国颁布了《人权宣言》、美国制定了1787年宪法。这说明了 A.以法律手段限
- 阅读下面文字 当今世界,光学技术广泛应用于医学、军事、工农业生产等领域,其中光学技术成果在 改善生态环境、推动农业
- 下列关于胚胎工程的叙述,错误的是 A.体外受精是指获能的精子和成熟的卵子在相应溶液中受精 B.受精卵发育到囊胚
- 《水浒》中一百零八位好汉个个都有一段精彩的故事,人人都有一个特征鲜明的外号。 (1)请用一句话写出《水浒》中你熟悉的故事
- 针对粮肉食用油等食品价格持续上涨,国务院法制办牵头修订了《价格违法行为处罚规定》。2008年全国共查处价格违法案件6.1
- 图中的四个点分别表示四个国家的人口出生率和 死亡率,其中人口自然增长率最高的国家是 A.①
- 按图的装置进行电解实验:A极是铜锌(均匀)合金,B极为纯铜,电解质溶液中含有足量的铜离子。通电一段时间后,若A极恰好全部
- __________________,小桥流水人家。(马致远《天净沙·秋思》 )
- 若集合A={1,a,b},B={1,﹣1,2},且B=A,则a+b的值为() A.3 B.1 C
- 下图表示某生态系统生物部分各组成成分相互依存关系图,以下不合理的选项是()A.甲是生产者 B.丙不是消费者 C.丁是分
- 随着“互联网+”战略的实施,公民可以通过网络更加便捷地参与国家政治生活。但与此同时,互联网也成为某些造谣者肆意散播谣言的
- 如图,在ABCD中,已知AB=9㎝,AD=6㎝,BE平分∠ABC交DC边于点E,则DE等于 ㎝.
- 香港特别行政区中学历史教材《新理论中国历史·中四上》中提到:“在封建制度下,周天子具有‘一尊'的统治地位,诸侯必须服从天




