江西省鹰潭市2021年高考化学二模试卷
江西省鹰潭市2021年高考化学二模试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在固态金属氧化物燃料电解池中,以H2—CO混合气体为燃料,基本原理如右图所示。下列说法错误的是( )
A . Y极是原电池的正极,发生还原反应
B . 负极的电极反应式是:H2-2eˉ+O2ˉ=H2O CO-2eˉ+O2ˉ= CO2
C . 总反应可表示为:H2+CO+O2 =H2O+CO2
D . 同温同压下两极消耗的气体的体积之比是1︰1
|
|
| 2. 单选题 | 详细信息 |
|
由苯酚制取
①取代;②加成;③氧化;④消去;⑤还原
A . ①⑤④①
B . ②④②①
C . ⑤③②①④
D . ①⑤④②
|
|
| 3. 单选题 | 详细信息 |
|
化学与科学、技术、社会、环境密切相关。下列有关说法正确的是( )
A . 燃放的焰火是焰色反应所呈现出来的色彩,此焰色反应是由于火药燃烧产生的高温使某些金属元素发出特殊颜色的光,所以焰色反应是化学反应
B . 石油的分馏、裂化、裂解以及煤的干馏和液化都能促使人们更有效地使用化石能源,有利于节能和环保
C . “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷的主要成分是硅酸盐
D . 用84消毒液与酒精混合使用能更有效杀灭新冠病毒
|
|
| 4. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 球碳盐K3C60中阴阳离子个数比为1:3
B . 标准状况下,46gNO2气体中所含的分子数为
 C . 32g铜与足量硫单质完全反应,转移电子数为NA
D . 22.4L Cl2和CO的混合气体中含有的原子数为2NA
C . 32g铜与足量硫单质完全反应,转移电子数为NA
D . 22.4L Cl2和CO的混合气体中含有的原子数为2NA
|
|
| 5. 单选题 | 详细信息 |
|
某废催化剂含SiO2、ZnS、CuS及少量的Fe3O4.某实验小组以该废催化剂为原料,回收锌和铜,设计实验流程如图:
下列说法错误的是( )
A . 步骤①操作中,生成的气体可用CuSO4溶液吸收
B . 检验滤液1中是否含有Fe2+ , 可以选用KSCN和新制的氯水
C . 步骤②操作中,应先加1.0mol·L-1H2SO4 , 然后不断搅拌下缓慢加入6%H2O2
D . 滤渣1中含有SiO2 , 滤渣2中含有S和SiO2
|
|
| 6. 单选题 | 详细信息 |
|
分属周期表前三周期的四种元素W、X、Y、Z可形成结构如图的物质,该物质中所有原子均满足稳定结构,W的原子序数最大,Y、Z处于同一周期。下列说法错误的是( )
A . X、Z可形成具有强氧化性的高效消毒剂
B . X、Y、Z的原子半径从大到小为: Y > Z >X
C . 由Z和W形成的化合物中可以存在共价键
D . Y的最高价氧化物对应的水化物中,除了氢原子外所有原子满足8电子稳定结构
|
|
| 7. 单选题 | 详细信息 |
|
25℃时,c(H2C2O4)+c(HC2O
 )+c(C2O )+c(C2O 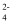 )=0.1mol·L-1的草酸溶液中,lgc(H2C2O4)、lgc(HC2O )=0.1mol·L-1的草酸溶液中,lgc(H2C2O4)、lgc(HC2O  )和lgc(C2O )和lgc(C2O 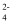 )随pH变化的关系如图所示。下列说法错误的是( ) )随pH变化的关系如图所示。下列说法错误的是( )
A . 曲线①代表lgc(H2C2O4),曲线③代表lgc(C2O
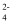 )
B . lg[Ka2(H2C2O4)]=-4.3
C . pH=2.8时,c(HC2O )
B . lg[Ka2(H2C2O4)]=-4.3
C . pH=2.8时,c(HC2O  )>0.01mol·L-1
D . pH由0变化至14过程中, )>0.01mol·L-1
D . pH由0变化至14过程中,  先增大后不变 先增大后不变
|
|
| 8. 实验探究题 | 详细信息 |
|
某化学兴趣小组对钠和钠的化合物进行了一系列的探究活动,下面是系列活动中的两个实验,请你回答下列问题:
|
|
| 9. 综合题 | 详细信息 |
|
高锰酸钾是中学化学常用的试剂。主要用于防腐、化工、制药等。实验室模拟工业上用软锰矿制备高锰酸钾的流程如下:
|
|
| 10. 综合题 | 详细信息 | |||||||||||||||
|
化学平衡及其移动是中学化学的重点知识,请回答下列问题:
|
||||||||||||||||
高中化学 试卷推荐
- 浙江省十校联盟2019-2020学年高三下学期化学开学考试卷
- 吉林省长春市九台区师范高级中学2019-2020学年高二下学期化学期中考试试卷
- 2015-2016学年山东省德州市武城二中高一下学期期末化学模拟试卷(二)
- 新疆乌鲁木齐地区2017-2018学年高考理综-化学一模考试试卷
- 2020年天津卷化学高考试题
- 贵州省遵义市2017-2018学年高考理综-化学二模考试试卷
- 备考2018年高考化学一轮基础复习:专题13 含氮化合物
- 2015-2016学年山西省太原五十三中高一上学期月考化学试卷(12月份)
- 2016年福建省福州市高考化学模拟试卷(3月份)
- 山东省潍坊市2017-2018学年高考理综-化学三模考试试卷
- 陕西省咸阳市武功县2019-2020学年高三上学期化学第一次月考试卷
- 2015-2016学年四川省眉山中学高一下学期期中化学试卷
最近更新
- 在下图中,不属于精子形成过程的是( )
- 有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适
- 将一条湿润的蓝色石蕊试纸投入盛有Cl2的集气瓶中,试纸将A.由蓝变白 B.由蓝变紫 C.由蓝变红 D.
- 阅读《鲁迅自传》选段 ①我于一八八一年生于浙江省绍兴府城里的一家姓周的家里。父亲是读书的;母亲姓鲁,乡下人,她以自修得到
- 冰在熔化过程中,下列判断正确的是 A.放出热量,内能减少 B.吸收热量,内能增加 C.温度、内能都不变 D.温度、内能都
- 读风化、侵蚀、搬运、堆积和固结成岩作用的相关示意图,表示形成新月形沙丘地貌的外力作用是()A.①
- 阅读图文材料,回答下列问题。 离岸金融亦称境外金融。离岸金融中心是20世纪50年代以来,为取得在资金、信息、贸易上的便利
- 下列各句中,加点成语使用正确的一项是( )(3分) A.有些同学为了在平时多挤出一些时间来提高自己的学习成绩,于
- 阅读下列材料 七月革命时,巴黎街头发生了巷战。在巷战中,一位名叫克拉拉·莱辛的姑娘,一马当先,在街垒上举起了象征法兰西共
- 用一根长1 m的轻质细绳将一幅质量为1 kg的画框对称悬挂在墙壁上。已知绳能承受的最大张力为10 N。为使绳不断裂,画框
- 下列关于乙醇的说法不正确的是() A.可用纤维素的水解产物制取 B.可由乙烯通过加成反应制取 C.与乙醛互为同分异构体
- 下列各句空格处应填入的词语正确的一项是 ( ) ①沿着荷塘,是一条曲折的小煤屑路。这是一条________的路;白天
- 读某地等高线地形图,分析回答下列各题。图中等高线X的数值最有可能是:( ) A.100m
- 用来完成基因的剪切与拼接的酶是( ) A、RNA聚合酶与DNA连接酶 B、限制酶与DN
- 人类研制“人造太阳”已经50多年,并在托卡马克这类装置的研究上取得了很大进展。目前即将建造的国际热核聚变实验堆就是一个全
- (本题满分12分)在△ABC中,已知,C=30,求A、B.
- 用铝箔包起0.1 mol金属钠,用针扎出些小孔,放入水中,完全反应,用排水集气法收集产生的气体,则收集到的气体为(标准状
- She likes reading. She usually________ some books from the
- 仔细观察下列各种结构模式图,据图回答:(内填图中标号)(1)图甲为置于0.3g/mL的蔗糖溶液中出现质壁分离现象的细胞,
- -2的绝对值是A.2B.-2 C. D.-






 NaN3+NaOH+NH3
NaN3+NaOH+NH3

 CO2(g)+NO(g)(正反应为放热反应)达到平衡后:
CO2(g)+NO(g)(正反应为放热反应)达到平衡后: 



