22017年高考化学备考复习专题八:化学反应与能量变化
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
已知25℃、101kPa条件下:3O2(g)=2O3(g)△H=+284.2kJ•mol﹣1下列说法正确的是( )
A . 等质量的O2比O3能量低,由O2变O3为吸热反应
B . 等质量的O2比O3能量高,由O2变O3为放热反应
C . O3比O2稳定,由O2变O3为吸热反应
D . O2比O3稳定,由O2变O3为放热反应
|
|
| 2. 单选题 | 详细信息 |
|
下列说法不正确的是( )
A . 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
B . 需要加热才能发生的反应一定是吸热反应
C . 化学键的断裂和形成是化学反应中能量变化的主要原因
D . 化学反应中的能量变化通常表现为热量的变化
|
|
| 3. 填空题 | 详细信息 |
|
从能量的角度看,断开化学键要 , 形成化学键要 . 已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151k J、299k J.则由氢气和碘反应生成1mol HI需要(填“放出”或“吸收”) k J的热量.当反应物的总能量高于生成物总能量时,该反应为反应;当反应物的总能量低于生成物总能量时,该反应为反应.
|
|
| 4. 单选题 | 详细信息 |
|
强酸和强碱的稀溶液中和热可表示为:H+(aq)+OH﹣(aq)⇌H2O(l)△H=﹣57.3kJ/mol以下4个化学方程式中,
①H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l) ②H2SO4(aq)+Ba(OH)2(aq)=BaSO4(aq)+2H2O(l) ③NH3•H2O(aq)+HCl=NH4Cl(aq)+H2O(l) ④NH3•H2O(aq)+CH3COOH(aq)=CH3COONH4(aq)+H2O(l) 其中反应热为﹣57.3kJ/mol的是( )
A . ①②
B . ③
C . ④
D . 均不符合
|
|
| 5. 填空题 | 详细信息 |
|
固态硫加热形成气态硫要吸收能量:1mol固态硫燃烧生成二氧化硫气体的焓变为△H1;1mol气态硫燃烧生成二氧化硫气体的焓变为△H2 , 则△H1 △H2 .
|
|
| 6. 综合题 | 详细信息 |
|
已知下列热化学方程式:2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJ/mol,H2(g)+
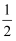 O2(g)=H2O(l)△H=﹣285.8kJ/mol,C(s)+ O2(g)=H2O(l)△H=﹣285.8kJ/mol,C(s)+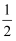 O2(g)=CO (g)△H=﹣110.5KJ/moL,C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/moL.回答下列各问题: O2(g)=CO (g)△H=﹣110.5KJ/moL,C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/moL.回答下列各问题:
|
|
| 7. 综合题 | 详细信息 | ||||||||||||||||||||
|
催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H1=﹣53.7kJ•mol﹣1 Ⅰ CO2(g)+H2(g)⇌CO(g)+H2O(g)△H2 Ⅱ 某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性;转化的CO2中生成甲醇的百分比 已知:①CO和H2的标准燃烧热分别为﹣283.0kJ•mol﹣1和﹣285.8kJ•mol﹣1 . ②H2O(1)═H2O(g)△H3=44.0kJ•mol﹣1 请回答(不考虑温度对△H的影响):
|
|||||||||||||||||||||
| 8. 单选题 | 详细信息 |
|
下列叙述正确的是( )
A . 使用催化剂能够降低化学反应的反应热(△H)
B . 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关
C . 原电池中发生的反应达平衡时,该电池仍有电流产生
D . 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小
|
|
| 9. 综合题 | 详细信息 |
|
联氨(又称肼,N2H4 , 无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:
|
|
| 10. 单选题 | 详细信息 |
|
通过以下反应均可获取H2 . 下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=571.6kJ•mol﹣1 ②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=131.3kJ•mol﹣1 ③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=206.1kJ•mol﹣1 .
A . 反应①中电能转化为化学能
B . 反应②为放热反应
C . 反应③使用催化剂,△H3减小
D . 反应CH4(g)═C(s)+2 H2(g)的△H=74.8kJ•mol﹣1
|
|
- 河北省唐山市2021年高考化学三模试卷
- 江苏省启东市2020-2021学年高三上学期化学期中考试试卷
- 天津市蓟县擂鼓台中学2020-2021学年高二上学期化学第一次月考试卷
- 四省八校2022届高三下学期开学考试理综化学试题
- 湖北省天门市2020-2021学年高一上学期化学10月月考试卷
- 2021年高考化学真题试卷(辽宁卷)
- 陕西省宝鸡市金台区2020-2021学年高二下学期期末考试化学试题
- 河南省信阳市2020-2021学年高二上学期化学期中考试试卷
- 山东省聊城市阳谷县第三中学2021-2022学年高一上学期化学10月月考试卷
- 山东省济宁市兖州区2021-2022学年高二下学期期中考试化学试题
- 内蒙古通辽市2021-2022学年高一上学期化学10月月考试卷
- 浙江省诸暨市2021-2022学年高二上学期期末考试化学试题
- 从下列物质中选择合适的物质,并将序号填在横线上: A、生石灰 B、碳酸钙 C、明矾 D、一氧化碳 E、氮气 F
- 下列现象和特征形成与自然选择无关的是 A.拟态 B.共生 C.应激性 D.性别决
- 爱因斯坦的相对论认为 ( )①时间和空间随物质运动则变化 ②物质质量随运动速度而变化③质量和能量是可以
- III.阅读理解 命题意图:以下几篇题阅读理解题主要选用了主题突出,语言流畅的叙述文、应用文和说明文,旨在训练学生的
- 秋在中国文人心中有着独特的内涵。“自古逢秋悲寂寥”,在秋的文化意识中,悲秋也可以算得上是普遍的意识了。“何处合成愁,离人
- 下列词语中设有错别字的一组是 A.告罄 绿茵场 喁喁私语 远大报负 B.脉搏 渡
- (09青岛)、实验室现有氯化镁和硫酸钠的固体混合物样品,小明同学想测定样品中氯化镁的质量分数。先称取该混合物样品20g,
- 根据句意,在相应的横线上,写出括号内所给单词的适当形式。 1. There’s not much___________
- 等质量的下列烃完全燃烧,消耗氧气最多的是( ) A.CH4 B.C2H6 C.C3
- 下列产业中,俄罗斯不具优势的是() A.能源 B.机械 C.纺织
- 下列各项中字形不合规范的一项是( ) A.厉行节约 民生凋敝
- TheInternet and the effect broughtabout did a lot of
- 下列所描述的变化不属于化学变化的是() A.用一种原子制造出另一种或几种原子 B.碳酸氢铵受热分解 C.蓝矾加热后变为白
- 一个物体在相互垂直的恒力F1和F2作用下,由静止开始运动,经过一段时间后,突然将F2的方向改为与F1同向,则物体以后的运
- 近年来,我们许多地方建成了经济技术开发区,形成这一工业集聚现象的出发点是: A.可以满足各厂家降低成本的需要 B.可以
- 如图所示,将一把金属叉子拴在一根约1 m长的金属线的中间,把线的两端分别缠绕在双手的食指上,缠绕多圈,插入耳朵.然后让叉
- 漫画中的做法有利于①扩大村民的政治权利②发扬民主,监督村务③增加决策的透明度 ④加强基层政权机关的建设 A.①②
- 如图,在正方形ABCD中,E是AB边上任意一点,BG⊥CE,垂足为点O,交AC于点F,交AD于点G。 (1)
- 来自中国外汇交易中心的最新数据显示,2013年1月4日人民币对美元汇率中间价报6.2897,较前一交易日下跌42个基点。
- PX是一种重要的化工原料。PX属于烃类,以其为原料合成高分子树脂E和P的路线如下:(部分条件省略)回答下列问题: (1)




