河南省南阳市2019-2020学年高一下学期化学期末考试试卷
河南省南阳市2019-2020学年高一下学期化学期末考试试卷
教材科目:化学
试卷分类:高一下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高一下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定碳酸钙固体与足量稀盐酸反应生成CO2的体积随时间的变化情况,绘制出下图所示的曲线甲。下列有关说法中错误的是( )
A . 在0-t1、t1-t2、t2-t3中,t1-t2生成的CO2气体最多
B . 因反应放热,导致0-t1内的反应速率逐渐增大
C . 若用单位时间内CO2的体积变化来表示该反应的速率,则t2-t3时间内平均反应速率为
 mL•s-1
D . 将碳酸钙固体研成粉末,则曲线甲将变成曲线乙 mL•s-1
D . 将碳酸钙固体研成粉末,则曲线甲将变成曲线乙
|
|
| 2. 单选题 | 详细信息 |
|
研究人员研制出一种新型储备电源-锂水电池(结构如图,高硅铸铁为惰性辅助电极),使用时加入水即可放电。下列关于该电池工作时的说法正确的是( )
A . 高硅铸铁发生氧化反应
B . OH-向高硅铸铁电极移动
C . 负极的电极反应式为Li-e-=Li+
D . 电流的方向:锂电极→导线→高硅铸铁电极
|
|
| 3. 单选题 | 详细信息 |
|
甲、乙、丙、丁为中学化学中的常见物质,其转化关系如下图所示,下列说法错误的是( )
A . 若甲为C,则丙可能为CO2
B . 若甲为NaOH,则丁可能为CO2
C . 若甲为Fe,则丁可能为Cl2
D . 若甲为H2S,则丙可能为SO2
|
|
| 4. 单选题 | 详细信息 |
|
下列有关化学用语使用正确的是( )
A . 次氯酸的结构式:
 B .
B .  (羟基)的电子式: (羟基)的电子式:  C . 比例模型
C . 比例模型 
|
|
| 5. 单选题 | 详细信息 |
|
下列反应过程中,同时有离子键和共价键的断裂和形成的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 6. 单选题 | 详细信息 |
|
下列变化符合如图示的是( )
①冰雪融化②CaCO3分解制二氧化碳③铝与盐酸的反应④Na2O2与水反应⑤硝酸铵溶于水⑥Ba(OH)2·8H2O和NH4Cl的反应
A . ②⑥
B . ①②⑤⑥
C . ②③
D . ③④
|
|
| 7. 单选题 | 详细信息 |
|
下列说法正确的是( )
A .
 ,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能。
B . 原电池的内外电路中,均是电子的定向移动形成电流
C . 因为铁的活动性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极
D . 用金属镁和铝作为电极,选择不同的电解质溶液组成原电池,镁可能作负极也可能作正极 ,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能。
B . 原电池的内外电路中,均是电子的定向移动形成电流
C . 因为铁的活动性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极
D . 用金属镁和铝作为电极,选择不同的电解质溶液组成原电池,镁可能作负极也可能作正极
|
|
| 8. 单选题 | 详细信息 |
|
分子式为
 的有机物 的有机物  ,它能在酸性条件下水解生成酸性物质 ,它能在酸性条件下水解生成酸性物质 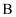 和醇 和醇 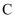 ,该醇中含有三个碳原子,则有机物A的结构最多有( ) ,该醇中含有三个碳原子,则有机物A的结构最多有( )
A . 4种
B . 8种
C . 12种
D . 16种
|
|
| 9. 单选题 | 详细信息 | |||||||||||||||||||||||||
|
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置).仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||||||||||||
| 10. 单选题 | 详细信息 |
|
下列离子方程式正确的是( )
A . 铁粉溶于过量稀硝酸:
 B .
B .  溶液中通入过量的 溶液中通入过量的  C . 向
C . 向  溶液中加入过量 溶液中加入过量  溶液: 溶液:  D .
D .  溶液中滴入少量 溶液中滴入少量  溶液: 溶液: 
|
|
高中化学 试卷推荐
- 2017年高考真题分类汇编(化学):专题2 物质的组成变化和性质用途、化学用语
- 山西省临汾市2020年高考化学一模试卷
- 第11讲:硫及其化合物
- 2015-2016学年海南省国科园实验学校高一下学期期末化学试卷
- 浙江省宁波市慈溪市六校2018-2019学年高二下学期化学期中考试试卷
- 广西桂林市2020年高考理综-化学一模试卷
- 江西省宜春市2020年高考化学5月模拟试卷
- 浙江省杭州市八校联盟2018-2019学年高一上学期化学期中考试试卷
- 广东省深圳市罗湖区2017-2018学年高二上学期化学期末考试试卷
- 备考2018年高考化学一轮基础复习:专题15 元素周期表和元素周期律
- 人教版化学高二选修5第四章第二节糖类同步练习
- 天津市武清区2018-2019学年高一上学期化学期中考试试卷
最近更新
- 个人着装风格的确立对商家制定合理的产品组合方式,实行品牌建设策略有着十分重要的意义。某服装公司对消费者进行抽样调查,结果
- 2012年4月15日,央视《每周质量报告》播出节目《胶囊里的秘密》,曝光用工业明胶生产药用胶囊。工业明胶中重金属铬(Cr
- 用同位素32P标记某一噬菌体的双链DNA分子,让其侵入大肠杆菌繁殖,最后释放出200个后代,则后代中有32P的噬菌体占总
- 1.下列各句中划线成语的使用,全都正确的一项是 ① 国女排时隔12年再次夺得奥运会冠军,女排姑娘们太了不起!郎指导太给力
- 阅读下面的作品,完成后面题目。 千古兰亭 祝 勇 王羲之不会想到,他的《兰亭序》,居然发起了一场浩浩荡荡的临摹和刻拓运
- 含CuCl2和HCl的100g混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液,参加反应的NaOH溶液质量与生成沉
- 某展室有9个展台,现有3件展品需要展出,要求每件展品独自占用1个展台,3件展品所选用的展台既不在两端又不相邻,且3件展品
- He decided to _________(捐献)all his books to the Hope Project
- 如图所示 .在磁感应强度为0.2T 的匀强磁场中 , 导体棒 AB 在金属框架上以 l0m/s 向右匀速滑动 , 金属框
- 如图所示,装置气密性良好,弹簧夹处于关闭状态.挤压胶头滴管加入液体,一段时间后,打开弹簧夹,能使气球a明显鼓起的是()试
- 将纯锌片和纯铜片插入同浓度的稀硫酸中一段时间,下列叙述正确的是 A. 甲中铜片是正极,乙中铜片是负极 B. 甲中铜
- 网络流行歌曲龚琳娜的《忐忑》,被大家称为“神曲”,是以五声音阶的复杂重叠,中国传统声乐技巧的夸张变形来创作的。龚琳娜在演
- 若点A(n,2)与点B(-3,m)关于原点对称,则n-m=( ) A.-1 B.-5 C.1
- The medical team __________(由……组成) ten nurses and three doct
- 阅读下列材料,回答问题:材料一:河南省地势西高东低,平原多分布在京广铁路以东,山地、丘陵主要分布在豫西北、豫西和豫南一带
- —Why don't you join us for breakfast? —Sure! ________ A.Goo
- 某工件的三视图如图2所示,现将该工件通过切割,加工成一个体积尽可能大的正方体新工件,并使新工件的一个面落在原工件的一个面
- --- can you see in the picture? ---Somebirds.
- 一段旅程的结束意味着新的开始,一次小小的转折也同样意味着新的开始。心情转变是开始,误会消除也是开始……在迈向开始的瞬间,
- 各类发电厂,我们使用的各种电池,工作时都是把不同形式的能转化为 能,而各种用电器工作时,又把 能转化





 中的物质
中的物质