2015-2016学年山东省青岛市即墨市创新学校高三下学期月考化学试卷(3月份)
2015-2016学年山东省青岛市即墨市创新学校高三下学期月考化学试卷(3月份)
教材科目:化学
试卷分类:高三下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在同温同压下,下列各组热化学方程式中△H2>△H1的是( )
A . 2H2(g)+O2(g)═2H2O(g),△H1; 2H2(g)+O2(g)═2H2O(l),△H2
B . S(s)+O2(g)═SO2(g),△H1; S(g)+O2(g)═SO2(g),△H2
C . C(s)+
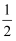 O2(g)═CO(g),△H1; C(s)+O2(g)═CO2(g),△H2
D . H2(g)+Cl2(g)═2HCl(g),△H1; O2(g)═CO(g),△H1; C(s)+O2(g)═CO2(g),△H2
D . H2(g)+Cl2(g)═2HCl(g),△H1; 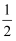 H2(g)+ H2(g)+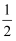 Cl2(g)═HCl(g),△H2 Cl2(g)═HCl(g),△H2
|
|
| 2. 单选题 | 详细信息 |
|
X元素最高价氧化物对应的水化物为H3XO4 , 则它对应的气态氢化物为( )
A . HX
B . H2X
C . XH4
D . XH3
|
|
| 3. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 可逆反应在其他条件不变时,升高温度,可以减小反应的活化能,加快反应速率
B . S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表一个电子
C . 氮原子的第一电离能低于氧原子的第一电离能,因为氮比氧非金属性弱
D . Fe3+ 比Fe2+稳定,因为Fe3+价电子构型是3d5 , d亚层处于半充满状态,稳定
|
|
| 4. 单选题 | 详细信息 | |||||||||||||||||||||||||||
|
根据表中八种短周期元素的有关信息判断,下列说法错误的是( )
A . 元素②⑥形成的化合物具有两性
B . 元素②气态氢化物的沸点小于元素⑤气态氢化物的沸点
C . 元素⑤对应的离子半径大于元素⑦对应的离子半径
D . 元素④的最高价氧化物的水化物比元素⑤的最高价氧化物的水化物酸性强
|
||||||||||||||||||||||||||||
| 5. 单选题 | 详细信息 |
|
下列反应的离子方程式,正确的是( )
A . 用小苏打治疗胃酸过多:CO
 +2H+═CO2↑+H2O
B . AlCl3溶液中加入足量的氨水:Al3++3OH﹣═Al(OH)3↓
C . 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+
D . 铝与浓氢氧化钠溶液反应:2Al+2OH﹣+2H2O═2AlO +2H+═CO2↑+H2O
B . AlCl3溶液中加入足量的氨水:Al3++3OH﹣═Al(OH)3↓
C . 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+
D . 铝与浓氢氧化钠溶液反应:2Al+2OH﹣+2H2O═2AlO  +3H2↑ +3H2↑
|
|
| 6. 单选题 | 详细信息 |
|
若NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 0.1molNa2O2中含有的离子数为0.4NA
B . 利用氧化还原反应原理制取1mol氧气,转移的电子数一定为4NA
C . 7.1g氯气与足量NaOH溶液反应电子转移数为0.2NA
D . 0.1mol氯气与金属铁完全反应时,转移电子数为0.2NA
|
|
| 7. 单选题 | 详细信息 |
|
1.52g铜镁合金完全溶解于足量的浓硝酸中,得到NO2气体1344mL (标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,发现金属离子全部沉淀,下列说法不正确的是( )
A . 该合金中铜与镁的物质的量之比是2:1
B . 可得到2.54 g沉淀
C . 如果是铜铝合金,则产生的NO2 的体积不会是1344mL
D . 恰好全部沉淀时,加入NaOH溶液的体积是600 mL
|
|
| 8. 单选题 | 详细信息 |
|
下列实验操作或对实验事实的描述正确的是( )
A . 欲将蛋白质从水中析出而又不改变它的性质,应加入CuSO4溶液
B . 乙醇可以被氧化为乙酸,二者都能发生酯化反应
C . 淀粉溶液中加入一定量稀硫酸,共热一段时间后,向溶液中加入新制氢氧化铜悬浊液并加热煮沸,未见红色固体产生,证明淀粉没有发生水解
D . 可用NaOH溶液除去混在乙酸乙酯中的乙酸
|
|
| 9. 单选题 | 详细信息 |
|
今年,中国女科学家屠呦呦获得诺贝尔奖.她获奖理由是:“因为创制新型抗疟药﹣﹣青蒿素和双氢蒿素,挽救了全球特别是发展中国家的数百万人的生命.”已知结构如图所示,则下列说法正确的是( )
A . 青蒿素与维生素C一样易溶于水工作
B . 所有碳原子都可能在同一平面上
C . 青蒿素晶体为分子晶体,其化学式为C15H22O5
D . 含有酯基,在胃酸作用下能水解,其水解产物能使氯化铁溶液显紫色
|
|
| 10. 多选题 | 详细信息 |
|
X元素的阳离子和Y元素的阴离子具有与氖原子相同的电子层结构,下列说法正确的是( )
A . 原子序数X<Y
B . 原子半径X>Y
C . 原子的最外层电子数X>Y
D . 元素的最高正价X<Y
|
|
高中化学 试卷推荐
- 备考2021年高考化学二轮专题 第2讲 非金属元素及其化合物
- 山东省济南市2021年高考化学三模试卷
- 北京市房山区2020-2021学年高二上学期期末考试化学试题
- 广东省惠州市2022届高三第一次模拟考试化学试题
- 四川省成都市蓉城名校联盟2020-2021学年高二下学期期末联考化学试题
- 上海市徐汇区2021年高考化学二模试卷
- 河南省南阳市六校2021-2022学年高二上学期第一次联合测试化学试题
- 江苏省苏州市吴中区2020-2021学年高二上学期化学期中考试试卷
- 山东省威海市威海文登区2020-2021学年高三上学期化学期中考试试卷
- 吉林省白山市2021-2022学年下学期高三第一次模拟考试理综化学试题
- 吉林省长春市榆树高级中学2020-2021学年高一上学期化学期中考试试卷
- 山东省德州市2021-2022学年高一上学期期末考试化学试题
最近更新
- 与0.3mol H2O含有相同氢原子数的是 A.0.3molHNO3
- 某物质在纯氧中燃烧生成了氮气和水蒸气,该物质一定含有 A. 氮元素和氧元素 B. 氢元素和
- 自2007年末发生金融危机以来,美元对主要贸易伙伴的一篮子货币的汇价共下跌了15%左右。对于美国来说,美元汇价下跌会产生
- 下列词语中,字形和加点字的读音全都正确的一项是 A.湛蓝 挑肥捡瘦 渐染(jiàn)
- 将0.1 mol・L-1CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起A.溶液的pH增加
- 据图回答下列问题: (14分)(1)图中所示的地区为___________________________(省区) (2
- 中国的立党之本、执政之基、力量之源是( )。
- 1.下列各句中,没有语病的一句是( ) A.一切儿童文学作品都应该永远持着守护童年的立场,遵循儿童思维发展规律,富
- 空间四边形中,互相垂直的边最多有( ) A、1对 B、2对 C、3对 D、
- 生态系统一般都包括( ) A.生产者、消费者、分解者 B.生产者和非生物部分 C.生
- 下列药品置于空气中很容易变质(括号内的物质是变质后的物质),其中不是因为氧化还原反应而变质的是( )A、Na2SO3(
- 债券与股票的共同点是 ①都是能获得一定收益的有价证券 ②都是筹集资金的手段 ③受益权相同
- (2009·舟山中学)下列词语中加点的字的读音全部正确的一组是( ) A.禅宗(chán) 伫立(zhù)
- 一代伟人在《沁园春·雪》中写到:“北国风光,千里冰封,万里雪飘”,雪的形成这种景象的主要物态变化是
- 若NA为阿伏加德罗常数的值,下列说法正确的是( ) A.NA个 Fe(OH)3 胶体粒子的质量为 107g B.CO2
- 下列由地球自转所产生的现象是( )A.昼夜 B.季节的
- 甲、乙两人,分别沿0°和180°经线同时从北极点出发,向南行进,速度相同,产生的现象是( ) A.他们之间始终保持等
- The Queen’s English is now sounding less upper-class, a
- 下图表示在高等动物的配子生成和融合过程中,细胞核中DNA的相对数量随染色体动态而发生的变化。请据图回答问题:(1)图中I
- The football match between Class One and Class Three was goi




