山东省临沂市兰陵县2020-2021学年高一下学期化学期中考试试卷
山东省临沂市兰陵县2020-2021学年高一下学期化学期中考试试卷
教材科目:化学
试卷分类:高一下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高一下学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
生产、生活中的化学知识随处可见。下列说法错误的是( )
A . 橡胶硫化的过程中发生了化学反应
B . 碳纳米管有优良的电学性能,可用于生产电池
C . 5G芯片“巴龙5000”的主要材料是高纯度的二氧化硅
D . 陶瓷化学性质稳定,具有耐酸碱腐蚀、抗氧化等特点
|
|
| 2. 单选题 | 详细信息 |
|
下列叙述错误的是( )
A . 酸雨的pH小于5.6
B . 能用浓硫酸干燥二氧化硫气体
C . 铁粉与硫粉反应生成硫化亚铁是放热反应
D . 锌锰干电池中,锌筒作正极
|
|
| 3. 单选题 | 详细信息 |
|
定容容器中发生反应I2(g)+H2(g)
 2HI(g),下列措施不能提高其反应速率的是( ) 2HI(g),下列措施不能提高其反应速率的是( )
A . 升高温度
B . 使用催化剂
C . 充入稀有气体,增大体系压强
D . 增加I2和H2的起始量
|
|
| 4. 单选题 | 详细信息 |
|
a、b、c、d、e分别是Cu、Ag、Fe、Al、Mg五种金属中的一种。已知:
⑴a、c、e均能与稀硫酸反应放出气体; ⑵b与d的硝酸盐反应,置换出单质d; ⑶c与强碱反应放出气体; ⑷c、e在冷浓硫酸中发生钝化。 由此可判断a、b、c、d、e依次为( )
A . Fe、Cu、Al、Ag、Mg
B . Al、Cu、Mg、Ag、Fe
C . Mg、Cu、Al、Ag、Fe
D . Mg、Ag、Al、Cu、Fe
|
|
| 5. 单选题 | 详细信息 |
|
下列有关化学反应速率和限度的说法中,错误的是( )
A . 实验室用H2O2分解制O2 , 加入MnO2后,反应速率明显加快
B . 在金属钠与足量水反应中,增加水的量能加快反应速率
C . 2SO2+O2⇌2SO3反应中,SO2的转化率不能达到100%
D . 实验室用碳酸钙和盐酸反应制取CO2 , 用碳酸钙粉末比块状反应要快
|
|
| 6. 单选题 | 详细信息 |
|
如图所示装置,开始时夹子处于关闭状态,将液体A滴入试管②中与气体B充分反应,打开夹子,可发现试管①中的水立刻沸腾了。则液体A和气体B的组合不可能是( )
A . 氢氧化钠溶液、氯化氢
B . 氢氧化钠溶液、一氧化碳
C . 水、二氧化硫
D . 水、二氧化氮
|
|
| 7. 单选题 | 详细信息 | ||||||||||||||||||||
|
用如图所示装置进行实验,下列实验现象的解释不合理的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 8. 单选题 | 详细信息 |
|
某学生用纯净的Cu与50mL过量浓HNO3反应制取NO2 , 实验结果如图所示。(气体体积为标准状况,且忽略溶液体积变化)。下列说法正确的是( )
A . OA段比AB段反应速率快
B . AB段反应速率加快,仅因为产物有催化作用
C . OC段用浓硝酸表示的反应速率为0.2 mol·L-1·min-1
D . 向反应体系中加入固体KNO3对反应速率无影响
|
|
| 9. 单选题 | 详细信息 |
|
根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化情况,判断下列说法正确的是( )
A . 该反应为放热反应
B . 2 mol氮原子结合生成N2(g)时需要放出946kJ能量
C . 1molNO(g)分子中的化学键断裂时需要放出632kJ能量
D . NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
|
|
| 10. 单选题 | 详细信息 |
|
绿色化学的原子经济性要求是在生产中所有原子均转化为产物,没有副产物。以下反应最符合绿色化学原子经济性要求的是( )
A . 将NO与O2按4:3的比例充分混合通入足量水中制备硝酸
B . 利用SO2与O2反应制SO3
C . 以铜和浓硝酸为原料生产硝酸铜
D . 用SiO2制备高纯硅
|
|
高中化学 试卷推荐
- 四川省内江市2020-2021学年高一下学期期末检测题化学(文)试题
- 备考2021年高考化学二轮专题 第4讲 反应热
- 广东省广州市2021年高考化学二模试卷
- 冲刺2021高考化学押题训练(十三)基本实验操作和分析
- 广东省潮州市2021年高考化学二模试卷(5月)
- 天津市部分区县2020-2021学年高三上学期化学期中考试试卷
- 吉林省长春市榆树市第一高级中学2020-2021学年高三上学期化学10月月考试卷
- 四川省自贡市2022届高三下学期第三次诊断性考试理综化学试题
- 河南省信阳市2021年高考化学二模试卷
- 四川省成都市2021年高考化学三模试卷
- 河北省承德市2020-2021学年高一下学期期末考试化学试题
- 山东省潍坊市2020-2021学年高二上学期化学期中考试试卷
最近更新
- 下列排列有错误的是 A.稳定性:HF>HCl>HBr>HI B.酸性:H4SiO4<H3PO4<H2SO4<HClO4
- 如图装置中,小试管内为红墨水,带有支管的U型管中盛有pH=4的雨水和生铁片。经观察,装置中有如下现象:开始时插在小试管中
- 我国建国之初的三大外交政策是当时中国的对外战略,奠定了整个50年代外交政策的基础。三大外交政策总的倾向是 A.努
- 关于声现象的说法中正确的是 A、声音可以在气体和液体中椽笔 B、声音在真空中的传播速
- 在R上定义运算⊙:a⊙b=ab+2a+b,则满足x⊙(x-2)<0的实数x的取值范围为() A.(0,2) B.(-2,
- 设想把一物体放在某行星的中心位置,则此物体与该行星间的万有引力是(设行星是一个质量分布均匀的标准圆球)( )A.零B.
- You can shut your eyes to the fact_______he did was right. A
- 下列实验现象的描述中,正确的是( ) A. 铁丝在氧气中燃烧,火星四射,生成黑色固体
- 由劳动和社会保障部起草修订的《工资条例》将在年内出台,全社会呼唤已久的工资协商制度、同工同酬等保障劳动者权益的条款将被纳
- 质量守恒定律是自然界最基本的规律之一。下列装置及实验(天平未画出)能用来验证质量守恒定律的是 ()图Z5-1
- Books are my best friends. They give me k________ and make m
- (9分)(1)常温下,有0.1mol/L的氨水和0.1mol/L的氢氧化钠溶液,回答下列问题:①pH 值:氨水 氢
- 图1-2-19所给出的是计算S=1-+-+…+-的程序框图,请将框图内所缺的式子填充,并写出程序.图1-2-19
- 下图是明清古建筑中的一幅牌匾,与它有关联的中国古代政治制度是()A.分封制 B.宗法制 C.三省六部制 D.内阁制
- 已知一植株的基因型为AABB,周围虽生长有其他基因型的玉米植株,但其子代不可能出现的基因型是( ) A.AABB
- 风吹灭蜡烛,主要灭火原理是() A.隔绝空气 B.降低可燃物的着火点 C.消除可燃物 D.使可燃物温度降到着火点以下
- –Big animals can be a lot of trouble. Maybe you should get a
- 由函数y=图像得到直线y=,就是将直线y=( )A.向上平移2个单位B.向右平移2个单位C.向上平移个单位D
- 下列物质中能导电的是 ①固体食盐 ②氨水 ③明矾④铂丝⑤蔗糖 ⑥氯化氢⑦液氨⑧磷酸水溶液 A.①④⑥⑧
- 曾爱国是一位生活在19世纪60年代的北京青年,他亲眼目睹了国家遭受列强入侵,便决定学习外语,以便为国尽一已之力。他应该进


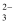 与Ba2+生成BaSO3沉淀
与Ba2+生成BaSO3沉淀




