高中化学人教版(2019)选择性必修1 第四章测试卷
高中化学人教版(2019)选择性必修1 第四章测试卷
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 填空题 | 详细信息 |
|
利用如图装置,可以模拟铁的电化学防护.
若X为铜,为减缓铁的腐蚀,开关K应置于 处.铁棒上发生的电极反应为,该种防护方法称为若X为锌棒,开关K置于处,铁棒上的电极反应为该电化学防护法称为.
|
|
| 2. 综合题 | 详细信息 |
|
如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:
|
|
| 3. 单选题 | 详细信息 |
|
下列是教材中常规电化学示意图,其标注完全正确的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 4. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则ΔH<0
B . 铁片镀锌时,铁片与外电源的正极相连
C . 以熔融NaCl为电解质进行电解冶炼钠,熔融体中Na+向阳极移动
D . t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)
 NO(g)+SO3(g),通入少量O2 , NO(g)+SO3(g),通入少量O2 ,  的值及SO2转化率不变 的值及SO2转化率不变
|
|
| 5. 单选题 | 详细信息 |
|
如图是家用消毒液发生器,下列分析错误的是( )
A . 碳棒a是阴极
B . 反应中碳棒b附近溶液显酸性
C . 电子由碳棒a经溶液流向碳棒b
D . 发生器中的总反应:NaCl+H2O
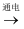 NaClO+H2↑ NaClO+H2↑
|
|
| 6. 单选题 | 详细信息 |
|
全世界每年因钢铁锈蚀造成了巨大的损失,下列有关说法错误的是( )
A . 钢铁腐蚀时化学能不能全部转化为电能
B . 钢铁腐蚀的负极反应式为Fe-2e-=Fe2+
C . 如图所示,将导线与金属锌相连可保护地下铁管
D . 如图所示,将导线与外接电源的正极相连可保护地下铁管
|
|
| 7. 单选题 | 详细信息 |
|
下列有关 2 个电化学装置的叙述错误的是( )
A . 图Ⅰ,在不改变总反应的前提下,可用 Na2SO4 替换 ZnSO4 , 用石墨替换 Cu 棒
B . 图Ⅰ,电流形成的完整过程是:负极 Zn-2e-=Zn2+ , 电子经导线流向正极,正极 Cu2++2e-=Cu
C . 图Ⅱ,通电后向两极滴加酚酞,左侧变红
D . 图Ⅰ,盐桥中 Cl-向左侧移动,图Ⅱ,溶液中 Cl-向右侧移动
|
|
| 8. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||
|
某小组同学利用原电池装置探究物质的性质。资料显示:原电池装置中,负极反应物的还原性越强,或正极反应物的氧化性越强,原电池的电压越大。
|
|||||||||||||||||||||||||||
| 9. 综合题 | 详细信息 |
|
化学电池的发明,是贮能和供能技术的巨大进步。
|
|
| 10. 单选题 | 详细信息 |
|
金属铬和氢气在工业上都有重要的用途。已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( )
A . 盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B . 理论上1molCr溶解,盐桥中将有2molCl-进入左池,2molK+进入右池
C . 此过程中H+得电子,发生氧化反应
D . 电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
|
|
高中化学 试卷推荐
- 2017年江苏省高考化学试卷 (正式版)
- 四川省绵阳市2017-2018学年高三理综-化学二模考试试卷
- 2017-2018学年高中化学新人教版必修二第二章化学反应与能量2.1化学能与热能
- 四川省泸州市2019-2020学年高一下学期化学期末考试试卷
- 安徽省芜湖市示范高中2020年高考理综-化学5月模拟试卷
- 2017_2018学年高中化学人教版选修四 第四章电化学基础4.4金属的电化学腐蚀与防护
- 浙江省杭州市塘栖中学2019-2020学年高一下学期化学3月月考试卷
- 江苏省南通市通州区2019-2020学年高一下学期化学期末考试试卷
- 福建省南平市2018-2019学年高三上学期化学期末考试试卷
- 高中化学人教版 必修1 第二章 化学物质及其变化 2.离子反应 离子反应及其发生的条件
- 2015-2016学年江苏省无锡市江阴市四校联考高一下学期期中化学试卷
- 人教(新课标)高中化学一轮复习:专题10化学反应速率与化学平衡
最近更新
- 综合运用。(8分) 2013年4月23日,是第18个“世界读书日”,学校为此举行了“好读书,读好书”的综合性学习活动。请
- 在一条离体神经纤维的中段施加电刺激,使其兴奋。下图表示刺激时膜内外电位变化和所产生的神经冲动传导方向(横向箭头表示传导方
- 表甲为某区域的空间数字模型,每个栅格的面积为250平方米,图中r表示林地,s表示滩地,p表示水体;表乙中的数值表示该区域
- 古诗文默写。(1)古文默写。二十四桥仍在,波心荡,____________。念桥边红药,____________!(姜夔
- 陆游《卜算子·咏梅》中表达自己虽遭不幸,但仍保持“质本洁来还洁去”的高风亮节的句子是 , 。
- 氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应,如右图所示,关于三个反应的叙述中不正确的是 A.都是化
- 阅读下面文字,完成下列小题。 “内圣外王”之说不符孔子圣人规 现代新儒家喜以“内圣外王”四字综括孔子之道及其所开创的儒家
- 设f(x)是定义在区间U上的增函数,且f(x)>0,则下列函数:①y=1-f(x);②y=;③(x);④y=-中为
- 已知,,则的最小值为 .
- 下列结构中,与小肠吸收营养物质无直接关系的是( ) A.小肠粘膜有皱襞和小肠绒毛 B.
- 我国宪法规定:“国家尊重和保障人权”。下列关于人权问题的阐述正确的是( )①尊重和保障人权,是发展社会主义民主政治的
- 有关我国西北地区地理特征的叙述,正确的是( )A .干旱是西北地区自然环境的主要特征B .制约西北地区农业生产发展的因素
- 近代《申报》曾评述道:“这是华北战争以来的第一次胜利,也是国共宣布合作以后的第一个喜讯。我们的抗战是全面的持久的抗战。…
- 阅读下面这首唐诗,然后回答问题。(8分) 晚 次 鄂 州 唐·卢纶 云开远见汉阳城,犹是孤帆一日程。 估客[1]昼眠知
- 在实验设计中,下列选项中不能作为一组对照的是 ( )A、25℃和0℃ B、有光和无光 C、有空气和无空气 D、温度和水分
- 斯塔夫里阿诺斯在《全球通史》中说:“(雅典)最初是实行君主政体,以后让位于由九个 执政官主持的寡头政治。这九个执政官是
- A2+B2=2AB的反应历程可以看作如下(△H表示该过程的能量变化): Ⅰ.A2=A+A △H1 Ⅱ.B2=B+B
- 下列搭配中,正确的是( ) A.西亚﹣﹣白种人﹣﹣佛教﹣﹣发展中国家 B.巴西﹣﹣黄
- 近来,根据革命历史创作的电视剧,如《潜伏》、《人间正道是沧桑》、《我的兄弟叫顺溜》的播出屡创收视奇迹。这表明 A.人们在
- 大河流域以其独特的地理环境孕育了人类璀璨的文明。下列不属于大河流域孕育的古代人类文明是 A.古印度文明 B.












