安徽省安庆市2021年高考理综-化学一模试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
化学在日常生活和生产中有着重要的作用。下列有关说法正确的是( )
A . 南朝《竹林七贤与启荣期》砖画砖块的主要成分是二氧化硅
B . 地沟油不能食用,但可以用来制肥皂或生物柴油,实现变废为宝
C . 84消毒液、过氧乙酸、医用酒精可灭活新冠病毒均利用了强氧化性
D . 纳米级的铁粉能通过吸附作用除去水体中的Cu2+、Hg2+等重金属离子
|
|
| 2. 单选题 | 详细信息 | |||||||||||||||
|
用下列实验装置能达到相关实验目的的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 3. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 25℃,pH=13的1.0LBa(OH)2溶液中含有OH-的数目为0.2NA
B . 60gSiO2晶体中Si—O键数目为2NA
C . 在K37ClO3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若有212g氯气生成,则反应中转移电子的数目为5NA
D . 加热条件下,20mL10mol•L-1浓硝酸与足量铜反应转移电子数为0.1NA
|
|
| 4. 单选题 | 详细信息 |
|
《新型冠状病毒肺炎诊疗方案(试行第七版)》中指出,洛匹那韦(Lopinavir)与氯喹类药物均可用于治疗新冠肺炎。洛匹那韦(Lopinavir)(图1)和羟基氯喹(图2)的结构分别如图所示,对这两种有机化合物描述正确的是( )
A . 洛匹那韦是一种人工合成的蛋白质
B . 洛匹那韦能够发生酯化、加成、氧化、还原反应
C . 羟基氯喹的分子式为C18H24N3OCl
D . 羟基氯喹分子苯环上的一氯代物有5种
|
|
| 5. 单选题 | 详细信息 |
|
主族元素Q、W、X、Y、Z的原子序数均不大于20。化合物ZW2与水剧烈反应,生成一种强碱和一种可燃性气体单质,Q与X同族,且X的最外层电子数是内层电子数的3倍,常温下,Y的单质能溶于Q的最高价氧化物对应的水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是( )
A . 简单离子半径:Z>Q>X>Y
B . 工业上用电解相应氯化物冶炼Y单质
C . Q与X形成的化合物中,每个原子最外层均满足8电子结构
D . 化合物ZW2中只含有离子键
|
|
| 6. 单选题 | 详细信息 |
|
锂—铜空气燃料电池(图1)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH- , 用该电池电解含有尿素[CO(NH2)2]的碱性溶液,用于废水处理和煤液化供氢,其装置如图2所示。装置中c、d均为惰性电极,隔膜仅阻止气体通过,电解时,c极接b极。下列说法错误的是( )
A . 放电时,b极的电极反应式为:O2+4e-+2H2O=4OH-
B . 电解时,理论上标准状况下,有33.6L O2参与反应时,c电极区可产生22.4L N2
C . 电解一段时间后,d电极区pH增大
D . 图1整个反应过程,Cu起了催化剂的作用
|
|
| 7. 单选题 | 详细信息 |
|
25℃时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol/L,lgc(CH3COOH)、lgc(CH3COO-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。已知Ka为CH3COOH的电离常数,下列说法正确的是( )
A . 曲线1为lgc(OH)随pH变化的曲线
B . N点时,pOH=14-lgKa
C . 该体系中,c(CH3COO-)=
 mol/L
D . O点时,c(CH3COOH)=c(CH3COO-) mol/L
D . O点时,c(CH3COOH)=c(CH3COO-)
|
|
| 8. 实验探究题 | 详细信息 |
|
亚氯酸钠(NaClO2)是一种重要的杀菌消毒剂,其作用原理是在酸性条件下发生反应生成ClO2。已知NaClO2受热、见光均不稳定。实验室制备NaClO2的装置如图所示:
|
|
| 9. 综合题 | 详细信息 |
|
氧化钪可制作成氧的传感器陶瓷、固体电解质等特种材料,在现代工业中用途广泛。工业上用钒钛磁铁矿选矿后所得的钪精矿制备Sc2O3的流程图如图所示:
|
|
| 10. 综合题 | 详细信息 | |||||||||||||||
|
氮氧化物和SO2是大气主要污染物,研究它们的转化关系有利于防治污染。
|
||||||||||||||||
- 上海市静安区2018-2019学年高考化学一模考试试卷
- 2015-2016学年四川省成都市龙泉中学高一下学期月考化学试卷(4月份)
- 四川省南充市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年江西省上饶市上饶县中学高一上学期第二次月考化学试卷
- 2016-2017学年黑龙江、吉林两省八校高一上学期期中化学试卷
- 北京市101中学2019-2020学年高三下学期化学第三次月考试卷
- 广西玉林市容县2016-2017学年高一下学期化学期末考试试卷
- 2016-2017学年山东省济南中学高二下学期期中化学试卷(理科)
- 上海市崇明区2018-2019学年高考化学一模(期末)考试试卷
- 2016-2017学年陕西省宝鸡市岐山县高二上学期期中化学试卷(理科)
- 内蒙古商都县高级中学2017-2018学年高一上学期化学期中考试试卷
- 浙江省丽水市2018-2019学年高二下学期化学期末考试试卷
- Can you speakEnglish,Mr Chen? —Yes,but only . A.little
- Two hours from the tall buildings of Manhattan and Philade
- 2007年7月,大阪大学松永幸大等研究人员在染色体中找到了一种使姐妹染色单体连接成十字形的关键蛋白质,并将其命名为“AS
- 在现在农村的小块田地里,你偶尔仍能看到农民用铁犁牛耕(或用驴耕)耕作的场景。中国古代农民用铁犁牛耕最早出现在 A.夏朝商
- (本小题满分8分)初中生对待学习的态度一直是教育工作者关注的问题之一.为此某市教育局对该市部分学校的八年级学生对待学习的
- 下列操作中,后者最终能被漂白的是 A.将H2O2加入到KMnO4溶液中 B.将足量SO2通人紫色石蕊试液中
- 读图,回答。图中所示范围从东到西自然景观的变化,属于从内蒙古到新疆自然景观变化示意图 A.从赤道到两极的地域分异
- 如图3所示,L1和L2是两个规格相同的小灯泡,L是一个自感系数相当大的线圈,其电阻与R相同.由于存在自感现象,在开关S
- 在《研究平抛物体运动》的实验中:某同学记录了A、B、C三点,取A点为坐标原点,建立了右图所示的坐标系。平抛轨迹上的这三点
- 2010年5月17日至19日,党中央、国务院在北京召开新疆工作座谈会,所有政治局常委及委员全部参加会议。如此高规格的会议
- “配制溶质质量分数一定的溶液”是我市初中学生化学实验的考查内容之一。请你仔细阅读并结合平时实验的实际操作,回答有关问题:
- 《光明日报》载文指出,人与社会是不可分割的,全面发展的社会要求全面发展的人,并为人的全面发展创造条件。过去我们往往把人的
- 如图,已知AB∥CD,∠B=65°,CM平分∠BCE,∠MCN=90°,求∠DCN的度数.
- 如图所示的游戏情境,小孩将毽子向上踢出,表明力可以改变物体的______;毽子被踢出后,由于________会继续向上运
- 下列有机物命名正确的是 A.2—甲基—3—乙基丁烷 B.2—氯
- 南非的开普敦(南半球,地中海气候)与我国南京的气候相比较,说法正确的是 A.两地都雨热同期 B.开普敦气温
- 下列实验设计和结论相符的是( )A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 B.某气体能使湿
- 5细胞内很多化学反应都是在生物膜上进行的,如图表示真核细胞中4种生物膜上发生的化学变化示意图,相关叙述不正确的是()
- 阅读下列德国与美国失业率变化图,你认为造成两国20世纪二三十年代高失业率的主要原因是( )A.经济大危机
- 原核细胞和真核细胞最明显的区别在于[ ] www.k@s@A.有无核物质 B.有无细胞质









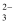 =2I+S4O
=2I+S4O  )。该样品中NaClO2的质量分数为(用含a、c、V的代数式表示)。
)。该样品中NaClO2的质量分数为(用含a、c、V的代数式表示)。
 和Fe3+ , Ti2O
和Fe3+ , Ti2O 
 2NO2(g) △H=-113.0kJ•mol-1
2NO2(g) △H=-113.0kJ•mol-1



